ar
الأسماء في صفحات التنقل

El virus del Zika[1] (ZIKV) ye un virus del xéneru Flavivirus, de la familia Flaviviridae, grupu IV del orde ensin clasificar que se tresmite pola picadura de mosquitos vectores del xéneru Aedes.[2]
Nos seres humanos produz la fiebre del Zika o enfermedá de Zika, que conozse dende la década de 1950 como proveniente de la rexón ecuatorial que toma d'África a Asia. El so nome provien del monte Zika, cerca de Entebbe (n'Uganda), onde s'aislló per primer vegada esti virus, en 1947.[3]
En 2014 el virus arrobinar al este al traviés del océanu Pacíficu escontra la Polinesia Francesa, y dempués escontra la Isla de Pascua pa llegar en 2015 y 2016 a América Central, el Caribe y América del Sur, onde'l biltu epidémicu del Zika algamó niveles pandémicos.[4][5] La enfermedá produz síntomes similares a formes leves de dengue, el so tratamientu consiste básicamente nel reposu, y na actualidá nun esisten melecines o vacunes pa la so prevención.[6][7][7] La fiebre del Zika ta rellacionada con otres enfermedaes similares, como la fiebre mariello y la fiebre del Nilo Occidental, que tamién son producíes por otros Flavivirus tresmitíos por mosquitos.[6] Esiste la posibilidá d'un venceyu ente la fiebre del Zika y la microcefalia en naciellos de madres infectaes.[8][9]
Al igual qu'otros virus del so xéneru Flavivirus, el virus del Zika ye un virus envueltu con cápside icosaédrica, y el so xenoma ye ARN non segmentado, monocatenario positivu. Ta estrechamente rellacionáu col virus Spondweni y ye unu de los dos virus nel clado de los virus Spondweni.[10][11]
El virus foi aislláu per primer vegada en 1947, nun macacu Rhesus proveniente del monte de Zika n'Uganda. En 1968 foi aislláu per primer vegada en seres humanos, a partir d'una amuesa llograda en Nixeria.[12] De 1951 a 1981, reportóse evidencia d'infeición en seres humanos n'otros países africanos tales como la República Centroafricana, Exiptu, Gabón, Sierra Lleona, Tanzania, y Uganda, según en delles partes d'Asia incluyendo India, Indonesia, Malasia, Filipines, Tailandia, y Vietnam.[12]
Créese que la patoxénesis viral empieza cola infeición de les célules dendríticas cercanes al sitiu de la inoculación, siguíu pola diseminación a los nódulos linfáticos y la riega sanguínea.[10] Xeneralmente, los Flavivirus retrucar na citoplasma, pero atopáronse antígenos de virus del Zika dientro del nucleu celular.[13]
Esisten dos llinaxes de virus del Zika, el llinaxe africanu y el llinaxe asiáticu.[14] Dellos estudios filoxenéticos indiquen que'l virus que ta espandiéndose pol continente americanu ta más estrechamente rellacionáu con cepes provenientes de la Polinesia Francesa.[14] Yá se publicaron les secuencies completes del xenoma del virus.[15] Dellos estudios preliminares d'estos afayos demuestren un posible cambéu nel funcionamientu del codón de la proteína non estructural 1, lo cual podría aumentar la tasa de replicación viral n'humanos.[16]
El virus del Zika ye tresmitíu por mosquitos con actividá diurna y foi aislláu a partir de delles especies nel xéneru Aedes, como l'A. aegypti, amás de mosquitos arborícoles como l'A. africanus, A. apicoargenteus, A. furcifer, A. hensilli, A. luteocephalus, y A. vitattus. Los estudios amuesen que'l periodu d'incubación estrínsecu nos mosquitos ye aprosimao de 10 díes.[12] Los güéspedes vertebraos del virus son principalmente monos y seres humanos.[17]
El potencial del riesgu d'infeición col virus del Zika puede tar llindáu a la distribución de les especies de mosquitos que lu tresmiten (el so vector epidemiolóxicu). La distribución mundial del portador más conocíu del virus Zika, el Aedes aegypti, ta espandiéndose debíu al comerciu global y los viaxes.[18] La distribución del Aedes aegypti ye agora la más estensa enxamás rexistrada, práuticamente en tolos continentes, incluyíes América del Norte y la periferia d'Europa.[19]
En 2009, Brian Foy, un biólogu de la Universidá Estatal de Coloráu nos Estaos Xuníos, tresmitió sexualmente'l virus del Zika a la so esposa. Foy visitara Senegal pa estudiar les poblaciones de mosquitos, y picáronlu en delles ocasiones. Pocos díes dempués de tornar a los Estaos Xuníos, contraxo fiebre del Zika, pero non antes de tener rellaciones sexuales ensin proteición cola so esposa. Dempués d'esto, ella tamién amosaría los síntomes de la infeición, inclusive fotosensibilidad. Foy ye la primer persona de la que se sabe que tresmitió por contautu sexual un virus que rique ser tresportáu por vectores a otru ser humanu.[20][21]
En 2015, detectóse'l ARN del virus del Zika nel líquidu amniótico de dos fetos, lo qu'indica que cruciaría la llibradura y podría causar la tresmisión vertical de la enfermedá d'una madre al so fíu non nato.[22] El 20 de xineru del 2016, científicos del estáu de Paraná en Brasil detectaron material xenético del virus del Zika na llibradura d'una muyer qu'albortó al so fetu por cuenta de microcefalia, lo cual confirma que'l virus ye capaz de cruciar la barrera placentaria.[23]
Los síntomes más comunes de la infeición col virus inclúin dolores de cabeza leves, eflorescencia o erupciones maculopapulares, fiebre, malestar xeneral, conxuntivitis y dolores articulares. El primer casu bien documentáu por infeición del virus del Zika describir en 1964; empezó con un dolor de cabeza leve y progresó hasta convertise nun sarapulláu maculopapular xuntu con fiebre y dolor de llombu. En dos díes, el sarapulláu empezó a menguar y al tercer día la fiebre venció pa solo quedar les erupciones. La fiebre del Zika considérase una enfermedá relativamente leve y llindada, y solo 1 de cada 5 persones van desenvolver los síntomes ensin aportar a fatal, anque'l verdaderu potencial como axente viral causante d'enfermedá ye desconocíu.[12]
Nun esisten vacunes o melecines preventives pal virus del Zika. Los síntomes pueden ser trataos con analxésicos como'l paracetamol, una y bones otros AINES como la aspirina solo tendríen de ser utilizaos en refugando infeición per dengue o otros Flavivirus, col fin d'amenorgar el riesgu de sangráu.[24]
Mientres la epidemia na Polinesia Francesa, confirmáronse 73 casos de síndrome de Guillain–Barré y otros carecimientos neurolóxicos, y abarrúntase que podríen ser entueyos del virus, anque nun hai estudios que lu confirmen.[17]
La microcefalia ye la dexeneración o malformación del celebru que determina la nacencia de neños con una cabeza de tamañu más pequeñu que'l normal y que n'ocasiones provoca la muerte. N'avientu del 2015, el Centru Européu pa la Prevención y Control d'Enfermedaes (ECDC) publicó un avisu sobre la posible asociación del virus del Zika con microcefalia conxénita.[25] Los datos suxuren que nos fetos de les muyeres infectaes pol virus mientres el primer trimestre del embaranzu esiste un riesgu alto de microcefalia; otres investigaciones indiquen qu'amás d'esi síndrome esti tipu de tresmisión vertical podría causar dañu cerebral.[26][27][28]
Na actualidá, esisten vacunes efectives contra munchos Flavivirus. Por casu, les vacunes contra la fiebre mariello, la encefalitis xaponesa y l'encefalitis tresmitida por cachiparros introducir na década de 1930, ente que la vacuna contra'l dengue haber sío apocayá.[29][30]
Los trabayos escontra'l desenvolvimientu d'una vacuna contra'l virus del Zika yá empezaríen, según el doctor Anthony Fauci, direutor del Institutu Nacional d'Alerxa y Enfermedaes Infeicioses de los Estaos Xuníos (NIAID).[31] El investigadores del NIAID yá tuvieron esperiencia previa al trabayar en vacunes contra enfermedaes similares como'l virus del Nilo Occidental, el virus chikunguña y el dengue.[31]
El tiempu necesariu pa desenvolver una vacuna efectiva, certificala y ponela en producción ye llargu y complexu. Los primeros pasos #llevar a cabu nel llaboratoriu ya inclúin pruebes n'animales, ensayos clínicos y les llicencies d'aplicación y aprobación riquíes.[32] Envalórase que podría llevar siquier unos 10 a 12 años el tener una vacuna efectiva contra'l virus del Zika disponible pal so usu.[33]
El virus del Zika (ZIKV) ye un virus del xéneru Flavivirus, de la familia Flaviviridae, grupu IV del orde ensin clasificar que se tresmite pola picadura de mosquitos vectores del xéneru Aedes.
Nos seres humanos produz la fiebre del Zika o enfermedá de Zika, que conozse dende la década de 1950 como proveniente de la rexón ecuatorial que toma d'África a Asia. El so nome provien del monte Zika, cerca de Entebbe (n'Uganda), onde s'aislló per primer vegada esti virus, en 1947.
En 2014 el virus arrobinar al este al traviés del océanu Pacíficu escontra la Polinesia Francesa, y dempués escontra la Isla de Pascua pa llegar en 2015 y 2016 a América Central, el Caribe y América del Sur, onde'l biltu epidémicu del Zika algamó niveles pandémicos. La enfermedá produz síntomes similares a formes leves de dengue, el so tratamientu consiste básicamente nel reposu, y na actualidá nun esisten melecines o vacunes pa la so prevención. La fiebre del Zika ta rellacionada con otres enfermedaes similares, como la fiebre mariello y la fiebre del Nilo Occidental, que tamién son producíes por otros Flavivirus tresmitíos por mosquitos. Esiste la posibilidá d'un venceyu ente la fiebre del Zika y la microcefalia en naciellos de madres infectaes.
Zika virusu — 1947-ci ildə müəyyən edilib. Onun daşıyıcısı "Aedes aegypti" adlı ağcaqanad növləridir.
Hamilə qadınlar üçün daha ciddi təhlükə yaratdığı deyilən bu virus, hələ doğulmamış körpənin beynində kiçilmə və fəsadlara, hətta ölümə belə yol aça bilər.[1]
Əlamətləri sırasına yüksək qızdırma, baş ağrısı, gözlərdə qızarma, qusma, səpmə, əzələ və oynaq ağrıları daxildir.
Hazırda dünyanın 21 ölkəsində bu virusun qeydə alındığı bildirilir. Latın Amerikası ölkələrinin hökumətləri virusun yayılmasının qarşısını almaq üçün mübarizəyə başlayıb.
Ümumdünya Səhiyyə Təşkilatı hesab edir ki, virus qərb yarımkürəsində sürətlə yayılacaq.
Vikianbarda Zika virusu ilə əlaqəli mediafayllar var.

Zika virusu — 1947-ci ildə müəyyən edilib. Onun daşıyıcısı "Aedes aegypti" adlı ağcaqanad növləridir.
El virus del Zika (ZIKV) [1] és un virus del gènere Flavivirus, família Flaviviridae, grup IV de la Classificació de Baltimore.[2] Té interès en medicina per produir la febre del Zika. La febre i el virus porten el nom del bosc de Zika, a Uganda, on el virus es va aïllar per primer cop el 1947.[3]
Les infeccions, conegudes com a febre del Zika, sovint no provoquen símptomes o són símptomes lleus. Des dels anys cinquanta, s'ha detectat la presència del virus dins d'un estret cinturó equatorial de l'Àfrica cap a Àsia. El 2014, el virus s'estengué a l'est a través de l'oceà Pacífic cap a la Polinèsia Francesa, després cap a l'illa de Pasqua i, el 2015, a Mèxic, Amèrica Central, el Carib i Amèrica del Sud, on el brot va assolir el caràcter de pandèmia.[4]
El virus del Zika està emparentat taxonòmicament amb els virus del dengue, la febre groga, l'encefalitis japonesa, el virus de l'encefalitis de Saint Louis i el virus del Nil occidental. Filogenèticament és molt proper al virus Spondweni, amb el qual forma un clade dintre del gènere Flavivirus.[5] Emprant serologies, no és fàcil veure les diferències entre aquests dos virus.[6]
Habitualment, la malaltia que provoca és semblant a una forma tènue de dengue,[7] si bé –en alguns casos d'infecció en dones embarassades– pot comportar lesions cerebrals fetals, sobre tot si la infecció es produeix durant el primer trimestre de gestació.[8] Així mateix, l'infecció materna implica un risc d'avortament.[9]
Alguns investigadors vinculen la infecció congènita pel ZIKV amb el desenvolupament de greus anomalies articulars (artrogriposi) en determinats nadons.[10] El ZIKV roman en el nadó infectat més de dos mesos.[11] També s'han descrit lesions oculars de diferents tipus en nens de mares infectades.[12][13] El virus és capaç d'inflamar greument la còrnia, la retina i el nervi òptic del fetus/nounat, fet que pot comportar la pèrdua de la visió, o provocar una important atròfia de la màcula.[14] En casos congènits, s'ha observat l'existència de coloboma, cataractes, glaucoma, ectòpia del cristal·lí, microftàlmia, estrabisme (convergent i divergent) i alteracions pigmentàries predominantment bilaterals.[15] Tanmateix, és una causa d'edema generalitzat (hydrops) fetal no-immune.[16] En adults, s'han identificat diversos casos d'uveïtis, tant anteriors com posteriors i de grau molt variable,[17] i també pèrdues transitòries d'audició.[18] En persones sota tractament immunosupressor el ZIKV pot ocasionar lesions corioretinals no necrotitzants.[19] La principal diferència entre les alteracions oculars de la síndrome congènita i de la infecció adquirida és la presència en aquesta d'uveïtis activa.[20]
Estudis ecocardiogràfics indiquen una prevalència alta de de defectes cardíacs en nadons afectes de la síndrome congènita per ZIKV, en especial del septe (no tots impliquen alteracions hemodinàmiques significatives).[21]
És un virus ARN monocatenari positiu, el seu diàmetre és d'uns 50 nmm, la càpsida és icosaèdrica i les seves característiques morfològiques només poden observar-se per mitjà d'un microscopi electrònic de transmissió.[22] Està format per 10,794 nucleòtids que codifiquen una poliproteïna de 3,419 aminoàcids, la qual es divideix en diferents proteïnes sota la acció de les proteases.[23] Amb crio-microscòpia electrònica d'alta resolució (9Å) s'han observat, a virus immadurs, diferències en les proteïnes i aminoàcids d'alguns components de la càpsida entre soques pre-epidèmiques i epidèmiques; que podrien modular la sensibilitat del ZIKV als anticossos i afectar el seu potencial infecciós.[24] En cultius cel·lulars humans, el virus presenta la propietat d'induir processos autofàgics que afavoreixen la seva replicació.[25] Com altres Flavivirus, el ZIKV té la característica d'infectar fàcilment determinades cèl·lules de la pell, fet que li permet disseminar-se amb rapidesa per tot l'organisme.[26] La glicoproteïna capsular E és la responsable de l'entrada del virus a les cèl·lules i es considera un objectiu de gran interès pel disseny d'anticossos terapèutics contra la infecció.[27]
La febre del Zika és una malaltia relativament nova, causada per un virus que pertany a la família Flaviviridae. El virus es va identificar per primera vegada el 1947 en els boscos de Zika, a Uganda, i sembla que fou detectar en éssers humans mitjançant estudis serològics a Nigèria (MacNamara, 1954) i a Àfrica Occidental (Bearcroft, 1956) com agent causal d'una malaltia febril suau i autolimitada.[28] Alguns especialistes opinen que, en realitat, aquestes primeres determinacions en humans corresponien al virus Spondweni i que la primera descripció de la infecció pel ZIKV amb la seva característica erupció maculopapular es degué a Simpson (1964), el qual patí la malaltia que va descriure al seu article.[29]
Fins als primers anys del segle XXI, el virus es va concentrar principalment a l'Àfrica i al sud d'Àsia. Va tenir caràcter epidèmic a l'oceà Pacífic i també es va localitzar a Malàisia i Micronèsia d'abril a juliol del 2007 (aquell any, a les illes Yap[30] dels Estats Federats de Micronèsia hi va haver un brot important amb 185 casos confirmats). L'abril del 2015, es va confirmar un brot de febre del Zika mitjançant la tècnica de RT-PCR[31] al Brasil, a la ciutat de Salvador de Bahia. Els estudis genòmics més recents indiquen que l'ancestre del ZIKV aparegué entre 1930-1945 i que la mutabilitat de les soques descendents ha anat augmentant en el decurs dels darrers anys.[32] Emprant procediments de genètica inversa un grup d'investigadors ha aconseguit reproduir soques del virus de diferents orígens temporals i geogràfics.[33] Es creu que soques primitives del ZIKV circulaven per Senegal i Costa d'Ivori abans de l'esclat de la malaltia.[34]
El primer cas conegut de febre del Zika es va documentar en un macaco rhesus (Macaca mulatta) "sentinella" (un animal en captivitat controlada i sotmès a vigilància analítica) en un arbre del bosc de Zika, Uganda, el 1947, per un equip de científics britànics dirigits pel Dr. Haddow. Es van notificar també alguns brots a l'Àfrica tropical i en algunes zones del sud-est asiàtic.[35] El primer estudi sobre embrions de pollastre infectats amb ZIKV fou publicat el 1952.[36]
L'any 1956, Boorman i Porterfield demostraren la seva transmissió per mosquits. Els moviments de tropes ocorreguts durant la IIGM (campanya de Birmània) podrien ser l'origen de l'expansió del virus de l'Àfrica a l'Àsia.[37] El 1978 es va descriure un petit brot de febre aguda a Indonèsia a causa de la infecció pel virus del Zika. Entre 1947 i 2006, varen ser identificats uns 20 casos d'infecció per ZIKV,[38] si bé les anàlisis actuals d'anticossos IgM fetes a mostres de sang antigues corresponents a malalts febrils del període 1992-2016 demostren que el ZIKV va infectar a persones de bona part d'Àfrica Occidental sense ser identificat.[39] Els especialistes creuen que aquesta virasi podria haver circulat lliurament per Àfrica molts anys, en forma de dos sub-línies genètiques diferents (Uganda i Nigèria), passant epidemiològicament desaperçebuda.[40]
El virus es va detectar principalment durant dues dècades al continent africà, tot i que també es va localitzar a Malàisia i a Micronèsia (incloent-hi les illes Yap) d'abril a juliol del 2007. El primer brot important, amb 185 casos sospitats (d'ells 49 confirmats i 59 probables), es va detectar l'any 2007 a 9 dels 10 municipis de dites illes dels Estats Federats de Micronèsia.[41] Aquesta va ser també la primera vegada que la febre del Zika es va manifestar fora de l'Àfrica i d'Àsia. Els símptomes més comuns van ser granellada, febre, artràlgies i conjuntivitis, però no es van reportar morts. Probablement, el mosquit Aedes hensilli, que era l'espècie predominant identificada a les illes Yap durant el brot, va ser el principal vector de transmissió i, tot i que es desconeix la manera com va arribar el virus a l'illa, se sospita que va introduir-s'hi a través de mosquits infectats o d'un humà portador.
El 2012 es varen identificar per primera vegada dues soques diferents del virus, la soca africana i la soca asiàtica, gràcies als treballs d'un equip d'investigadors encapçalat pel net del Dr. Haddow, descobridor del ZIKV.[42]
Entre l'octubre del 2013 i l'abril del 2014 es va produir un brot a les illes de la Polinèsia francesa. 32.000 persones (un 11.5% de la població) acudí als centres de salut amb símptomes suggestius d'infecció pel ZIKV.[43] 42 malalts desenvoluparen una síndrome de Guillain-Barré.[44] Algunes persones infectades van presentar meningoencefalitis o manifestacions autoimmunitàries (púrpura trombopènica o leucopènia). Els vectors implicats foren els mosquits Aedes aegypti i Aedes polynesiensis.[45] A principis del 2014 es produïren també casos a Nova Caledònia i a les illes Cook.[46]
El ZIKV va circular inicialment per Haití entre maig del 2014 i febrer del 2015, d'acord al estudi de les mostres preses a nens amb febre durant aquest període.[47] Les dades obtingudes entre octubre del 2015 i setembre del 2016 recullen 3,036 casos sospitosos, encara que la veritable incidència de la malaltia en el país és desconeguda fins ara.[48]
El maig del 2015, el Brasil va informar oficialment dels seus primers 16 casos de la malaltia.[49] El 27 de novembre del 2015, l'OMS va alertar de la possible relació d'aquest virus amb la microcefàlia, i va detallar que fins al 21 de novembre del 2015 s'havien detectat 739 casos de microcefàlia en 9 estats del Brasil, un d'ells mortal.[50] El 15 de desembre del mateix any, l'OMS informà de 1761 casos, 19 mortals i a 14 estats federals.[51] Segons un informe del Ministeri de Salut del Brasil, en aquest país la incidència de microcefàlia en nounats ha augmentat 20 vegades des de l'any 2010: llavors es registraven 5 casos cada 100.000 nascuts, i cinc anys més tard se'n registraven gairebé 100 de cada 100.000.
El novembre del 2015, les autoritats sanitàries brasileres van començar a sospitar que la causa d'aquesta multiplicació de casos de microcefàlia era el virus del Zika. El 17 de novembre, l'Institut Oswaldo Cruz de Rio de Janeiro va detectar el virus del Zika en dues dones embarassades de Paraíba, els fetus de les quals havien estat diagnosticats de microcefàlia. El 28 de novembre del 2015, l'Institut Evandro Chagas de malalties tropicals, a Belém, va tornar a detectar el virus del Zika en la sang d'un bebè de l'estat de Pará que tenia microcefàlia i altres anomalies, i que va morir al cap de cinc minuts de néixer. Va ser en aquesta ocasió que el Ministeri de Salut del Brasil va establir per primera vegada la relació entre el virus i la microcefàlia, i l'ens de Vigilància en Salut Pública va alertar-ne. El mateix dia, l'entitat va notificar tres defuncions associades a la infecció pel virus del Zika, que corresponien a dos adults i un nounat. Estudis recents indiquen una clara relació temporal entre l'aparició de lesions cutànies (exantema -un tipus d'erupció a la pell-) en embarassades infectades, la síndrome de Guillain-Barré, i el desenvolupament de microcefàlia fetal.[52] Aquesta relació no es produeix en infeccions similars, com la del virus del dengue.[53] A hores d'ara, la relació causal entre la infecció materna pel ZIKV i la microcefàlia es considera provada segons els criteris teratogènics de Shepard i els epidemiològics de Hill (Bradford Hill criteria).[54] Aplicar aquests darrers criteris de forma rigorosa i coherent és una de les recomanacions fetes pels experts a l'hora d'elaborar polítiques o restriccions relacionades amb el ZIKV i els seus efectes fetals.[55] A part de microcefàlia, els resultats de la imatge per ressonància magnètica en fetus i nounats infectats demostren una gran diversitat d'anomalies cerebrals,[56] objectivades als 10 dies post-infecció en models experimentals d'inoculació induïda.[57] La ressonància magnètica amb contrast gadolínic de nounats normocefàlics exposats in utero al ZIKV ha evidenciat l'existència d'engrandiments dels nervis cranials en nens de només tres dies de vida i d'infarts cerebrals isquèmics en nens de setze dies.[58]
Molts autors consideren la infecció fetal pel ZIKV com una síndrome congènita pròpia i particular amb un ampli ventall de manifestacions.[59] Dins d'aquest ventall es podrien incloure anomalies en el desenvolupament de la medul·la espinal del fetus (microcalcificacions intraespinals, distorsions estructurals i despoblació neuronal),[60] amb canvis al neuròpil i als ganglis del sistema nerviós autònom i degeneració wal·leriana.[61]
Els especialistes en radiologia consideren que les troballes de neuroimatge, sense ser patognomòniques, són altament indicatives d'aquesta síndrome congènita si concorden amb les analítiques i les dades clíniques. Encara que emfatitzen sobre la predominança de la desproporció craniofacial amb aspecte microcefàlic, les calcificacions cortico-subcorticals, la ventriculomegàlia i les anomalies del cos callós en les exploracions cerebrals, alerten sobre l'ampli espectre de subtils alteracions que la síndrome pot originar i sobre el fet que l'absència radiològica de microcefàlia no descarta en absolut una afectació del SNC fetal o postnatal pel ZIKV.[62]
El virus té la propietat de lesionar cèl·lules claus per un correcte funcionament del SNC. Per això, el conjunt de seqüeles de la infecció inclou l'epilèpsia, la pèrdua d'agudesa visual, problemes de deglució, complicacions ortopèdiques o l'augment de susceptibilitat a les infeccions respiratòries.[63]
Un grup d'investigadors ha identificat dues proteïnes (NS4A i NS4B) al ZIKV, responsables d'actuar sobre les cèl·lules mare nervioses, augmentar l'autofàgia i alterar la normal neurogènesi fetal.[64] S'ha demostrat que el ZIKV lesiona directament els orgànuls de les cèl·lules mare neurals embrionàries humanes, ocasionant anomalies en tota una xarxa de gens que regulen l'apoptosi, la diferenciació cel·lular i el desenvolupament del sistema nerviós.[65] Com altres virus neuroteratogènics, el ZIKV pot travessar la placenta, ja que té la capacitat d'infectar diferents tipus de cèl·lules placentàries[66] -com les corials- i creuar la barrera hematoencefàlica del fetus.[67] Una altra hipòtesi proposada per explicar la greu teratogènia causada pel ZIKV es fonamenta en la seva capacitat d'interferir el metabolisme dels retinoides.[68] Es creu també que durant la replicació del virus aquest indueix una resposta immunològica contra els gangliòsids del cervell, que altera la sinaptogènesi i lesiona de forma indirecta el normal creixement del sistema nerviós fetal.[69] Segons sigui la soca, el ZIKV pot presentar diferents patrons infectius de les cèl·lules neurals.[70] Experiments amb ratolins immunocompetents posen de manifest que hi ha una relació directa entre determinades malformacions (disràfia espinal, hidrocefàlia, artrogriposi) i l'exposició al virus durant la gastrulació i el període inicial d'organogènesi. També existeix una relació entre la presència de malformacions i el nombre de dies post-coitals. Les malformacions més tardanes són relacionables amb els danys a la capa laberíntica (equiparable al cori humà)[71] Cal tenir en compte que els treballs experimentals amb animals de laboratori (ratolins o primats no humans) tenen les seves limitacions, fet que comporta la necessitat de desenvolupar nous models d'estudi que reflecteixin millor els efectes del virus en funció de la influència de les variacions genètiques d'aquests hostes.[72]
In vitro s'ha demostrat que les cèl·lules estromals de l'endometri humà, en especial durant la fase de decidualització, són un blanc crucial pel ZIKV, per la via de la vasculatura uterina en el període de virèmia o per transmissió sexual i una font potencial d'expansió del virus als trofoblasts placentaris durant l'embaràs.[73]
Les autòpsies anatomopatològiques efectuades a fetus infectats confirmen l'especial neurotropisme del virus i l'absència d'alteracions citopàtiques a altres òrgans o sistemes (pulmonar, hepatobiliar, cardiovascular, genitourinari, gastrointestinal, endocrí o hematopoètic).[74] Altres sèries d'autòpsies neonatals també posen de manifest l'alt grau de neurotropisme viral, apreciant a més hipoplàsia pulmonar i canvis inflamatoris a fetge, pulmons i bufeta concordants amb infecció multiorgànica pel ZIKV.[75] Els estudis postmortem fets a macacos demostren que el ZIKV persisteix al teixit nerviós, teixit limfoide, teixit muscular i articular i teixit dels tractes reproductors masculins i femenins, entre 4-6 setmanes després de la infecció.[76]
Entre les manifestacions mucocutànies de la infecció pel ZIKV es poden destacar: erupció papular eritematosa difusa descendent, petèquies al paladar, escleròtica hiperèmica i un infiltrat linfocític perivascular a la dermis superior observat a les biòpsies de pell.[77]
El primer cas fatal va ser el d'un home adult sense cap trastorn neurològic, però diagnosticat de lupus eritematós, artritis reumatoide, alcoholisme i que havia fet un ús crònic de corticoides. Va ingressar amb sospita de dengue, però el diagnòstic final va ser infecció pel virus del Zika mitjançant la tècnica RT-PCR. Es va detectar el genoma del virus del Zika en mostra de sang, cervell, fetge, melsa i en una mescla de vísceres (ronyons, pulmons i cor). Addicionalment es va dur a terme una seqüenciació parcial del virus i es va identificar el Zika. El segon cas fatal va ser el d'una noia de 16 anys del municipi de Benevides, en l'estat de Pará. Tampoc no va presentar cap trastorn neurològic, i va ingressar al servei hospitalari amb sospita de dengue. Els símptomes (cefalea, nàusees i petèquies) van començar el 29 de setembre del 2015 i va morir a final del mes d'octubre. Es va confirmar infecció pel virus del Zika a través de la tècnica RT-PCR. Els següents casos fatals foren cinc nounats. Es sospita que, en adults no immunodeprimits, infeccions prèvies per altres Flavivirus poden condicionar un pitjor pronòstic en la malaltia.[78] L'extrapolació dels experiments fets en animals es motiu de controvèrsia, però es creu que la infecció pel ZIKV té pitjors efectes en casos d'infecció prèvia pels virus del dengue o del Nil Occidental.[79] En realitat, fins ara no existeixen estudis clínics fefaents que demostrin un fenomen de potenciació depenent d'anticossos en aquesta virasi.[80] S'ha publicat algun quadre de mielitis aguda derivada d'una infecció per ZIKV.[81] En la RM espinal, s'observa sovint que la mielitis afecta tres o més segments de la medul·la, la qual presenta signes edematosos.[82] A Nova Caledònia s'han descrit un parell de casos de miastènia gravis subseqüents a infecció per ZIKV.[83] Al Brasil s'han publicat diversos casos de polineuritis aguda transitòria en adults, associats a la infecció pel virus.[84] A mesura que es coneix millor el risc que comporta la infecció en adults i adolescents i les proves per detectar el virus es fan més habituals, augmenta la casuística de les lesions nervioses relacionades amb el ZIKV. S'ha descrit l'aparició d'una encefalomielopatia sis setmanes després de l'inici del quadre viral agut.[85] En aquesta línia, almenys en adolescents amb un substrat psicològic determinat, sembla que la infecció pel ZIKV podria desencadenar o ajudar a desencadenar canvis neuropsiquiàtrics i cognitius.[86]
Entre finals de 2015 i principis de 2016, la soca asiàtica del ZIKV causant de la pandèmia americana es va estendre per les illes de Cap Verd, registrant-se tres casos de microcefàlia i unes 7.500 persones infectades.[87]
A Europa, el primer cas d'un nadó afecte de microcefàlia, relacionat amb infecció materna per ZIKV, va ser identificat a Barcelona, a l'Hospital Universitari Vall d'Hebron.[88] Investigadors d'aquest hospital confirmaren que la presència prolongada d'ARN del ZIKV al sèrum de la mare pot ser un indicador d’infecció fetal i que -al mateix temps- dita presència seria atribuïble a la seva replicació al fetus o a la placenta, a causa d'un efecte de retroalimentació entre la placenta i la mare.[89] A hores d'ara, no s'ha determinat clarament si la presència d'immunitat i/o seropositivitat a altres virus en la mare és un factor que condiciona el desenvolupament de microcefàlia fetal.[90]
A Itàlia, ja al maig de 2015 es va detectar un cas d'infecció simptomàtica per ZIKV en una persona persona vinguda del Brasil dos dies abans.[91] Investigadors francesos varen publicar al desembre de 2016 el primer cas de miocarditis en un adult derivada d'una infecció aguda importada per ZIKV.[92] El nombre d'articles publicats sobre els efectes del virus sobre el miocardi és -per ara- molt reduït. Alguns especialistes posen l'accent sobre el desconeixement de les possibles complicacions cardíaques a llarg termini derivades de la infecció.[93]
L'agost de 2016, els casos a l'Estat Espanyol eren 247.[94] El mateix mes es va detectar l'expansió autòctona del virus a Singapur.[95] A principis de juny de 2017, els casos confirmats pel Ministeri de Sanitat, Serveis Socials i Igualtat segons les dades de la Red Nacional de Vigilancia Epidemiológica eren 325, 120 a Catalunya, 81 a Madrid, 20 a l'Aragó, 15 a Andalusia, 14 a Castella i Lleó, 13 a València, 13 a Galícia, 8 a La Rioja, 9 al País Basc, 7 a les Illes Balears, 6 a Navarra, 6 a Astúries i la resta molt repartida per tot l'Estat; 46 d'ells dones embarassades i 4 nadons indicant infecció congènita per ZIKV, tots fills de mares infectades a zones de risc. Dels 325 casos, dos eren autòctons i deguts a transmissió sexual i dotze han estat diagnosticats l'any 2017.[96] Des de la setmana 44 de control, el nombre de casos detectats va minvar molt. Entre 2016 i 2017 es notificaren un total de 512 casos (344 confirmats i 158 probables). El març de 2017 va ser publicada pel MSSSI la darrera avaluació (8a) del risc de transmissió del virus a l'Estat[97] i el gener de 2018 fou emés un informe final sobre l'epidèmia, que comunica la fi del seguiment mensual de la malaltia.[98]
Al Japó es van detectar els primers casos importats per viatgers provinents de la Polinèsia francesa entre el període desembre 2013-gener 2014.[99] Posteriorment, s'han registrat més casos d'infecció importats des de Brasil (febrer de 2016), Fiji,[100] Tailàndia i Vietnam.[101]
El 2 de desembre de 2016, segons la Divisió de malalties transmeses per vectors dels CDC, els països i territoris a Amèrica, Asia, Oceania i Àfrica amb transmissió activa del ZIKV eren 61.[102] A 75 països han estat identificades infeccions –de transmissió activa o passiva– pel ZIKV, 58 d'ells amb brots importants (novembre 2016). A tot el món, les darreres projeccions (febrer del 2017) consideren que uns 2.261 milions de persones tenen un alt risc d'exposició al ZIKV; en especial a les zones costaneres atlàntiques i pacífiques de l'Àfrica central i sud, les atlàntiques de Sud-amèrica i les properes al mar Carib d'Amèrica del Nord i Central.[103] Fins al primer trimestre de 2017, a 29 països s'han detectat casos de malformacions neurològiques en fetus o nadons relacionades amb infecció congènita causada pel virus del Zika.[104]
El butlletí d'abril del 2017 de la publicació informativa epidemiològica de l'OMS eleva a 70 els països amb brots de certa importància i destaca la manca d'informació veraç sobre el nombre total de casos, ja que molts dels infectats no cerquen ajut sanitari.[105]
Els motius de la forta emergència del ZIKV no es coneixen del tot. Tanmateix, els científics han observat una circumstància global: la transmissió infecciosa del dengue o del virus chikungunya precedeix a les infeccions pel ZIKV. Els brots simultanis de dengue o d'altres Flavivirus semblen alterar les característiques del virus, comporten errors de diagnòstic i dificulten el desenvolupament d'un test molecular identificatiu estàndard.[106] Alguns investigadors posen l'accent en el paper del fenomen de 'El Niño' en la ràpida propagació de la infecció el 2015.[107]
La primera constatació de la presència del virus del Zika a Amèrica va ser confirmada el febrer del 2014 a l'illa de Pasqua, a Xile. La soca viral identificada a aquesta illa era similar a la causant del brot de la Polinèsia francesa.[108] La presència del virus es va detectar fins al juny del mateix any en aquesta àrea. Fins a l'1 de desembre del 2015, eren 9 els estats membres de l'Organització Panamericana de la Salut que havien confirmat la presència local del virus del Zika: el Brasil, Xile (a l'illa de Pasqua), Colòmbia, El Salvador, Guatemala, Mèxic, Paraguai, Surinam i Veneçuela.[109]
El maig del 2015, es van confirmar els primers casos de transmissió al Brasil. Fins a l'1 de desembre del 2015, un total de 18 estats van confirmar la circulació autòctona del virus: regió nord (Amazones, Pará, Rondônia, Roraima i Tocantins), regió nord-est (Alagoas, Bahia, Ceará, Maranhão, Paraíba, Pernambuco, Piauí i Rio Grande do Norte), regió sud-est (Espírito Santo, Rio de Janeiro i São Paulo), centre-oest (Mato Grosso) i regió sud (Paranà).[110] El Ministeri de Salut del Brasil estima que durant els nou primers mesos de l'any 2016 es donaren 200,465 casos d'infecció per ZIKV; d'aquests, 109,596 van ser confirmats emprant criteris clínics o epidemiològics per carència de tests de laboratori específics pel diagnòstic acurat de l'existència del virus.[111] Estudis més recents recullen 1,673,272 casos registrats durant el període 2015-2016. D'ells, 41,473 (un 2,5%) foren infeccions en dones embarassades i es confirmaren 1,950 casos de microcefàlia relacionada amb la infecció en aquest grup.[112] El virus es va estendre per tot el país en uns 5–6 mesos, des de la costa nord-est a la costa sud-est i la frontera occidental, amb una velocitat mitjana de 42 km/dia.[113] Brasil ha estat el país del món amb el major nombre de casos d'infecció per aquest patogen i on s'ha observat l'existència de més nens amb malformacions cerebrals relacionades amb el ZIKV. Un estudi sobre la qualitat diagnòstica dels laboratoris brasilers encarregats de la detecció molecular del virus, realitzat l'any 2017 per un equip internacional d'experts, ha posat de manifest que dos terços de dits centres tenia una limitada especificitat/sensibilitat diagnòstica; amb una moderada, però preocupant, quantitat de falsos-positius i falsos-negatius en els resultats.[114]
L'octubre del 2015 les autoritats de salut de Colòmbia notificaren la detecció del primer cas autòcton d'infecció per virus del Zika al departament de Bolívar. Aquest mes es va registrar el primer cas a Surinam causat per la mateixa soca responsable del brot 2013-2014 a la Polinèsia francesa, segons els estudis genòmics fets a l'Institut Pasteur de la Guyana.[115] Fins a desembre del 2015, 26 de les 36 entitats territorials americanes van confirmar la circulació autòctona del virus. Colòmbia liderava la llista d'infectats amb 578 diagnòstics confirmats de 3.170 casos informats. La regió del nord de Santander presentà la quantitat més gran d'infectats, amb 350 casos. L'anàlisi epidemiològic temporo-espacial a posteriori del brot a Colòmbia indicà 107.870 casos registrats en 1.122 municipis del país, quasi 20.000 d'ells en gestants.[116] Fou al novembre del 2015 quan El Salvador, Guatemala, Mèxic, Paraguai i Veneçuela van confirmar casos de transmissió autòctona.[109] El primer cas notificat a l'OMS per Bolívia va ser el gener de 2016.[117] Perú registrà la primera infecció a l'abril del mateix any.[118]
Als EUA, els primers casos de transmissió local del ZIKV foren detectats pel Florida Department of Health al juliol de 2016,[119] aconsellant els CDC que les dones embarassades no vagin a determinats llocs del Comtat de Miami-Dade.[120] A finals d'agost, un cas d'infecció pel ZIKV va ser detectat a Pinellas, molts kilòmetres al nord de la ciutat de Miami.[121] Les inundacions ocorregudes durant dit mes a Louisiana i al juny a Texas podrien afavorir el creixement dels mosquits vectors i, per tant, la possible extensió de la malaltia per tots els estats del Golf de Mèxic nord-americà.[122] Emperò, aquest fet no ha estat provat de forma científica. La primera mort relacionada amb el ZIKV d'un nen a Texas va ser informada a l'agost de 2016.[123] Segons els CDC, el primer cas d'infecció per transmissió local en aquest Estat va ser detectat al novembre de 2016.[124] Un altre cas va ser confirmat al desembre a la zona de Brownsville.[125] Valorant la presència del mosquit Aedes aegypti i els indicadors de potencial transmissió del virus per via sexual, 507 comtats dels estats del sud dels EUA -des del litoral atlàntic a Califòrnia- presenten un risc alt de patir infeccions pel ZIKV, especialment a Mississipí.[126] De les 1.297 dones embarassades amb criteris d'infecció per ZIKV controlades pel U.S. Zika Pregnancy Registry (USZPR) durant l'any 2016, un 5% amb possible infecció, un 10% amb infecció confirmada i un 15% amb infecció confirmada al primer trimestre de gestació tingueren nens (o fetus en cas de gestacions no viables) amb defectes.[127] Una qüestió per aclarir és si la infecció fou un factor causal determinant en els casos d'avortament compilats en dit Registre, o si aquests es degueren a circumstàncies concorrents.[128] Segons els CDC, un estudi fet als territoris no incorporats (Gener 2016-Abril 2017) indica que en un 8% dels casos de dones amb infecció confirmada durant el primer trimestre de gestació, en un 5% durant el segon i en un 4% durant el tercer, es van detectar anomalies del fetus/nadó.[129] La preocupació pels efectes de l'expansió del virus i les seves conseqüències és important al país. Un exemple d'això és la transmissió formalitzada de missatges informatius sobre la malaltia per les diferents organitzacions comunals i religioses de la nació.[130] Durant el decurs de l'any 2016, als EUA (50 estats i Districte de Columbia) es va registrar un total de 5.168 casos d'infecció no congènita pel ZIKV. Un 95% d'ells foren diagnosticats en viatgers retornats de zones afectades per la virasi, un 4% en persones infectades localment a través de mosquits i un 1% en persones infectades per altres vies (sexual, accident de laboratori o persona-persona sense mecanisme de transmissió definit).[131] Durant el 2017 es diagnosticaren 1.088 casos d'infecció simptomàtica, no congènita: 433 als estats i 655 als territoris, incloent els casos confirmats i probables segons els criteris del Council of State and Territorial Epidemiologists.[132]
Un estudi realitzat als territoris francesos americans en una cohort de dones embarassades amb infecció pel ZIKV simptomàtica confirmada per PCR, mostrà que el risc general de presentació d'anomalies fetals neurològiques i oculars o de microcefàlia és d'un 7%, una dada bastant similar a la obtinguda pel USZPR controlant indistintament infeccions simptomàtiques o asimptomàtiques. Els casos de microcefàlia greu es limitaren a infeccions maternes ocorregudes durant el primer o segon trimestre de gestació. El percentatge de defectes neonatals relacionats amb el virus, distribuït per trimestres, fou d'un 12,7 (primer trimestre), 3,6% (segon trimestre) i 5,3% (tercer trimestre). L'estudi va detectar la presència de microcefàlies lleus proporcionades i desproporcionades en infeccions esdevingudes a tots els trimestres (considerant proporcionades les microcefàlies observades en nounats petits segons l'edat gestacional[133] i desproporcionades les de nens amb un pes normal en relació a dita edat). L'evidència de microcefàlies proporcionades suggereix que, en alguns casos, el ZIKV pot alterar el creixement fetal sense concurrència de lesions destructives cerebrals específiques o amb ella.[134]
Com efecte no desitjat de les fumigacions preventives contra els mosquits vectors amb insecticides organofosforats neurotòxics (Naled), a les zones tractades amb el producte varen morir millions d'abelles.[135] El Departament de Treball dels EUA va publicar, com mesura preventiva, un document amb normes i recomanacions dirigit als treballadors exposats als mosquits.[136] La FDA va aprovar, com mesura de biocontrol, l'alliberament de mosquits genèticament modificats a Key West,[137] malgrat el rebuig majoritàri dels habitants de l'illa.[138] Aquesta tècnica, que va ser emprada mesos abans a Piracicaba, comporta que les larves d'Aedes aegypti no arribin a la maduresa.[139] Per controlar les larves del mosquit també s'han utilitzat fumigacions amb el bacteri Bacillus thuringiensis serotip israelensis (Bti), un microorganisme firmicut present al sòl que forma espores tòxiques que ataquen molt selectivament aquesta espècie de culícids i no afecten a altres insectes que no són objecte de control.[140]
La celebració dels Jocs Olímpics d'estiu de 2016 va generar una forta polèmica científica sobre la possibilitat d'un augment de la seva expansió incontrolada, els possibles riscos a assumir i les mesures de control recomanables.[141][142][143] Malgrat algunes previsions, no es va detectar cap cas d'infecció per ZIKV entre els atletes o els visitants.[144]
Sent una malaltia infecciosa fortament emergent i en procés de ràpida extensió geogràfica, es considera una amenaça per a la salut mundial.[145] La OMS la va declarar "emergència de salut pública d'importància internacional" al febrer de 2016.[146] Nou mesos després, al novembre de 2016 el portaveu de la OMS va declarar que, segons els criteris de dita organització, el Zika ja no es considerava "emergència global"; si bé especificant que ha de ser vist com un greu problema a llarg termini.[147] Els CDC varen publicar a finals de 2016 un estudi molt detallat, fent un repàs als principals esdeveniments de l'any relatius al tema i anticipant les prioritats del treball sobre el ZIKV a les Amèriques.[148] L'OPS va presentar al maig del mateix any un recull d'instruccions i recomanacions per prevenir, diagnosticar, notificar i controlar les infeccions pel ZIKV en les gestants.[149] Dita organització lliurà, uns mesos abans, un algoritme de detecció basat en les xarxes de vigilància del dengue ja existents (22 laboratoris nacionals de referència).[150]
Segons les dades de l'OPS recollides fins a mitjans del mes de desembre de 2016, 48 països i territoris americans han registrat casos d'infecció pel ZIKV.[151] El document d'actualització redactat per aquest organisme amb data 25 de maig de 2017 no informa de casos autòctons nous per transmissió vectorial a més llocs d'Amèrica. Cinc països han identificat la transmissió del virus per via sexual. El nombre acumulat de casos de síndrome congènita associada a la infecció és de 3.231.[152]
Alguns investigadors plantejen factors ambientals, com la contaminació, a l'hora de valorar les possibles concauses de la teratogènia del ZIKV.[153] Científics brasilers, recopilant les dades obtingudes des de l'esclat de la malaltia al seu país indiquen que podrien existir casos sense diagnosticar, malgrat les normes de l'OPS.[154]
L'adaptabilitat vectorial del virus a diverses espècies de mosquits i la concurrència d'activitats humanes modernes expliquen la rapidesa de la seva expansió.[155] La soca viral causant de les infeccions a les Amèriques és d'origen asiàtic i s'ha dividit en petits subtipus locals. De fet, la dinàmica evolutiva del virus al continent americà és molt notable i s'ha posat de manifest la co-circulació de diferents línies genètiques del ZIKV a diversos països d'aquesta zona geogràfica.[156]
Quasi dos anys després de l'inici de la pandèmia a les Amèriques, els experts alerten sobre les causes del seu esclat: deforestació, desastres naturals, augment de la temperatura mitjana, pobresa, manca de control dels vectors, recessió, accés limitat als serveis de sanitat, corrupció política i generalització dels viatges. Aquest conjunt de factors dibuixa un panorama molt procliu al ressorgiment i l'emergència de les malalties vectorials per arbovirus.[157] Projeccions estadístiques basades en l'anàlisi espacial d'alta resolució de les dades obtingudes en Sud-amèrica i el Carib presenten resultats teòrics preocupants pel futur de la sanitat a dites regions: uns ∼12,3 milions/any nous casos d'infecció pel ZIKV, unes ∼64.400/any noves síndromes de Guillain-Barré i unes ∼4.700/any noves microcefàlies. Potencialment, el cost econòmic anyal només de les seqüeles neurològiques seria altíssim.[158]
Els resultats dels estudis genòmics realitzats per diferents grups d'investigadors indiquen que el ZIKV estava present al continent americà molts mesos abans de ser detectat epidemiològicament el 2015.[159][160][161] Segons una recensió d'aquests estudis, la seqüència de transmissió del ZIKV (amb unes "finestres" temporals aproximades) a les Amèriques hauria sigut: des de les illes del Pacífic - a Brasil (finals 2013); des de Brasil - a Honduras/Colòmbia/Puerto Rico/Carib (entre finals del 2014-inicis del 2015); i des de diferents punt del Carib - a Florida (inicis del 2016).[162]
Una investigació desenvolupada a 16 països americans posa de manifest que l'alçada sobre el nivell del mar (considerada una variable proxy), és una eina per predir l'expansió del ZIKV a determinades zones del continent. Per sobre dels 1.900 m, menys d'un 1% de la població d'aquests països viu en llocs on és previsible la presència del vector Ae. aegypti. Als EUA (estats i territoris), no s'ha detectat cap infecció pel ZIKV relacionada amb mosquits per sobre dels 2.000 m.[163]
Es transmet amb la picada d'un mosquit del gènere Aedes, com l'Aedes aegypti, que causa el dengue. Aedes albopictus és considerat també un vector important.[164] Aedes africanus i diferents espècies de Haemagogus (un mosquit arborícola de les selves d'Amèrica) es consideren potencials vectors.
Investigadors xinesos de l'Institut de Zoologia de Kunming han descobert que una proteïna de les glàndules salivals del Aedes aegypti, anomenada LTRIN, facilita la transmissió del ZIKV. LTRIN té la capacitat de modular la resposta immune de l'hoste contra la picada del mosquit, afavorint així l'entrada del virus. Un anticòs dirigit contra dita proteïna podria utilitzar-se en poblacions de risc per disminuir les possibilitats d'infecció.[165]
Com moltes virasis, pot transmitir-se per transfusions amb sang infectada.[166] Això obliga a establir noves tipologies analítiques per utilitzar amb seguretat aquesta sang o els seus derivats,[167] com les plaquetes,[168] ja que alguns donants poden estar infectats i no haver manifestat cap símptoma. Els mètodes per aconseguir una donació de sang amb garanties sanitàries depenen de molts factors, especialment dels criteris geogràfics.[169] En aquesta línia, s'ha comprovat que els mètodes d'inactivació vírica utilitzats en la preparació de derivats de plasma, són eficaços en el cas de presència de ZIKV.[170] En mostres de sang total, el virus segueix actiu més de dos mesos després de l'extracció.[171] Proves fetes amb macacos també indiquen una major persistència de l'ARN viral a la sang total i el teixit hemolimfàtic que al plasma.[172] Als EUA continentals van detectar els primers casos de donants de sang infectats emprant una combinació de analítiques serològiques i tests d'àcid nucleic d'alta especificitat (cobas® Zika Test).[173] Al juny de 2016 la Creu Roja dels EUA adoptà el mètode Procleix® Zika Virus Assay[174] per identificar l'ARN del ZIKV en les donacions. Un estudi de 2018, basat en 4.325.889 donacions efectuades entre juny de 2016 i setembre de 2017, posa de manifest que 160 mostres es consideraren inicialment positives i només 9 d'elles van ser confirmades després; una ràtio de 1/480.654 casos positius.[175]
La presència d'ARN del virus al vitri d'un donant de còrnia asimptomàtic reforça la necessitat d'aconseguir un mètode segur i regulat per l'anàlisi d'aquest tipus especial de teixits.[176] En el cas dels trasplantaments d'òrgans sòlids i donant viu, s'ha de valorar l'antecedent d'estància prèvia d'aquest a llocs amb ZIKV i posposar el procediment el temps necessari, segons els protocols de l'Organització Nacional de Trasplantaments. Si l'òrgan a trasplantar pertany a una persona difunta cal fer les analítiques pertinents de forma rigorosa i ràpida.[177]
Entre humans, la transmissió és vertical (placentària de mare a fetus i per la llet materna) i horitzontal (transfusions i contacte sexual -veure Prevenció-).[178] Al igual que altres malalties transmeses per mosquits (com la febre groga), un mosquit vector pot picar a una persona infectada -si el virus roman present a la sang perifèrica- i infectar a un altre individu no infectat amb una nova picada.[179] La transmissió per la llet materna sembla no ser una constant, o -almenys- la presència de partícules víriques en ella no implica necessàriament una transmissió perinatal eficaç del ZIKV.[180] S'ha demostrat la presència del virus al calostre (244 × 10⁴ còpies/mL) i la llet d'una dona infectada a les 36 setmanes de gestació i l'absència de particles virals a placenta, líquid amniòtic, sang de cordó i orina del nadó (nascut a les 38 setmanes sense anomalies). Es detectà el virus a la llet 9 dies després del part (216,000 copies/mL), amb capacitat infecciosa segons els cultius realitzats, fet que va desaconsellar la lactància.[181] Alguns investigadors pensen que dita aparent inconstància en aquesta forma de transmissió materna podria ser deguda a la variabilitat del temps d'incubació del virus, fet que fa difícil distingir-la d'altres vies de transmissió perinatal.[182] Segons un recull de casos estudiats a Florida acuradament, el període d'incubació oscil·la entre dos i tretze dies i tots els malalts presentaven erupció cutània en el moment de ser visitats per primera vegada, la majoria d'ells en la segona setmana de la infecció.[183]
A hores d'ara, malgrat els avenços en el coneixement de la patofisiologia de la infecció, molts mecanismes implicats en la transmissió vertical del ZIKV resten per descobrir. Com s'ha vist en altres tipus de trastorns congènits de causa viral, en cas d'embaràs gemel·lar dizigòtic és possible que el ZIKV provoqui importants malformacions en un dels fetus i que l'altre es desenvolupi normalment.[184] En ratolins immunocompetents, s'ha comprovat que l'exposició materna al virus ocasiona greus alteracions placentàries i que els nivells d'ARN del ZIKV en la placenta o els teixits embrionaris no són predictius dels canvis patològics desenvolupats en els embrions. Dites alteracions inclouen una considerable hiperplàsia dels trofoblasts, necrosi de la zona d'unió de la placa coriònica i la placa decidual i pèrdua de vasos. Dins del context d'una infecció murina controlada, aquestes troballes suggereixen que la patologia placentària podria ser el principal factor causant de malformacions i no la infecció viral directa de l'embrió o del fetus.[185] Experimentalment i també en rates, un antipalúdic que inhibeix l'autofàgia, la hidroxicloroquina (fàrmac aprovat per ser administrat a dones embarassades), atenua els efectes de la infecció placentària i fetal pel ZIKV.[186] Alguns especialistes dels EUA afirmen que la cloroquina, combinada amb sofosbuvir, podria ser emprada eficaçment en la profilaxi i tractament de les infeccions per aquest virus.[187]
Els darrers estudis epidemiològics i d'entomologia mèdica indiquen que primats no humans poder ser hostes del virus i que aquest és endèmic a alguns països d'Àfrica i Asia. Aquest fet fa que es consideri possible la transmissió zoonòtica directa per la mossegada de dits animals. Tan sols hi ha constància d'un cas d'infecció en un viatger mossegat per un macaco a Bali.[188] En una sèrie d'exemplars de dues espècies de primats de 4 països africans s'ha trobat una seropositivitat al ZIKV del 16%, aproximadament, en alguna de les poblacions estudiades.[189] Probablement, fins ara, moltes infeccions per ZIKV es confonien amb virasis semblants.[190] A banda dels primats, encara no es coneix amb certesa el paper d'altres animals salvatges o domèstics en la transmissió indirecta del virus, en especial en zones periurbanes.[191]
Fins ara no s'ha demostrat la transmissió del virus a través de la saliva,[192] si bé no es pot descartar en el cas de persones amb lesions a la mucosa oral i/o malaltia periodontal.[193] El ZIKV es pot mantenir un mes en les llàgrimes i el líquid conjuntival dels individus infectats.[194]
Actualment, només hi ha descrit un cas d'infecció per ZIKV en un treballador de laboratori, a causa d'una punció d'agulla.[195] Cal tenir en compte que el virus pot sobreviure en superfícies dures i no desinfectades algunes hores, segons les condicions ambientals. La major part de substàncies sanitàries desinfectants d'ús comú aplicades sobre aquests tipus de materials inactiva el virus.[196] A banda de la via sexual (veure Prevenció), encara es desconeixen molts aspectes de la transmissió del ZIKV persona-persona. Un estudi sobre el contagi d'un familiar -sense cap altre tipus d'exposició- que va cuidar un malalt mort per la malaltia a Utah (2016, juny) i que tenia una càrrega viral molt alta, posa de manifest la necessitat d'investigar el risc infecciós que representen alguns fluids corporals i els factors individuals que poden augmentar la susceptibilitat davant el virus.[197]
Es creu que casos asimptomàtics, amb una baixa virèmia, poden tenir un paper significatiu en la transmissió del virus, fet a tenir en consideració quan es realitzen models epidemiològics.[198]
El virus del Zika pot ser identificat mitjançant una prova de RT-PCR (en anglés: Real Time-Polymerase Chain Reaction, una de les tècniques de la PCR) a sang, saliva, orina i semen,[199][200] en pacients greument malalts, o fins i tot asimptomàtics,[201] i per serologia mitjançant la detecció d'anticossos IgM específics a partir del cinquè dia posterior a l'aparició de la febre (tècnica ELISA).[202] És possible que es manifestin reaccions serològiques creuades amb altres flavivirus estretament relacionats, com el dengue[203] o el virus de l'encefalitis japonesa.[204][205] Equips de recerca europeus treballen en una nova prova ELISA modificada amb proteïnes ZIKV recombinades, per reduir el nombre de dites reaccions creuades i millorar la capacitat diagnòstica precoç.[206] La baixa especificitat d'alguns immunoassajos es pot millorar repetint la prova en una nova mostra recollida un temps després de la primera, procediment no sempre fàcil de realitzar. L'ús combinat dels Euroimmun Zika Virus IgM i IgG ELISAs tests proporciona una bona especificitat (82%).[207] Un grup multinacional d'investigadors ha desenvolupat un test serològic (NS1-BOB) capaç d'evitar les reaccions creuades, però encara pendent d'alguna millora en relació al DENV tipus 4.[208] Un nou test que millora els resultats dels anteriors, anomenat ZIKV-NS2B-concat ELISA, amplia la finestra de detecció del virus amb una sensibilitat i especificitat molt altes (96.0% i 95.9%, respectivament).[209]
Un nou mètode colorimètric de tipus MTT i d'alt rendiment, per detectar el virus en cèl·lules vives o quantificar la seva infectivitat (grau de poder infectiu d'un agent patògen) després de diferents tractaments, ha estat descrit recentment (febrer 2017). Aquest test pot ser valorat amb rapidesa a ull nu o de forma automatitzada i el seu cost és molt baix.[210]
L'ARN del ZIKV de les mostres d'orina es degrada amb facilitat, inclús conservada a baixes temperatures. Per aconseguir una correcta detecció del ZIKV en aquestes mostres, és convenient afegir un estabilitzador nucleic durant el procés d'anàlisi.[211]
Existeixen ja aparells poc costosos per identificar la presència del ZIKV en la saliva humana fora d'un laboratori.[212] Es treballa per perfeccionar un innovador mètode diagnòstic del virus, ideat pel seu ús en punts d'atenció primària, que utilitza les capacitats tecnològiques dels telèfons intel·ligents i que també pot detectar altres Flavivirus.[213][214] Investigadors de la Universitat de Nova York i de l'empresa Rheonix desenvolupen, a partir d'un model ja existent emprat per la detecció ràpida del VIH en saliva, un test que reconeix marcadors diagnòstics del ZIKV en una fracció del temps requerit pels mètodes comercialitzats fins ara. El test combina una variant de la PCR, l'amplificació isotèrmica, per identificar els àcids nucleics del virus en 20 minuts; i antígens ZIKV-específics millorats que aconsegueixen un immunoassaig fiable, basat en un microarray peptídic d'alta densitat, en menys d'una hora.[215]
Emprant la RT-PCR en temps real, el virus pot ser detectat a mostres de moltes espècies de mosquits vectors en tres hores.[216] Els CDC han desenvolupat un test de laboratori que detecta conjuntament el RNA del ZIKV, del virus del dengue i del virus chikungunya (Trioplex rRT-PCR), per emprar en cas d'emergència.[217] Als EUA, s'han comercialitzat tests automàtics d'amplificació isotèrmica de l'àcid nucleic per detectar qualitativament l'ARN del ZIKV en sèrum i orina (com el sistema Aptima®), una alternativa a la PCR que no necessita de dispositiu termociclador i utilitza un software específic.[218] Les primeres avaluacions d'aquest test indiquen que té major especificitat i una sensibilitat més alta que els procediments clàssics de RT-PCR.[219] Basat també en la tècnica d'amplificació isotèrmica de l'àcid nucleic, s'ha desenvolupat un nou test capaç de detectar i diferenciar la soca asiàtica i la soca africana del ZIKV.[220]
Altres investigadors han presentat un mètode perfeccionat de RT-PCR per identificar molt ràpidament el ZIKV en mostres d'orina a zones sense equipaments analítics.[221] Un mètode de detecció millorada ha estat dissenyat per laboratoris europeus utilitzant la RT-PCR (RealStar® Zika Virus RT-PCR Kit), pendent de validació a Amèrica.[222] S'han fet assajos en humans i animals d'una nova tècnica de RT-PCR dirigida a detectar la regió 5'-UTR (de l'anglès untranslated region), que no presenta in vivo o in vitro reaccions creuades amb altres virus.[223] Ha estat dissenyada una plataforma diagnòstica de gran especificitat basada en la nanotecnologia plasmònica, que permet diferenciar la infecció per ZIKV de la causada per altres flavivirus.[224]
Un nou enfocament dins del camp de la diagnosi precoç d'aquesta virasi és el desenvolupament de biosensors basats en xips de grafè, els quals tenen una gran portabilitat i poden detectar quantitativament i en temps real l'antigen ZIKV-NS1 de forma molt específica.[225]
A Catalunya, els organismes de vigilància epidemiològica tenen establerts protocols davant els possibles casos d'infecció per ZIKV.[226]
A l'Estat, la vigilància d'aquest tipus de virasis s'emmarca dins del Plan Nacional de Preparación y Respuesta frente a Enfermedades Transmitidas por Vectores.[227]
El virus del Zika és un flavivirus transmès principalment per mosquits relacionats amb la transmissió del virus del dengue. S'ha identificat -poques vegades fins ara- també en mosquits dels gèneres Culex (Culex perfuscus), Anopheles (Anopheles coustani) i Mansonia (Mansonia uniformis).[228] El virus va ser aïllat per primera vegada l'any 1947 a la sang d'un macaco rhesus infectat del Yellow Fever Research Laboratory britànic, ubicat al bosc de Zika, a Uganda.[229] Es creu que l'espècie Aedes henselli fou el principal vector del brot de ZIKV a Yap i que Aedes furcifer i Aedes africanus (una espècie amb gran afinitat pels primats arborícoles) són els mosquits de major prevalença al continent africà.[230] Es considera que el mosquit Culex quinquefasciatus –almenys en determinats llocs i ambients– és un més que possible vector.[231] Estudis experimentals fets per grups d'investigadors europeus indiquen que els tipus de Culex habituals a Europa Central no són vectors competents de transmissió del ZIKV. El mosquit Aedes albopictus -a 27°C- mostra una capacitat de transmissió similar a la de l'espècie Aedes aegypti, fet no observat a temperatures més baixes.[232] De moment no hi ha cap estudi que demostri que l'Aedes japonicus japonicus (una espècie invasora de culícids, considerada un vector del dengue i de la chikungunya i recentment identificada a Alemanya, França, Bèlgica, Suïssa, Itàlia i Àustria) sigui capaç de transmetre el ZIKV.[233] L'aparició de mecanismes de resistència a la piretrina a soques de l'Aedes aegypti replanteja l'eficàcia d'aquests tipus d'insecticides per controlar el mosquit.[234]
S'ha demostrat la competència vectorial de l'Aedes aegypti per transmetre simultàniament el ZIKV i el virus chikungunya amb una única picada.[235]
Els Culex quinquefasciatus i els Culex pipiens pipiens d'Amèrica del Nord no són vectors competents del virus.[236] Per contra, l'abundància i el comportament agressiu de l'espècie Aedes vexans fan que sigui considerada un probable vector del ZIKV en aquesta zona geogràfica.[237] Al Brasil, s'ha comprovat la presència a la saliva i tracte digestiu de C. quinquefasciatus alimentats artificialment amb sang infectada pel ZIKV i aïllat genoma del virus a mosquits lliures de la mateixa espècie.[238] A China, els epidemiòlegs creuen que l'Aedes albopictus -espècie que predomina en el país- és potencialment el principal vector autòcton del virus.[239]
Un informe de la United States Government Accountability Office de maig del 2017, destaca que als EUA existeixen uns 900 centres i organismes dedicats al control de mosquits que no arriben a cobrir totes les zones del país. Ja que el cicle dels vectors és estacional, l'informe posa l'accent en la necessitat d'establir estratègies múltiples de vigilància i control fonamentades en el coneixement de la biologia i distribució dels mosquits. També recomana programar la disponibilitat de recursos en conjunt, mantenir actualitzada la informació sobre la distribució dels vectors, lligar els efectes de les activitats de control amb els brots d'infecció pel ZIKV i compartir les dades obtingudes entre les diferents entitats responsables de les campanyes de control.[240]
Models predictius indiquen que 35 espècies de mosquits poden ser potencials vectors del virus.[241] A hores d'ara, una anàlisi dels estudis realitzats a 10 laboratoris de 15 països sobre 18 poblacions diferents de mosquits del gènere Culex posa de manifest que les seves espècies no són vectors efectius del ZIKV.[242] Els especialistes alerten, però, sobre el perill de considerar l'Aedes aegypti com el principal vector estable del ZIKV, ja que la història evolutiva dels Flaviviridae, segons múltiples estudis filogenètics, demostra una gran capacitat per diversificar la seva transmissió vectorial mitjançant moltes espècies de culícids.[243]
Inclús durant els moments més àlgids dels brots d'aquesta infecció, el nivell de detecció del ZIKV en el conjunt de les mostres recollides de mosquits vectors es considera baix. Els entomòlegs mèdics pensen que dit fet pot relacionar-se amb quatre problemes principals: retard entre la identificació de la malaltia en humans i el desenvolupament d'investigacions de camp, dificultat per trobar les cases o nuclis poblats infectats, mètodes ineficients de mostreig i la desinsectació prematura de les zones d'infecció sense prèvia presa d'exemplars entomològics. Això fa evident la necessitat de protocols de vigilància coordinats i més acurats en els focus d'amplificació dels insectes vectors en els països afectats.[244]
És un consens que el virus es transmet pels mosquits i, per això, el control del vector és un element essencial per reduir la incidència de la malaltia. Òbviament, una forma bàsica de prevenció és emprar repel·lents d'insectes a les zones de risc, com ara els DEETs, la picaridina o l'oli de Corymbia citriodora (p-mentà-3,8-diol o PMD).[245] A banda del PMD, altres olis essencials (com per exemple els que contenen citronel·lol) tenen propietats repel·lents i es poden emprar encapsulats per evitar una ràpida evaporació.[246] La nepetolactona, component principal de l'oli de Nepeta cataria, altera les capacitats quimiosensorials dels culícids i es considera també un repel·lent eficaç.[247]
A hores d'ara, es treballa en una nova forma de control del mosquit Aedes aegypti, infectant-lo amb el bacteri intracel⋅lular Wolbachia.[248] És un microorganisme que afecta al 40% dels artròpodes terrestres.[249] Aquest bacteri endosimbiòtic, Wolbachia pipientis, limita la disseminació del virus pels teixits de l'interior del mosquit, de forma que la seva saliva no conté partícules transmissibles de ZIKV.[250] S'ha demostrat que la soca wMel del bacteri redueix significativament la infecció pel ZIKV i pel virus Chikungunya en aquests mosquits, i que les femelles d'Aedes aegypti portadores de dita soca de Wolbachia tenen una capacitat molt disminuïda per transmetre els dos tipus de virus.[251] De fet, el bacteri actua com un sistema immunitari accessori del mosquit i ocasiona un efecte d'incompatibilitat citoplàsmica que limita la viabilitat dels ous de l'hoste.[252] La soca wMel, a més d'alterar els paràmetres de digestió de la sang ingerida pel mosquit, disminueix determinades proteïnes dels gens precursors de la reproducció necessàries per una correcta oogènesi.[253] Models predictius indiquen que aquest procediment pot tenir un impacte efectiu, però lent, en l'espai ocupat per les poblacions del mosquit objecte de control.[254] Observacions fetes a diferents llocs d'Austràlia durant dos anys confirmen els resultats d'aquests models i demostren que la dinàmica de l'esmentat bacteri sobre les poblacions del vector Aedes aegypti pot ser una bona estratègia per controlar l'expansió del ZIKV a zones urbanes.[255] Una altra soca d'aquest bacteri pertanyent al clade B de l'espècie, anomenada Wolbachia wStri i aïllada en el delfàcid Laodelphax striatellus, té la capacitat d'inhibir almenys dos mecanismes independents implicats en la replicació del virus.[256]
La FDA ha autoritzat una prova de control del vector Aedes aegypti emprant mosquits genèticament modificats,[257] a Key Heaven, una de les illes inferiors dels Keys de Florida.[258] Brasil ha iniciat al setembre de 2016 un proyecte d'alliberament general en dos anys d'uns 100 milions de mosquits modificats, de la soca OX513A (anomenats Friendly Aedes™), a 10 districtes del municipi de Piracicaba.[259] Aquests tipus de mosquits incorporen un marcador fluorescent per facilitar la seva identificació. També s'ha estudiat la possibilitat d'alliberar a determinades zones milions de mosquits mascles esterilitzats per radiacions gammma.[260] Aquest mètode ha estat assajat al Brasil per tècnics de l'Agència Internacional de l'Energia Atòmica i de la FAO, emprant drons per estendre de forma regular i eficaç els mosquits estèrils en bones condicions sobre àmplies àrees de terreny, ja que el seu alliberament des de medis aeris convencionals provoca lesions a molts exemplars.[261]
Una empresa privada, amb suport dels NIH, desenvolupa una trampa entomològica de baix cost, emprant aigua i un odoritzant que li confereix una olor a fenc, per atraure i eliminar els mosquits vectors.[262] Un larvicida relativament nou del grup dels anàlegs de l'hormona juvenil, el piriproxifèn,[263] ha demostrat la seva eficàcia atacant les formes primerenques dels mosquits vectors a l'Amazònia.[264] Un altre oli essencial, el de la planta asiàtica Blumea eriantha, que te abundants terpens, sesquiterpens i aldehids ha estat proposat com un larvicida alternatiu 'natural' per controlar els mosquits vectors del ZIKV i d'altres malalties.[265] És un oli ja conegut per la seva capacitat antimicrobiana[266]
Un altre sistema per reduir el nombre de mosquits vectors en les superfícies aquàtiques és utilitzar peixos larvívors, com ara Gambusia affinis, Gambusia holbrooki o Poecilia reticulata. És un procediment emprat des de fa anys en campanyes antipalúdiques i en alguns països s'ha aplicat contra el ZIKV. Existeixen, però, dubtes sobre la reducció real de mosquits adults que els peixos poden aconseguir. A més la introducció d'espècies no natives comporta un greu impacte ambiental (algunes són predadores també de larves i ous d'altres peixos) que acaba per incidir fora de la regió objectiu del control.[267]
La infecció es transmet per via sexual en els humans.[268] El primer cas de transmissió del virus per aquesta via fou descrit l'any 2011, després del contagi no vectorial de la dona d'un científic americà infectat al sud-est de Senegal un temps abans.[269] De fet, l'investigador i la seva dona van presentar un quadre similar al dengue a poc de tornar aquell d'Àfrica el 2008, però les serologies no confirmaren aquesta malaltia. Durant una conversa sobre el cas amb un entomòleg mèdic, l'any 2010, es va apuntar la possibilitat d'una infecció per ZIKV. Les noves analítiques de les mostres de sèrum de 2008 van demostrar que la infecció soferta pel científic i la seva dona, la qual no havia viatjat a Senegal, fou causada pel ZIKV. En aquell moment, el ZIKV només era present al brot de Micronèsia i el fet de la transmissió sexual del virus fou ignorat.[270] Ha estat filiada la transmissió dona-home per aquesta via, fet no descrit fins al 2016 i que fa recomanable augmentar les mesures de precaució,[271] ja que el virus es replica amb facilitat al tracte vaginal i manté la capacitat infecciosa durant setmanes.[272] Es detecta a frotis vaginals 15 dies després de la presa de la mostra. A l'Estat Espanyol el primer cas de transmissió home-dona per aquesta via fou detectat el juny de 2016 a Madrid.[273] La infecció per via sexual pot donar-se sense símptomes evidents.[274] Si bé aquesta no és la principal forma de transmissió i no pot ser considerada per se una veritable malaltia de transmissió sexual, encara no es coneix exactament la persistència temporal del virus als fluids i mucoses en funció de les variables individuals, motiu que fa considerar el contacte sexual com un potencial "reservori" víric a zones i estacions de l'any amb baixa presència de mosquits.[275] Aquestes circumstàncies, en conjunt, fan que un sector científic recomani que la infecció pel ZIKV sigui contemplada com una MTS des del punt de vista de la salut pública.[276] Algunes estimacions matemàtiques indiquen que la capacitat de transmissió sexual del virus està subestimada i que és un factor que pot originar fàcilment endemismes de la malaltia.[277]
Ha estat demostrada la presència d'ARN del ZIKV al semen, uns 6 mesos després dels primers símptomes infecciosos.[278] Ara bé, dita presència no implica que el semen sigui infecciós tot aquest període de temps. De fet, els investigadors dels CDC afirmen que els homes infectats pel ZIKV i simptomàtics poden transmetre la infecció per via sexual durant un mes després de l'adquisició del virus.[279] Proves fetes en ratolins mascles del tipus C57BL/6 (una variant especialment seleccionada per treballs de laboratori) indiquen que el ZIKV provoca orquitis-epididimitis i altera l'espermatogènesi d'aquests animals.[280] També s'ha observat que la infecció per la soca MEX2-81 del virus provoca atròfia testicular i baixos nivells de testosterona sèrica en el mateix tipus de ratolins.[281] La replicació del virus té lloc en l'epiteli dels túbuls seminífers, una zona bastant resguardada de l'activitat immunitària.[282] Per aquest motiu, alguns especialistes opinen que el ZIKV en semen es pot convertir en una font de transmissió d'especial rellevància en regions no vectorials.[283] Cap estudi portat a terme fins a la data demostra que la infecció per ZIKV comporti -o que no comporti- infertilitat masculina persistent en humans.[284] Tot i així, alguns especialistes consideren molt possible el fet ja que diverses malalties virals causen aquest trastorn, especialment les que lesionen les cèl·lules de Sertoli.[285] Un estudi experimental realitzat per investigadors taiwanesos també amb ratolins afirma que l'ebselen (un fàrmac antioxidant que s'utilitzava en la prevenció de l'ictus) millora els danys testiculars i impedeix la transmissió sexual del ZIKV en dits múrids.[286] La detecció d'ARN del virus en mostres de semen de donants asimptomàtics representa un nou risc que implica la pràctica sistemàtica de proves analítiques serològiques o moleculars als bancs de semen.[287]
Hi ha investigadors que recomanen programar l'embaràs, a determinades zones, en funció del cicle vital dels mosquits vectors del ZIKV.[288] Models epidemiològics indiquen que ajornar l'embaràs més de sis mesos als llocs afectats pot ser recomanable per reduir els casos de malformació fetal, si bé és una mesura que s'ha d'acompanyar dels corresponents programes d'educació parental.[289] Es recomana també que els viatgers provinents de zones amb ZIKV, encara que no presentin cap símptoma, procurin evitar les picades de mosquit -almenys durant les tres setmanes posteriors a la tornada- per tal d'impedir l'extensió del virus entre la població local de mosquits no infectats, però potencials vectors de la malaltia.[290]
El 2016 es va proposar una sistematització metodològica d'accés obert en la recerca de nous fàrmacs, per tractar amb eficàcia aquest tipus d'infecció vírica.[291] Han estat identificats compostos orgànics de molècula petita (emiracsan, niclosamida i un inhibidor cinasa dependent de ciclina conegut com PHA-690509) que redueixen la mort neuronal causada pel ZIKV i podrien ser útils en el desenvolupament de fàrmacs antivirals.[292] Treballs experimentals fan pensar que la nanchangmicina (un antibiòtic poliestèric obtingut de la fermentació del bacteri Streptomyces nanchangensis),[293] és capaç de bloquejar els primers passos emprats pel ZIKV per penetrar dintre de les cèl·lules; és a dir, altera el mecanisme d'endocitosi depenent de clatrina que utilitza per internalitzar-se.[294] El flavonoide glicosilat isoquercetina[295] també impedeix l'entrada de soques africanes i asiàtiques del virus dins de diferents línies cel·lulars humanes cultivades.[296]
Un mecanisme per impedir la replicació del ZIKV és crear antivirals que alterin els enzims que regulen el seu cicle vital. Concretament, bloquejar una helicasa ARN pròpia dels flavivirus -la NS3-Hel, de la qual es coneix molta informació estructural- responsable de la replicació genòmica i de la síntesi de l'ARN viral.[297] També, gràcies al coneixement estructural detallat de les seves metiltransferases (MTs), es podrien dissenyar fàrmacs per alterar mecanismes catalitzadors necessaris en la replicació del virus.[298] En concret, es creu possible desenvolupar molècules que alterin les funcions de la NS5-MT del ZIKV.[299]
Un fàrmac antiviral emprat per tractar l'hepatitis C crònica, el Sofosbuvir, ha demostrat que pot inhibir la replicació del ZIKV -alterant la seva ARN-polimerasa i provocant errors en el mecanisme de replicació viral. És un producte aprovat clínicament i es contempla utilitzar-lo contra les infeccions pel ZIKV.[300] Models matemàtics aconsellen una dosi dues vegades superior a la utilitzada en els casos d'infecció pel VHC; així com avaluar in vivo els possibles efectes secundaris.[301] Ara per ara, sembla reduir experimentalment la mortalitat i les seqüeles a curt i llarg termini en rosegadors infectats pel virus.[302]
La cavinafungina, una substància extreta del fong Colispora cavincola[303] que creix als forats dels troncs dels arbres, altera també la replicació del ZIKV i del virus del dengue.[304] S'ha considerat que la nitazoxanida (un compost antiparasitari i antivíric),[305] té un gran valor potencial per controlar la infecció pel ZIKV, ja que és un fàrmac aprovat per la FDA per tractar oralment gestants sense risc fetal.[306] Molts altres compostos han estat, o estan avui dia, en procés d'investigació com a possibles elements terapèutics: la gemcitabina (un anàleg de nucleòsid del grup de les pirimidines), la suramina (un antihelmíntic), el 7-DMA (un inhibidor de la polimerasa viral), el T-705 i el T-1105 (també inhibidors de la polimerasa del virus)[307] o el NITD008 (un anàleg específic de l'adenosina).[308]
Certs polifenols podrien tenir efectes virucídics contra els Flavivirus (ZIKV, virus del dengue i virus del Nil Occidental) que alterarien la seva capacitat infecciosa.[309] El silvestrol[310] un compost natural pertanyent a la família de les rocaglamides i provinent de la planta Aglaia foveolata, inhibeix la replicació del ZIKV en diferents línies de cèl·lules humanes cultivades.[311]
Un grup de la Universitat Purdue ha aïllat un anticòs humà d'una persona infectada pel ZIKV amb una regió Fab (en anglès: Fragment antigen-binding) que s'uneix a una proteïna de la càpside del virus i neutralitza soques virals d'Àfrica, Àsia i Amèrica, i que sembla capaç de reduir significativament la infecció i la mort fetal en ratolins.[312] La viperina (una proteïna cel·lular capaç d'inhibir molts virus d'ADN i ARN, com el VHC, el VCHIK, el DENV, el WNV o alguns influenzavirus) i els seus mecanismes d'expressió en l'hoste, podrien ser uns factors determinants per impedir la replicació del ZIKV i dissenyar noves estratègies contra la infecció.[313]
Científics europeus han posat de manifest que la proteïna neurodesenvolupant Musashi 1 (MSI1)[314] interactua amb el genoma del ZIKV, afavorint així la replicació viral.[315] Aquest fet, almenys en part, pot explicar el mecanisme patogènic que origina les anomalies neurals que pateixen molts fetus infectats. Dita interacció entre una regió específica de l'ARN del virus i la MSI1 (proteïna amb una alta expressió en les cèl·lules progenitores nervioses a partir de les quals es creen les neurones i els astròcits) determina els danys que la infecció provoca en el SNC en formació.[316]
Una altra línia d'investigació és la recerca de substàncies que actuïn contra una proteasa determinada del virus, la NS2B-NS3pro, la qual és necessària en el procés de replicació del ZIKV. Amb aquest objecte, han estat proposats diversos compostos, com la bromocriptina (un fàrmac utilitzat per tractar la malaltia de Parkinson i trastorns hipòfisaris). També es treballa per trobar inhibidors al·lostèrics de dita proteasa en plantes comestibles.[317]
L'heparina no té un efecte significatiu sobre la replicació del virus; per contra, disminueix els danys citopàtics provocats pel ZIKV en les cèl·lules progenitores neurals humanes.[318] Es creu que l'azitromicina pot actuar contra la infecció pel virus de les cèl·lules glials,[319] si bé aquesta propietat no ha estat confirmada per estudis in vivo.[320]
In vivo i in vitro, l'emetina (un alcaloide en desús que s'emprava com a medicament antiamèbic) i el seu derivat cefaelina[321] limiten la infectivitat del ZIKV i del virus Ebola a través de dos mecanismes moleculars: la inhibició de la replicació viral i la reducció de la seva capacitat d'entrada a les cèl·lules.[322]
Fent un repàs als treballs d'investigació realitzats en els darrers dos anys per trobar antivirals efectius contra el ZIKV emprant diverses metodologies, cal destacar les proves fetes amb substàncies ja utilitzades en el tractament d'altres virasis i la recerca de múltiples molècules bioactives potencialment útils (antiparasitàries, antibiòtiques, anticanceroses, antiinflamatòries, modificadores dels enzims virals, inhibidores de la síntesi de nucleòsids, etc.), algunes esmentades en aquest article. Un problema important per validar aquestes teràpies antivirals és que són especialment necessàries en grups de persones molt especials (dones embarassades i poblacions sense suficient suport mèdic o amb altres patologies afegides). Això implica una avaluació molt acurada dels possibles efectes indesitjats abans d'aprovar el seu ús clínic.[323]
Alguns assajos clínics, amb l'objectiu d'aconsseguir una vacuna contra el virus, es troben en fases avançades.[324][325] Aquests estudis -proves controlades aleatòries- requereixen un disseny molt acurat, ja que els possibles efectes nocius sobre el sistema nerviós a llarg termini són, a hores d'ara, desconeguts.[326] En especial, cal tenir en compte els possibles efectes teratogènics de les substàncies a assajar en dones embarassades i les particulars característiques farmacocinètiques i farmacodinàmiques que comporta la gestació.[327] S'ha publicat, segons estudis in silico, que la vacunació contra certes variants de grip (Influenzavirus A) podria ser un factor coadjuvant en la prevenció de les infeccions pel ZIKV.[328] Actualment, més de 30 possibles vacunes estan en desenvolupament preclínic seguint les pautes de l'OMS de 2016.[329]
Els NIH han aprovat un assaig (fase I/Ib), en grups de voluntaris,[330] d'una vacuna experimental contra el ZIKV (GLS-5700, InOvio/GeneOne).[331] L'Institut Walter Reed, el NIAID (National Institute of Allergy and Infectious Diseases) i Sanofi-Pasteur, van engegar un assaig (fase I) per probar una vacuna basada en virus inactivats amb formol, a l'octubre de 2016.[332] Segons un treball publicat a principis de 2018, els resultats d'un grup de tres assajos a tres centres diferents d'aquesta vacuna 'candidata' indiquen que és segura i immunogènica en humans sans.[333] Un equip multidisciplinari publicà també a l'octubre de 2016 els seus resultats sobre una vacuna efectiva en primats no humans.[334] Les proves d'una nova vacuna, basada en molècules de mRNA amb nucleòsids modificats (encarregades de codificar determinades glicoproteïnes d'una soca de ZIKV de l'any 2013) i encapsulades en nanopartícules lipídiques han demostrat un alt nivell d'eficàcia protegint macacos i ratolins de la infecció, emprant una dosi única.[335] Alterant de forma específica el mRNA, s'aconsegueix evitar la reactivitat creuada epitòpica amb el virus del dengue i reduir possibles efectes adversos de la vacuna. A més, dites nanopartícules podrien incloure mRNA addicional codificador d'altres proteïnes pròpies dels flavivirus (com la NS1), augmentant així la resposta de protecció.[336] Aquests dos projectes de vacuna, el del grup de Pardi i el del grup de Richner, són -almenys per ara- els que semblen tenir més possibilitats d'aconseguir una immunització activa contra el virus.[337] Al març de 2017, el NIAD va iniciar un assaig en fase 2/2b[338] d'una vacuna ADN experimental en un grup de 2490 persones sanes dels EUA i Amèriques del Sud i Central. Aquesta vacuna es basa en un plasmidi amb gens que codifiquen dues proteïnes de superfície del ZIKV. Una vegada injectades aquestes proteïnes formen partícules que imiten la presència del virus i desenvolupen la resposta immune. La vacuna no porta material infecciós i no pot ocasionar la febre de Zika.[339] Una altra vacuna amb virus inactius de la soca africana MR 766 sembla tenir una bona capacitat protectora en models experimentals in vivo murins.[340] Una vacuna de nova generació, la GLS-5700, que conté ADN sintètic capaç de provocar en humans una bona resposta immune davant determinats antígens del ZIKV amb una seguretat adequada, es troba es una fase I d'assaig clínic.[341]
Les característiques immunològiques de la infecció pel ZIKV són especialment complexes i s'han identificat reaccions creuades ZIKV-DENV per part de les cèl·lules T, a banda de la resposta antigènica comuna abans comentada. Una infecció prèvia pel DENV potencia els efectes del ZIKV, mentre que dos o més semblen tenir un efecte protector contra ell que depèn en essència del lapse de temps transcorregut entre les infeccions de dengue i no de la soca causal. Inversament, alguns investigadors creuen que la immunitat desenvolupada després de la infecció pel ZIKV podria tenir efectes protectors creuats davant el dengue.[342] Aquestes particularitats, encara no enteses del tot pels immunòlegs, són crucials per dissenyar una vacuna efectiva.[343]
Un nou projecte: OpenZika (IBM World Community Grid), que utilitza una plataforma BOINC, ha estat engegat el 2016. El seu propòsit és recollir dades genòmiques i clíniques dels principals centres investigadors i bancs de biologia molecular, per afavorir la recerca i desenvolupament d'estratègies globals i productes terapèutics de darrera generació contra el ZIKV.[344] Un dels objectius del projecte és emprar l'homologia molecular i trobar proteïnes diana similars en altres microorganismes, de les quals sigui coneguda ja la seva estructura a nivell atòmic.[345] En aquesta línia, s'ha fet una compilació de totes les proteïnes produïdes pel ZIKV i dels genotips virals resultants, disponible a la Virus Pathogen Resource.[346] La necessitat d'harmonitzar els protocols globals de prevenció i actuació ha estat reconeguda a diferents conferències internacionals.[347] Es pot veure una tendència creixent en el nombre d'articles relacionats amb el ZIKV indexats a PubMed en els darrers anys: 2013=3; 2014=23; 2015=37; 2016=1.564; 2017=1.648. Aquest gran increment de publicacions comporta un risc de parcialitat o de manca de rigor metodològic, especialment en els criteris de selecció i control de casos, que pot ser evitat seguint els protocols estandarditzats d'investigació clínica i epidemiològica elaborats per centres de referència internacional.[348] Malgrat els considerables esforços científics fets arreu del món per conèixer la virologia, patogenètica, transmissió, curs clínic i diagnosi del ZIKV, encara no ha estat assolida una bona implementació dels resultats en la pràctica mèdica general. Als EUA, per exemple, només es recomanà entre gener i desembre de 2016 la realització de proves de neuroimatge en un 25% dels nens exposats al virus i un alt percentatge d'ells no fou sotmès a tests de detecció específics.[349]
S'està valorant la possibilitat de crear nous models d'estudi de la microcefàlia per ZIKV -induïda experimentalment- emprant organoids cerebrals millorats o bé organoids de regions específiques del cervell. Aquest mètode permetria simular molt acuradament els efectes del virus sobre les molècules del cervell humà en desenvolupament i seria una eina útil per a facilitar sense risc la validació de l'eficàcia de nous fàrmacs.[350] Ara com ara, s'ha demostrat que el virus altera el creixement i la viabilitat d'organoids cerebrals i de neuroesferes (grups de cèl·lules mare neurals cultivades que s'utilitzen per estudiar in vitro les cèl·lules nervioses precursores).[351] Els organoids cerebrals recreen aspectes de la corticogènesi fonamentals per conèixer els tipus de resposta de la immunitat innata induïts pel ZIKV que desencadenen l'apoptosi de les cèl·lules progenitores cerebrals.[352] A banda dels organoids cerebrals, els testiculars són una eina d'investigació molt valuosa per l'estudi dels danys que provoca el virus en aquestes gònades. La infecció de dits organoids posa de manifest un descens de la viabilitat general de les seves cèl·lules, probablement relacionat amb fenòmens apoptòsics, i una baixa expressivitat dels marcadors corresponents als espermatogonis i a les cèl·lules de Sertoli.[353]
Una línia de recerca d'especial interès és la creació de models de cultiu 3D de cèl·lules endotelials de la barrera hematoencefàlica humana, que ajudin a identificar els mecanismes emprats pel ZIKV i altres virus d'ARN per creuar-la i accedir al SNC.[354]
Alguns investigadors proposen fer prediccions dinàmiques i millorar els sistemes de vigilància tradicionals dels brots de ZIKV, emprant les dades en temps real obtingudes per mitjà de l'eina Google Trends (creada per conèixer el nivell de cerca d'una paraula clau durant un període de temps determinat).[355]
Una anàlisi dels vídeos de YouTube en anglès relatius al ZIKV revela que nomes una part molt petita d'ells ha estat editada per professionals o institucions sanitàries, mentre que la majoria es deu a la feina de particulars o ha sigut extreta de notícies d'Internet o de TV. Això posa de manifest la necessitat de presentar informació fonamentada en evidències científiques en aquest lloc web.[356]
L'Hospital La Paz-Carlos III va crear el febrer de 2016 una línia d'atenció telefònica per facilitar informació actualitzada i contrastada sobre el virus als viatgers. Durant els primers 6 mesos de funcionament, en molts casos no fou necessària una consulta presencial en un servei especialitzat abans o després del viatge.[357]
Científics dels EUA han identificat les regions peptídiques que diferencien el ZIKV dels altres Flavivirus transmesos per mosquits.[358] Diversos fàrmacs peptídics experimentals, com el Z2, derivats d'una part de la proteïna E (embolcalladora) del ZIKV, podrien ser emprats contra la infecció, ja que lesionen la membrana dels Flavirirus.[359]
S'ha aconseguit un domini purificat de la polimerasa d'ARN del ZIKV, actiu in vitro, capaç de sintetitzar de novo el genoma viral. Aquest avenç es considera de gran valor per a la recerca sobre determinats tipus d'inhibidors de la replicació del virus.[360]
Una forma no coneguda fins fa poc d'aquesta virasi és la bifàsica (observada anteriorment en el dengue, però). Això significa una reaparició de la simptomatologia després d'una milloria inicial o, inclús, una vegada resolta per complet. No es coneix la causa del fet o si comporta un pitjor curs de la malaltia. Es pensa que podria ser el resultat d'una virèmia silent perllongada o de la persistència del ZIKV a "llocs santuari" no determinats encara.[361] A mesura que augmenta la casuística, creix la varietat de problemes mèdics relacionats amb la infecció. Ha estat publicat el primer cas de meningoencefalitis pel ZIKV en un malalt immunodeprimit en el context d'un trasplantament de cor.[362] La coinfecció ZIKV/VCHIK és possible i pot tenir resultats fatals en persones amb malalties reumatològiques -com ara el LES- sotmeses a tractament immunosupressor, ja que l'efecte citopàtic dels dos virus incideix negativament sobre la funció renal d'aquest tipus de pacients.[363] Un estudi realitzat en nens afectes de la síndrome congènita per ZIKV demostra l'existència en ells de bufeta neurògena (alteració de la dinàmica miccional amb origen en el sistema nerviós).[364]
Un descobriment fonamental per entendre perquè la síndrome congènita afecta a uns individus i a altres no, és l'existència d'una susceptibilitat intrínseca en les cèl·lules progenitores neurals d'alguns fetus, que ha estat estudiada en bessons i que es creu relacionada amb mecanismes oligogènics i/o epigenètics.[365] En humans, la ràtio mares gestants simptomàtiques versus mares asimptomàtiques en els casos de síndrome congènita és 1:1.[366]
Experiments en rosegadors indiquen que una primera infecció asimptomàtica pregestacional pel ZIKV té efectes protectors contra una reinfecció i que aquests efectes es mantenen durant l'embaràs. Això obra la porta a noves vies terapèutiques dirigides a evitar el dany que provoca el virus en mares i fetus. El sèrum adequadament preparat de donants o anticossos monoclonals purificats humans amb les corresponents característiques genotípiques podrien ser algunes de les possibles opcions.[367]
Modificant lleugerament determinats anticossos (unes proteïnes immunitàries anomenades anti-EDE1) presents en malalts humans amb dengue, s'ha aconseguit tractar eficaçment la infecció pel ZIKV en ratolins i evitar inclús la transmissió del virus a les cries d'animals gestants infectats. Això podria ser d'utilitat per dissenyar una futura vacuna dual.[368]
D'altra banda, el virus del Zika té un efecte oncolític sobre les cèl·lules precursores del glioblastoma. Dit d'una altra manera, almenys de forma experimental, és capaç d'infectar i matar un tipus específic de cèl·lules tumorals cerebrals, amb una mínima afectació del teixit normal d'un cervell adult de rosegador. Això fa pensar en la futura possibilitat de modificar genèticament el virus i obrir una nova línia de recerca terapèutica en el tractament de dita neoplàsia.[369] L'anàlisi dels canvis citopàtics de les cèl·lules tumorals infectades amb ZIKV, utilitzant tècniques avançades d'espectrometria de masses, indica que el virus té la capacitat de desencadenar la síntesi endògena de molècules de H-digoxina en les cèl·lules del glioblastoma (un glicòsid que provoca l'apoptosi cel·lular de determinats processos cancerosos, com ara el melanoma o el càncer de mama), induint així la seva mort.[370] In vivo i in vitro, científics brasilers han posat de manifest que el ZIKV elimina selectivament cèl·lules embrionàries precursores d'altres línies tumorals molt agressives, com ara les del medul·loblastoma i del tumor teratoide/rabdoide.[371]
Les dues varietats epidemiològiques del virus, l'africana i l'asiàtica, afecten en particular als astròcits, alterant el seu reticle endoplasmàtic i provocant l'alliberament de citoquines i quimiocines proinflamatòries en els cervells infectats. Això confirma la hipòtesi que sosté que ambdues línies del ZIKV poden ocasionar danys similars en el SNC.[372]
Un grup de treball multinacional, dirigit per científics del Centre Mèdic de la Universitat de Texas a Galveston, ha descobert que determinades parts del ZIKV són molt similars a components del sistema immune de l'hoste, fet que podria desencadenar una resposta defensiva del cos contra el virus i també contra el seu propi sistema del complement, el qual és important pel desenvolupament del fetus i per la correcta funcionalitat immunitària. Aquest error d'identificació pot ser la causa dels defectes congènits i dels trastorns neurològics en adults que pateix una fracció dels individus infectats pel ZIKV. Les anàlisis cel·lulars fetes amb plataformes bioinformàtiques demostren que la proteïna E del virus comparteix un gran nombre de característiques amb una proteïna de l´hoste anomenada proteïna del sistema del complement C1q, el que fa pensar que el seu comportament biològic és pràcticament idèntic. Els investigadors observaren alts nivells d'anticossos anti-C1q en la sang de ratolins i primats no humans, fet que indica que el virus indueix una potent reacció autoimmunitària.[373]
Investigadors de la Universitat Emory han comprovat que -en cries de Macaca mulatta- la infecció postnatal pel ZIKV provoca anomalies cerebrals durant els primers mesos de vida que modifiquen la seva conducta. En un grup d'animals infectats als pocs dies de néixer es desenvoluparen alteracions en determinades àrees del cervell responsables de la visió i de les emocions i en les connexions entre l'amígdala i l'hipocamp, observant-se en ells respostes estranyes davant situacions d'estrès. Es desconeix, però, si lesions similars poden afectar a llarg termini la salut mental dels nadons exposats al virus.[374] S'ha observat que la transmissió materno-fetal del virus és molt alta en primats no humans. L'administració subcutània de dosis moderades de la línia asiàtica del ZIKV en les mares, durant el primer o a finals del segon/inici del tercer trimestre de l'embaràs comporta la infecció de tots els fetus, apreciant-se patologia en la interfície placentària i una variable distribució de l'ARN viral en el fetus.[375] Una combinació d'anticossos monoclonals provinents de la sang d'una persona infectada i que prèviament havia aconseguit impedir la infecció en macacos,[376] ha demostrat la capacitat d'eliminar el virus en la majoria d'exemplars de Macaca mulatta gestants infectats, però no evitar l'entrada del ZIKV al líquid amniòtic i la morts dels fetus, ja que dits anticossos no poden creuar la barrera placèntaria en quantitats suficients.[377] En aquesta línia de recerca, científics xinesos han demostrat que un anticòs monoclonal humà, el ZK2B10, exerceix una potent activitat neutralitzant contra el virus, ja que dóna protecció complerta contra ell a ratolins sense infectar (gestants o no) i minora de forma significativa la patologia tissular dels exemplars infectats amb una única injecció.[378] Un problema que afecta la interpretació general d'aquests tipus de treballs és la dificultat per comparar entre ells els resultats de la fase I dels diferents estudis efectuats i també per fer-ho amb els dels anticossos neutralitzants utilitzats en vacunes ja aprovades contra altres Flavivirus (virus de l'encefalitis japonesa, virus de l'encefalitis per paparres[379] i febre groga) ja que les característiques de dits anticossos són diverses i no existeixen per ara estàndards definits. A més dels assajos clínics en curs, són nombroses les investigacions en marxa relacionades amb la profilaxi passiva i el desenvolupament de vacunes candidates per protegir els teixits reproductius.[380]
El patró d'activitat del virus en els cervells d'embrions de pollastre infectats indica que el ZIKV lesiona de forma selectiva unes zones determinades encarregades d'expressar substàncies claus en la regulació del desenvolupament cerebral primerenc, anomenades morfògens. Això implicaria que la infecció és capaç de danyar indirectament moltes cèl·lules del SNC atacant només alguns punts crítics de la neurogènesi embrionària. Aquesta troballa pot ajudar als investigadors a interpretar millor la capacitat teratogènica del ZIKV.[381]
Fonamentant-se en observacions empíriques i models matemàtics, un grup d'investigadors ha determinat que la temperatura òptima de transmissió del ZIKV és cinc graus més alta que la del virus del dengue, una dada que fa reconsiderar a la baixa les estimacions predictives sobre la possible expansió mundial del ZIKV segons criteris d'idoneïtat ambiental.[382]
El virus del Zika (ZIKV) és un virus del gènere Flavivirus, família Flaviviridae, grup IV de la Classificació de Baltimore. Té interès en medicina per produir la febre del Zika. La febre i el virus porten el nom del bosc de Zika, a Uganda, on el virus es va aïllar per primer cop el 1947.
Les infeccions, conegudes com a febre del Zika, sovint no provoquen símptomes o són símptomes lleus. Des dels anys cinquanta, s'ha detectat la presència del virus dins d'un estret cinturó equatorial de l'Àfrica cap a Àsia. El 2014, el virus s'estengué a l'est a través de l'oceà Pacífic cap a la Polinèsia Francesa, després cap a l'illa de Pasqua i, el 2015, a Mèxic, Amèrica Central, el Carib i Amèrica del Sud, on el brot va assolir el caràcter de pandèmia.
El virus del Zika està emparentat taxonòmicament amb els virus del dengue, la febre groga, l'encefalitis japonesa, el virus de l'encefalitis de Saint Louis i el virus del Nil occidental. Filogenèticament és molt proper al virus Spondweni, amb el qual forma un clade dintre del gènere Flavivirus. Emprant serologies, no és fàcil veure les diferències entre aquests dos virus.
Habitualment, la malaltia que provoca és semblant a una forma tènue de dengue, si bé –en alguns casos d'infecció en dones embarassades– pot comportar lesions cerebrals fetals, sobre tot si la infecció es produeix durant el primer trimestre de gestació. Així mateix, l'infecció materna implica un risc d'avortament.
Alguns investigadors vinculen la infecció congènita pel ZIKV amb el desenvolupament de greus anomalies articulars (artrogriposi) en determinats nadons. El ZIKV roman en el nadó infectat més de dos mesos. També s'han descrit lesions oculars de diferents tipus en nens de mares infectades. El virus és capaç d'inflamar greument la còrnia, la retina i el nervi òptic del fetus/nounat, fet que pot comportar la pèrdua de la visió, o provocar una important atròfia de la màcula. En casos congènits, s'ha observat l'existència de coloboma, cataractes, glaucoma, ectòpia del cristal·lí, microftàlmia, estrabisme (convergent i divergent) i alteracions pigmentàries predominantment bilaterals. Tanmateix, és una causa d'edema generalitzat (hydrops) fetal no-immune. En adults, s'han identificat diversos casos d'uveïtis, tant anteriors com posteriors i de grau molt variable, i també pèrdues transitòries d'audició. En persones sota tractament immunosupressor el ZIKV pot ocasionar lesions corioretinals no necrotitzants. La principal diferència entre les alteracions oculars de la síndrome congènita i de la infecció adquirida és la presència en aquesta d'uveïtis activa.
Estudis ecocardiogràfics indiquen una prevalència alta de de defectes cardíacs en nadons afectes de la síndrome congènita per ZIKV, en especial del septe (no tots impliquen alteracions hemodinàmiques significatives).
Aelod o deulu'r Flaviviridae ydyw'r firws Zika (neu ZIKV) a'r genws Flavivirus,[3][4] sy'n cael ei gario liw dydd gan y mosgito Aedes aegypti.[4] Daw'r enw Zika o'r Fforest Zika yn Wganda lle gwelwyd y firws yn 1947 am y tro cyntaf.[5]
O fewn bodau dynol, mae'r symtom cyntaf yn ddigon diddim didda ac ysgafn a gelwir ef yn 'dwymyn Zika', sydd wedi'i hastudio o fewn rhuban o dir o Affrica i Asia ers yr 1950au. Am ryw reswm, yn 2014, ymledodd y firws tua'r dwyrain ac ar draws y Cefnfor Tawel ac i Ynys y Pasg. Yn 2015 ymledodd ymhellach - i ganol America, y Caribî a De America, lle cafwyd epidemig y firws Zika.[6] Mae'r firws Zika yn perthyn yn eithaf agos i gwibgymalwst (neu 'deng'), y dwymyn felen, Japanese encephalitis a firws Gorllewin y Nil.[7] Mae'r dwymyn a geir yn ddigon tebyg i gwibgymalwst,[7] a chaiff ei thrin drwy orffwyso'r claf,[8] ond nid oes unrhyw feddyginiaeth a all ei gwella. Ceir cysylltiad rhwng y dwymyn Zika â Microceffali mewn babanod newydd eu geni, pan fo'r fam wedi'u heintio a throsglwyddir y firws i'r plentyn yn y groth.[9][10].
Yn Ionawr 2016 cyhoeddodd Canolfan Atal Heintiau Unol Daleithiau'r America (CDC) ganllawiau manwl ynglŷn â theithio i'r gwledydd hynny lle mae'r firws yn rhemp, gan gynnwys cymryd gofal cyn dechrau'r daith, canllawiau i ferched beichiog gydag awgrym y dylent ganslo'r daith.[11][12] Dilynwyd y CDC gan nifer o gyrff tebyg mewn gwledydd eraill.[13][14]
Yn Ionawr 2016 hefyd, cyhoeddodd Cyfundrefn Iechyd y Byd ei bod yn bur debygol y gwelir y firws yn ymledu drwy'r rhan fwyaf o'r Americas.[15]
Trosglwyddir y firws Zika gan fosgito yn y genws Aedes, fel yr A. aegypti sy'n weithgar yn ystod y dydd a'r mosgito A. africanus, A. apicoargenteus, A. furcifer, A. hensilli, A. luteocephalus, a'r A. vitattus sy'n byw mewn coedwigoedd. Dengys yr astudiaeth ddiweddaraf (2016) fod cyfnod deor i'r mosgitos hyn oddeutu 10 diwrnod. Wedi i'r pryfyn gael mynediad i'r corff dynol, drwy gyfathrach rhywiol, mae'n turio i mewn i gorff merch, ac i mewn i'w brych ac yn ymosod ar y ffetws cyn ei eni.
Aelod o deulu'r Flaviviridae ydyw'r firws Zika (neu ZIKV) a'r genws Flavivirus, sy'n cael ei gario liw dydd gan y mosgito Aedes aegypti. Daw'r enw Zika o'r Fforest Zika yn Wganda lle gwelwyd y firws yn 1947 am y tro cyntaf.
O fewn bodau dynol, mae'r symtom cyntaf yn ddigon diddim didda ac ysgafn a gelwir ef yn 'dwymyn Zika', sydd wedi'i hastudio o fewn rhuban o dir o Affrica i Asia ers yr 1950au. Am ryw reswm, yn 2014, ymledodd y firws tua'r dwyrain ac ar draws y Cefnfor Tawel ac i Ynys y Pasg. Yn 2015 ymledodd ymhellach - i ganol America, y Caribî a De America, lle cafwyd epidemig y firws Zika. Mae'r firws Zika yn perthyn yn eithaf agos i gwibgymalwst (neu 'deng'), y dwymyn felen, Japanese encephalitis a firws Gorllewin y Nil. Mae'r dwymyn a geir yn ddigon tebyg i gwibgymalwst, a chaiff ei thrin drwy orffwyso'r claf, ond nid oes unrhyw feddyginiaeth a all ei gwella. Ceir cysylltiad rhwng y dwymyn Zika â Microceffali mewn babanod newydd eu geni, pan fo'r fam wedi'u heintio a throsglwyddir y firws i'r plentyn yn y groth..
Yn Ionawr 2016 cyhoeddodd Canolfan Atal Heintiau Unol Daleithiau'r America (CDC) ganllawiau manwl ynglŷn â theithio i'r gwledydd hynny lle mae'r firws yn rhemp, gan gynnwys cymryd gofal cyn dechrau'r daith, canllawiau i ferched beichiog gydag awgrym y dylent ganslo'r daith. Dilynwyd y CDC gan nifer o gyrff tebyg mewn gwledydd eraill.
Yn Ionawr 2016 hefyd, cyhoeddodd Cyfundrefn Iechyd y Byd ei bod yn bur debygol y gwelir y firws yn ymledu drwy'r rhan fwyaf o'r Americas.
Zika virus[1][2] (zkráceně ZIKV,[2] česky virus Zika[3] či virus zika[4]) je virus patřící do čeledi Flaviviridae, který je přenášen komáry egyptskými. Způsobuje horečku zika, která se kromě vysokých teplot projevuje také vyrážkou a bolestí hlavy i kloubů.[5] Vysoké riziko představuje pro těhotné ženy, jejichž dětem může způsobit těžkou vývojovou poruchu mikrocefalii.[6]
Virus šíří komár egyptský a přenos je také možný z komára na jeho vajíčko. V laboratorních podmínkách bylo nakaženo průměrně jedno z 290 vajíček.[7]
Původně se uvádělo, že virus Zika není mezi lidmi nakažlivý.[6] V únoru 2016 ale BBC uvedla, že se virus přenáší mezi lidmi pohlavním stykem.[8] Dle amerických vědců virus přežívá v lidském spermatu, čímž se z nakažených mužů stávají přenašeči tohoto onemocnění.[9]
Krátce poté brazilští zdravotníci potvrdili také přenos viru prostřednictvím krevní transfúze.[10] Aktivní virus byl objeven také ve vzorcích moči a slin.[11]
Ohledně šíření viru se vyskytlo také několik nepravdivých informací. Server Osel.cz zveřejnil aprílový článek o tom, že mezi toxoplasmózou a virem zika může být vazba.[12]
Proti onemocnění neexistuje lék, brazilská vláda usiluje o urychlený vývoj vakcíny. Jedinou prevencí proto zůstává ochrana před komářím bodnutím. Armáda a zdravotníci likvidují stojaté vody, v nichž se komáři množí.[13] Vědci doporučují v postižených oblastech nemít doma žádné nádoby s vodou, protože se tam vyskytují larvy a vajíčka přenašečů. Vyvíjejí také pesticidy, jež by vyhubily komáry i vajíčka, na která je virus přenosný v jednom z 290 případů. To se sice zdá jako nízké číslo, ale v reálných vysokých počtech komárů to představuje riziko, že pokud by byly vymýceni dospělí komáři, nezamezilo by to dalšímu šíření onemocnění.[7]
Inkubační doba u viru zika činí 3–12 dní, přičemž 80 % postižených nevykazuje žádné symptomy.[14]
Pokud člověk v poslední době cestoval do zemí zasažených virovou infekcí Zika, je doporučeno po návratu navštívit lékaře, který provede krevní testy pro vyloučení nákazy. I když u více než poloviny nakažených se nemusí projevit žádné příznaky, mezi popsané příznaky patří horečka, bolest kloubů či svalů a zánět spojivek. Tyto příznaky jsou společné s horečkami dengue a chikungunya. Příznaky jsou obvykle velmi mírné a do týdne odezní.[15]
Virus způsobuje horečku zika, která se kromě vysokých teplot projevuje také vyrážkou a bolestí hlavy i kloubů.[5] Horečka zika obvykle nevyžaduje hospitalizaci v nemocnici.[15]
Virus zika způsobuje vážné poruchy plodu včetně mikrocefalie, která se projevuje zakrněním nebo předčasným ukončením růstu mozku.[16] Zatímco v roce 2014 se v Brazílii s touto vadou narodilo 150 dětí, o rok později jich bylo 2 700.[5] V některých částech Brazílie byl v této souvislosti vyhlášen výjimečný stav. Párům, plánujícím narození potomka, lékaři doporučují odložení početí.[6][17]
Již nejméně pět dětí kvůli viru v Brazílii zemřelo.[13]
Podle Světové zdravotnické organizace může virus zika způsobit také vzácný Guillainův-Barrého syndrom. Toto neurologické onemocnění působí u dospělých dočasné ochrnutí.[7]
Virus byl poprvé objeven v roce 1947 u opic v pralese Zika nedaleko Entebbe v Ugandě.[18][19] První případy nákazy člověka byly hlášeny o sedm let později v Nigérii roku 1954. Pravděpodobně po roce 1945 virus migroval do Jihovýchodní Asie. V roce 2006 byl rozluštěn genetický kód viru. První velká epidemie způsobená virem Zika byla monitorována v Mikronésii, kde v dubnu až květnu 2007 onemocnělo 185 lidí. Několik desítek dalších lidí tvrdilo, že prodělali nemoc s podobnými příznaky, avšak v jejich krvi nebyly zjištěny protilátky. Nebyla tehdy pozorována žádná úmrtí.[19] Ještě na počátku roku 2014 bylo hlášeno okolo 250 nových případů nákazy, zejména v Africe a v Asii. Ovšem podle odborníků mohlo být toto nízké číslo způsobeno tím, že u většiny ostatních případů došlo k záměně s horečkou Dengue a dalšími virovými nákazami, které mají podobné příznaky.[20]
Viroložka Hana Zelená v září 2016 uvedla, že se v České republice nacházelo 12 lidí nakažených virem Zika a 8 lidí s nákazou proběhlou v minulosti.[21] V listopadu roku 2016 se počet mírně zvýšil, a to o 4 lidi nakažené virem Zika a 7 lidí s nákazou proběhlou v minulosti.[22]
V roce 2015 se začal virus dramaticky šířit především v jiho- a středoamerických státech. V roce 2016 už byl zjištěn ve více než dvaceti zemích, např. Brazílie, Kolumbie[23], Ekvádor, Paraguay, Panama, Mexiko.[6] Přední američtí lékaři se obávali, že má virus pandemický explozivní potenciál a Světová zdravotnická organizace odhadovala, že v následujících několika letech může být nakaženo 3 až 4 miliony lidí.[24]
V únoru 2016 vyhlásila Světová zdravotnická organizace (WHO) globální stav nouze, který stáhla v listopadu téhož roku s tím, že už nákaza nepředstavuje ohrožení veřejného zdraví mezinárodního významu.[25] Stěžejní v boji s ní přitom bude výzkum.[26]
V Brazílii byl největší výskyt zaznamenán na severovýchodě země. Případy nákazy se však objevily i na jihovýchodním pobřeží, kde se nachází bývalé hlavní město země Rio de Janeiro, v němž se v srpnu 2016 konaly letní olympijské hry. Brazílie tak v souvislosti s hrami zahájila v únoru 2016 masivní kampaň proti komárům a proti šíření viru a navýšila výdaje ministerstva zdravotnictví. Po celé zemi rozeslala příručky, jak se bránit nákaze, do postižených oblastí plánovala 13. února vyslat 220 000 vojáků, aby ten den obcházeli domácnosti a rozdávali pesticidy a moskytiéry.[27]
Kvůli rekordně silnému kurzu dolaru chtělo mnoho Američanů strávit prázdniny v Jižní Americe. V lednu 2016 ale v souvislosti s dramaticky se šířící nákazou začali měnit plány a cesty odkládat nebo rušit.[24]
Zika virus (zkráceně ZIKV, česky virus Zika či virus zika) je virus patřící do čeledi Flaviviridae, který je přenášen komáry egyptskými. Způsobuje horečku zika, která se kromě vysokých teplot projevuje také vyrážkou a bolestí hlavy i kloubů. Vysoké riziko představuje pro těhotné ženy, jejichž dětem může způsobit těžkou vývojovou poruchu mikrocefalii.
Zikavirus (ZIKV) er en virus i familien flavivirus. Virusen overføres af Aedes-myg og kan hos mennesker forårsage en normalt mild sygdom, som kaldes Zikafeber, og som siden 1950'erne tidvis er forekommet inden for et smalt bælte langs ækvator fra Afrika til Asien. I 2014 spredte virusen sig over Stillehavet til Fransk Polynesien og videre til Påskeøen, og i løbet af 2015 nåede den også til Sydamerika, Centralamerika og Caribien. Udbruddet klassificeredes som en pandemi.[1][2]
Sygdommen opleves som en mild form af denguefeber,[3] og kan netop nu ikke behandles eller forebygges med lægemidler eller vaccine.[4] Sygdommen er beslægtet med gul feber og vestnil-feber (engelsk: West Nile-fever), som også forårsages af insekttransporteret flavivirus.[3]
I januar 2016 offentliggjordes rapporter om eventuelle forbindelser mellem zikavirusinfektion og alvorlige komplikationer, som kan ramme fostre. Virusen menes at kunne forårsage mikrocefali hos fostre, som via mødre, er blevet smittet under graviditeten, men forbindelsen og den eventuelle risiko er ikke helt klarlagt, og undersøgelser var fortsat i gang i midten af januar 2016.[5][6] Den 15. januar 2016 udsendte USA's folkesundhedsmyndighed CDC anbefalinger til rejsende vedrørende de berørte lande i Sydamerika, som indebar, at gravide kvinder burde overveje at udskyde rejsen.[7] Hen mod slutningen af januar 2016 blev meddelt om de første tilfælde af inficerede individer i Europa, som havde besøgt Latinamerika.
Zikavirus (ZIKV) er en virus i familien flavivirus. Virusen overføres af Aedes-myg og kan hos mennesker forårsage en normalt mild sygdom, som kaldes Zikafeber, og som siden 1950'erne tidvis er forekommet inden for et smalt bælte langs ækvator fra Afrika til Asien. I 2014 spredte virusen sig over Stillehavet til Fransk Polynesien og videre til Påskeøen, og i løbet af 2015 nåede den også til Sydamerika, Centralamerika og Caribien. Udbruddet klassificeredes som en pandemi.
Sygdommen opleves som en mild form af denguefeber, og kan netop nu ikke behandles eller forebygges med lægemidler eller vaccine. Sygdommen er beslægtet med gul feber og vestnil-feber (engelsk: West Nile-fever), som også forårsages af insekttransporteret flavivirus.
I januar 2016 offentliggjordes rapporter om eventuelle forbindelser mellem zikavirusinfektion og alvorlige komplikationer, som kan ramme fostre. Virusen menes at kunne forårsage mikrocefali hos fostre, som via mødre, er blevet smittet under graviditeten, men forbindelsen og den eventuelle risiko er ikke helt klarlagt, og undersøgelser var fortsat i gang i midten af januar 2016. Den 15. januar 2016 udsendte USA's folkesundhedsmyndighed CDC anbefalinger til rejsende vedrørende de berørte lande i Sydamerika, som indebar, at gravide kvinder burde overveje at udskyde rejsen. Hen mod slutningen af januar 2016 blev meddelt om de første tilfælde af inficerede individer i Europa, som havde besøgt Latinamerika.
Das Zika-Virus () (ZIKV) gehört zur Gattung Flavivirus der Familie Flaviviridae. Es wurde erstmals 1947 aus einem gezielt zum Auffinden des Gelbfiebervirus gefangen gehaltenen Rhesusaffen (einem sogenannten Markertier oder sentinel monkey) einer Forschungsstation im Zika Forest in Entebbe, Uganda, isoliert und nach dem Ort benannt.[3][4] Das Virus kommt endemisch in Afrika und Südostasien vor, die verschiedenen Virusstämme werden deshalb in eine afrikanische und eine asiatische Gruppe unterteilt.[5][6] Da Infektionen mit dem Zika-Virus („Zikafieber“) und neu beobachtete Schädigungen von Föten bei Schwangeren seit 2015 erstmals und zugleich gehäuft in Lateinamerika beobachtet werden, erklärte die Weltgesundheitsorganisation (WHO) am 1. Februar 2016 den „Öffentlichen Gesundheitsnotstand internationalen Ausmaßes“.[7]
Der prinzipielle Aufbau und die möglichen Virusproteine des Zika-Virus unterscheiden sich nicht wesentlich von anderen Vertretern der Gattung Flavivirus. Am nächsten ist das Zika-Virus mit dem (noch nicht offiziell bestätigten) ‚Spondweni-Virus‘ verwandt, mit dem es eine Klade innerhalb der Moskito-übertragenen Flaviviren bildet.[8][9][10] Das Virusgenom besteht aus einer 10.794 Basen langen Einzelstrang-RNA positiver Polarität, die einen etwa 10.300 Basen langen offenen Leserahmen enthält, der für die Virusproteine kodiert und am 5′- und am 3′-Ende von nicht-kodierenden Sequenzen flankiert ist. Das 5′-Ende besitzt eine Cap-Struktur und das 3′-Ende keinen Poly-A-Schwanz, sondern bildet eine schleifenförmige Sekundärstruktur aus. Diese Schleife wird von der zellulären RNase XRN1 erkannt und vom Genom abgespalten.[11] Das dabei freigesetzte 3'-Ende (subgenomic flavivirus RNA, sfRNA) ist als Virulenzfaktor an der Pathogenität der Flaviviren beteiligt, vermutlich durch die Hemmung des zellulären Resistenzfaktors RIG-I.[11] Die erste vollständige Sequenz des Virusgenoms eines Isolates wurde im Jahr 2006 publiziert.[12] Aus dem RNA-Genom wird im Zuge der Proteinbiosynthese ein Polyprotein von etwa 3417 bis 3423 Aminosäuren gebildet, das anschließend durch virale und zelluläre Proteasen in die einzelnen viralen Proteine gespalten wird.
Das Zika-Virus (und einige Verwandte) kann den Abbau der RNA verhindern, indem es dieser auf spezielle Weise „verknotet“, wodurch eine Exoribonuklease-resistente RNA (en. exoribonuclease-resistant RNA, xrRNA) entsteht.[13][14]
Nahe Verwandte des Zika-Virus sind die Flaviviren Dengue-Virus und West-Nil-Virus, die ebenfalls von Aedes-Mücken übertragen werden und als emerging pathogens eingestuft wurden, beim Menschen jedoch weitaus schwerere Erkrankungen hervorrufen können. Ein weiterer Verwandter ist das Gelbfieber-Virus, das durch die Gelbfiebermücke (Stegomyia aegypti, früher Aedes aegypti) übertragen wird. Auch diese Flaviviren bilden xrRNA.[15]
Nach vollständiger Sequenzierung des Virusgenoms eines Isolats aus Französisch-Polynesien aus dem Jahr 2013 wurden folgende mögliche Virusproteine aus der Nukleotidsequenz abgeleitet:[16]
Das Virion besitzt einen Durchmesser von circa 50 Nanometer und eine ikosaedrische Form der Virushülle und des Kapsids, mit je drei Homodimeren des E-Proteins (Rezeptor, Transmembranprotein und fusogenes Protein) auf jeder Fläche der Außenseite.[11] Das E-Protein besitzt eine Serinprotease-Aktivität. Teilweise verdeckt vom E-Protein liegt das andere Transmembranprotein M in der Virushülle.[11] Unter der Virushülle liegt das Kapsid aus dem Kapsidprotein C, das die virale RNA ummantelt.[11]
Nach der Bindung des viralen Rezeptors E-Protein an ein bisher unbekanntes zelluläres Oberflächenprotein erfolgt die Einstülpung des Virions per Endozytose in ein Endosom. Im Endosom sorgt das E-Protein als fusogenes Protein für die Verschmelzung von Virushülle und Endosomenmembran, wodurch das Kapsid ins Zytosol freigesetzt wird. Dort erfolgt die Entpackung des Kapsids und des RNA-Genoms. Die Replikation des Genoms erfolgt im Zytosol durch die RNA-Polymerase NS5, bei der doppelsträngige virale RNA gebildet wird. Da das RNA-Genom eine positive Polarität aufweist, wird aus den kopierten RNA-Genomen und gleichzeitig aus dem entpackten RNA-Strang per Proteinbiosynthese direkt (ohne Replikation) das virale Polyprotein erzeugt, welches anschließend durch Proteolyse in die einzelnen viralen Proteine gespalten wird. Der Zusammenbau eines neugebildeten Virions findet im endoplasmatischen Retikulum statt. Nach einem Transfer in den Golgi-Apparat erfolgt die Reifung des Virions durch eine Proteolyse des Proteins prM. Zika-Viren sind nichtlytische Viren und verlassen die Wirtszelle durch Exozytose.
Der Tropismus des Zika-Virus umfasst unter anderem Zellen der Haut und neuronale Stammzellen.[17][18] Aufgrund der Infektion neuronaler embryonaler Stammzellen entstehen vermutlich die Schäden bei der neuronalen Entwicklung von Embryonen.[18] Das Zika-Virus führt in Mäuse-Föten zu neuronalen Infektionen und in Folge zu neuronalen Defekten.[19][20]
Das Zika-Virus ist beim Menschen Verursacher des Zikafiebers.
Erstmals im Menschen nachgewiesen wurde das Zika-Virus im Jahr 1952 in Uganda und Tansania.[21][22] In den folgenden Jahrzehnten breitete sich das Virus in Afrika und Asien weiträumig aus.[5][23] Bis 2007 waren jedoch weniger als 15 Infektionen beim Menschen bekannt, die alle in Afrika oder Südostasien nachgewiesen wurden.[24]
Der erste große Ausbruch beim Menschen – auf den Yap-Inseln Mikronesiens im Jahr 2007 – hat dazu geführt, dass das Zika-Virus als sogenanntes Emergent Virus eingestuft wurde, das heißt als Krankheitserreger, der sich möglicherweise noch weiter über die Welt ausbreiten könne.[25] Nachfolgend kam es 2013-2014 zu einer Epidemie in Französisch-Polynesien, bei der erstmals ein vermehrtes Vorkommen des Guillain-Barré-Syndroms (GBS) beobachtet wurde, sowie eine Übertragung auf das ungeborene Kind belegt werden konnte.
Ab 2015 wurden dann zunehmend mehr Fälle von Zika-Fieber in Süd-, Mittelamerika und der Karibik beobachtet, die alle durch die asiatische Linie des Zikavirus ausgelöst wurden. Phylogenetisch wird vermutet, dass das Virus bereits 2013 in Amerika angekommen ist. Ab 2015 wurden wieder Ausbrüche zurück in Afrika (Kap Verde, Guinea-Bissau und Angola) beschrieben, die ebenfalls durch die asiatische Linie ausgelöst wurden.
Der Ausbruch in Lateinamerika 2015 wird als „perfekter Sturm“ beschrieben, weil eine neue Linie, die amerikanische Subklade, auf eine komplett empfängliche (suszeptible) Bevölkerung traf und 60 % der exponierten Bevölkerung infizierte.[26]
Erste endemische Zika-Virus-Übertragungen durch Stechmücken in Europa wurden im Herbst 2019 aus Südfrankreich berichtet.[27]
Das natürliche Vorkommen der Zika-Viren liegt im tropischen Afrika; Infektionsfälle gibt es aber in der gesamten tropischen Klimazone. Reisende haben das Virus gelegentlich auch in andere Klimazonen, beispielsweise nach Europa, verschleppt.
Die Biologie und die Übertragungswege des Zika-Virus waren bis Ende 2015 wenig erforscht.[24] Bekannt war jedoch, dass die Viren wohl vor allem durch Stechmücken der Art Aedes aegypti[28] sowie durch andere Arten der Gattung Aedes, darunter möglicherweise auch die Asiatische Tigermücke (Aedes albopictus)[29][30][31] übertragen werden. In mehreren Laborexperimenten wurde seit 2016 nachgewiesen, dass auch Aedes albopictus – jedoch erst bei Temperaturen über 27 Grad – die Viren übertragen kann.[32] Ob und in welchem Umfang Stechmücken der Art Culex Zika-Viren übertragen, wird aktuell (2019) untersucht. Am besten erforscht ist die Vektorkompetenz von Cx. quinquefasciatus. Noch nie wurde ZIKV-RNA in Stechmücken dieser Art im Rahmen einer Felduntersuchung nachgewiesen. Die Fähigkeit zur Übertragung im Labor wird durch eine überwiegende Anzahl von Studien widerlegt[33]. Es gibt auch Ergebnisse von Experimenten, die dafür sprechen[34][35][36]. Dass in Mitteleuropa endemische Culex-Arten an der Übertragung von Zika-Viren beteiligt sind, kann aktuell jedoch recht sicher ausgeschlossen werden. Am umfassendsten konnte das Fehlen einer relevanten experimentellen Vektorkompetenz für Zika für die drei in Mitteleuropa häufigsten Arten Cx. p. pipiens, Cx. p. molestus und Cx. torrentium gezeigt werden.[37][32]
Auch eine Übertragung über sexuellen Kontakt zwischen Menschen ist möglich, wenngleich bislang lediglich Einzelfälle bekannt sind. Bereits aus dem Jahr 2009 ist ein Fall dokumentiert, in dem ein Biologe der Colorado State University seine Frau mit dem Virus angesteckt haben soll.[38][39] Anfang Februar 2016 gab es erneut Berichte, wonach in Dallas eine sexuelle Übertragung zwischen Menschen nachgewiesen wurde.[40][41] Im Oktober 2016 wurde in einer Fachzeitschrift publiziert, dass das vollständige Virusgenom aus Samenflüssigkeit isoliert wurde.[42] Einer 2019 veröffentlichten Studie zufolge waren die Viren in Spermaproben bei 8 von 97 untersuchten Patienten mit anfangs hoher Viruslast noch bis zu 38 Tage nach der ersten Diagnose nachweisbar.[43]
Auch im Urin und Speichel von symptomatischen Patienten wurde genetisches Material von Zikaviren nachgewiesen. Inwiefern die Zikaviren auch durch Urin und Speichel übertragen werden können, ist noch nicht bekannt.
Die bekannt gewordenen Infektionsverläufe waren zunächst relativ milde, und nur eine von fünf infizierten Personen entwickelt Symptome: insbesondere Hautausschlag und Fieber („Zikafieber“), Gelenkschmerzen, Konjunktivitis sowie seltener Muskel- und Kopfschmerzen und Erbrechen. Die Symptome klingen in der Regel bereits nach wenigen Tagen, spätestens nach einer Woche, ab.[44] Es gibt bislang keine gesicherten Todesfälle. Allerdings gibt es Verdachtsfälle in Kolumbien, bei denen bei drei Patienten nach einer Zika-Infektion das Guillain-Barré-Syndrom aufgetreten sei und dies zum Tod der Erkrankten geführt hätte.[45] In einer Studie mit Patienten aus Französisch-Polynesien wurde eine Häufung von Guillain-Barré-Syndromen bei serologischem Nachweis einer früheren oder kürzlichen Infektion mit dem Zika-Virus festgestellt. In den untersuchten Serumproben von 42 Patienten mit einem Guillain-Barré-Syndrom konnten spezifische Antikörper gegen das Zika-Virus nachgewiesen werden, bei einigen Patienten zusätzlich Antikörper gegen weitere tropische Arboviren. Keiner dieser Patienten mit GBS ist an diesem verstorben.[46]
Aufgrund der epidemiologischen Daten gab es seit Ende 2015 den dringenden Verdacht auf einen Zusammenhang zwischen Infektionen mit dem Zika-Virus bei Schwangeren während des ersten Drittels der Schwangerschaft[47] und Mikrozephalien bei Föten[48][49] beziehungsweise bei Neugeborenen.[50][51]
Anfang 2016 wurde der erste sichere virologische Nachweis für eine Infektion des fötalen Gehirns mit dem Zika-Virus bei bestehender Mikrozephalie erbracht:[52]
Eine Frau, die sich in Natal (Brasilien) aufhielt, wurde dort schwanger und erkrankte in der 13. Schwangerschaftswoche (SSW) mit allen klinischen Zeichen des Zika-Fiebers. Die Ultraschall-Untersuchung zeigte beim Fötus in der 14. und 20. SSW keine morphologischen Auffälligkeiten. Zurück in Ljubljana fanden sich in der 29. SSW erste Anzeichen einer Mikrozephalie beim Fötus, in der 32. SSW schließlich eine schwergradige Mikrozephalie (Hirngröße unterhalb der 2. Perzentile), intrazerebrale Verkalkungen, eine Vergrößerung der Hirnventrikel und eine schwere generelle Wachstumsstörung (Gewicht des Fötus unterhalb der 3. Perzentile). Auch in der Plazenta fielen Verkalkungen auf. Nach dem Schwangerschaftsabbruch fand man im Hirngewebe des Fötus virale RNA des Zika-Virus. Dessen gesamtes Genom wurde sequenziert. Das Virusisolat stimmte auf RNA-Ebene zu 99,7 Prozent mit einem Isolat aus Französisch-Polynesien überein, das im Jahr 2013 sequenziert wurde. In anderen Organen (Plazenta, Herz, Lunge, Haut, Thymus, Milz, Leber und Nieren) wurde kein Zika-Virus nachgewiesen. Bei einer elektronenmikroskopischen Untersuchung des Hirngewebes zeigten sich Flavivirus-ähnliche Partikel.
Die Schädigung des fötalen Gehirns beginnt ab der 20. SSW mit einer Störung der Hirnrinden-Reifung und der Verzögerung der gyralen Faltung. Ungewöhnlich ist auch der Umstand, dass das Virus 21 Wochen beim Fötus persistierte und die nach der mütterlichen Infektion gebildeten IgG-Antikörper nach Ausheilung der akuten Infektion nicht in der Lage waren, die Infektion beim Fötus ebenfalls zu beenden.
Die Ergebnisse untermauern den vorherigen Nachweis von Zika-Virus-RNA im Fruchtwasser bei zwei mikrozephalen Föten in Brasilien in der 29. bzw. 30. SSW.[53] Auch bei diesen zwei Fällen entsprach die virale RNA den asiatischen Zika-Virus-Isolaten. Die US-Gesundheitsbehörde CDC kam im April 2016 nach Auswertung diverser Studien zu dem Schluss, dass Zika-Viren eindeutig die Schädelfehlbildung Mikrozephalie bei Föten verursachen.[54][55][56][57] Im Dezember 2016 wurde in einer ersten, größeren Verlaufstudie an Schwangeren Belege dafür gefunden, dass infolge einer Zika-Virus-Infektion das Risiko für Fehlbildungen und andere Schädigungen im Vergleich mit einer Kontrollgruppe sehr erheblich erhöht wird.[58]
Nach bisherigen Erkenntnissen verläuft das Zika-Fieber für Schwangere selbst nicht schwerer, länger oder mit einer erhöhten Häufigkeit von Komplikationen als bei Nicht-Schwangeren.
Frühere Dengue-Infektionen schützen vor Zika-assoziierten Schäden des Fötus.[59]
Die Diagnose von Zika-Virus-Infektionen aufgrund der klinischen Symptomatik ist schwierig, da es andere in den entsprechenden Regionen endemische Arboviren gibt, die sehr ähnliche unspezifische klinische Symptome hervorrufen.[60] In akut erkrankten Patienten konnte das Zika-Virus per RT-PCR nachgewiesen werden. Die virämische Phase, in der dieser Nachweis aus dem Blut gelingt, kann mit nur wenigen Tagen allerdings kurz sein.[61] Aus diesem Grund empfiehlt die Weltgesundheitsorganisation die Durchführung von RT-PCR-Tests mit Serumproben innerhalb von ein bis drei Tagen nach Auftreten der ersten Symptome, und zusätzlich innerhalb von drei bis fünf Tagen nach Auftreten der ersten Symptome in Speichel- oder Urinproben.[62] Serologische Tests zum Nachweis von spezifischen IgM- und IgG-Antikörpern wurden ebenfalls verwendet, obwohl ihr Aussagewert bezüglich Spezifität und Sensitivität eingeschränkt ist. IgM kann meist innerhalb von drei Tagen nach Krankheitsbeginn nachgewiesen werden.[63] Die Antikörpernachweise, insbesondere der IgM-Nachweis, können falsch positive Ergebnisse erbringen, da eine serologische Kreuzreaktivität mit engverwandten (d. h. aus derselben Gattung stammenden) Flaviviren wie dem Dengue-Virus und West-Nil-Virus oder nach Impfungen gegen Flaviviren (Gelbfiebervirus, FSME-Virus) möglich sind.[61][64][65]
Die Centers for Disease Control and Prevention (CDC) in den USA weisen darauf hin, dass die Differentialdiagnostik von Zika-Infektionen, basierend auf den typischen klinischen Zeichen, sehr breit gefächert ist und dass eine Vielzahl anderer viraler, aber auch bakterieller Infektionen abzugrenzen sind. Speziell in Lateinamerika ist das häufige Denguevirus auszuschließen, das bei akuter Infektion ähnliche Allgemeinsymptome und ein ähnliches Exanthem hervorrufen kann. Als virale Ursachen kommen noch weltweit verbreitete Infektionen mit Rötelnvirus, Masernvirus und Parvovirus B19 (alle mit einem möglichen Exanthem) sowie nicht-exanthematische Infektionen mit Enteroviren, Adenoviren und verschiedenen Alphaviren (z. B. Chikungunya-Virus, Mayaro-Virus, Ross-River-Virus, Barmah-Forest-Virus, O’nyong-nyong-Virus und Sindbis-Virus) differentialdiagnostisch in Frage. Als bakterielle Infektionskrankheiten sind eine Leptospirose, Rickettsiose und Infektionen mit A-Streptokokken abzugrenzen, die jedoch ähnlich wie eine in den Tropen stets auszuschließende Malaria zusätzlich charakteristische Symptome aufweisen.[66][67]
Nach Angaben der Gesellschaft für Virologie vom April 2016 ermöglicht ein neuer ZIKV NS1[68]-Antigen-basierter Test nunmehr nach wenigen Stunden die eindeutige Diagnose einer durchgemachten Zika-Virus-Infektion.[69] Forscher konnten nachweisen, dass dieser neue Test zum Nachweis von ZIKV-Antikörpern auch dann hochspezifisch ist, wenn bei dem zu Untersuchenden eine früher erfolgte und laborgesicherte FSME-Infektion oder -Impfung vorliegt.[70]
Es existieren bislang weder eine Impfung noch Medikamente zur Krankheitsprävention. Bis möglicherweise ein Impfstoff verfügbar ist, könnten nach Einschätzung vieler Wissenschaftler Jahre vergehen.[71] Erste potentielle Impfstoffe werden seit Juli 2016 in Phase-I-Studien getestet, erste Ergebnisse werden jedoch nicht vor Ende 2017 vorliegen.[72] Als Schutzmaßnahmen gelten daher lediglich ein allgemeiner Schutz gegen Moskitostiche oder gar das Meiden entsprechender Klimazonen.[73] Aufgrund von Berichten über eine sexuelle Übertragung der Viren gelten die allgemeinen Schutzmaßnahmen vor sexuell übertragbaren Krankheiten, wie insbesondere der Gebrauch von Kondomen.
Es ist bislang nicht bekannt, ob eine einmal durchgemachte Infektion zumindest zu einer zeitlich begrenzten Immunität führt.[74]
In Deutschland ist der direkte oder indirekte Nachweis des Zika-Virus namentlich meldepflichtig nach des Infektionsschutzgesetzes (IfSG), soweit der Nachweis auf eine akute Infektion hinweist. Meldepflichtig sind die Leitungen der Labore usw. ( IfSG).
In Österreich sind Zika-Virus-Infektionen anzeigepflichtige Krankheiten gemäß Abs. 1 Nr. 2 Epidemiegesetz 1950. Meldepflichtig sind Erkrankungs- und Todesfälle. Zur Anzeige verpflichtet sind unter anderen Ärzte und Labore ( Epidemiegesetz).
In der Schweiz ist der positive laboranalytische Befund zum Zika-Virus meldepflichtig durch das untersuchende Labor und zwar nach dem Epidemiengesetz (EpG) in Verbindung mit der Epidemienverordnung und der Verordnung des EDI über die Meldung von Beobachtungen übertragbarer Krankheiten des Menschen. Zudem ist Zika-Fieber eine meldepflichtige Krankheit nach den genannten Normen und der genannten Verordnung des EDI.
Das Zika-Virus () (ZIKV) gehört zur Gattung Flavivirus der Familie Flaviviridae. Es wurde erstmals 1947 aus einem gezielt zum Auffinden des Gelbfiebervirus gefangen gehaltenen Rhesusaffen (einem sogenannten Markertier oder sentinel monkey) einer Forschungsstation im Zika Forest in Entebbe, Uganda, isoliert und nach dem Ort benannt. Das Virus kommt endemisch in Afrika und Südostasien vor, die verschiedenen Virusstämme werden deshalb in eine afrikanische und eine asiatische Gruppe unterteilt. Da Infektionen mit dem Zika-Virus („Zikafieber“) und neu beobachtete Schädigungen von Föten bei Schwangeren seit 2015 erstmals und zugleich gehäuft in Lateinamerika beobachtet werden, erklärte die Weltgesundheitsorganisation (WHO) am 1. Februar 2016 den „Öffentlichen Gesundheitsnotstand internationalen Ausmaßes“.
El Virus Zika (ZIKV) a l'è on virus descovert per la prima volta in del 1946 in Uganda, e in di ultim agn el s'è spantegaa in tutt el mond.
Principalment, el Zika 'l se trasmett cont i zanzar, anca se l'è possibil la trasmission cont el sperma.
In di omm, el virus el fa vegnì ona fever leggera, infiamazzion a la pell, infezion ai oeugg e mal al coo. Gh'è mia ona cura, ma basta el trattament sintomategh.
Inveci, in di fomme in contra, pò dà on fracch di problema al fioeu. In di facc, el Zika l'è fortement sospetaa de dà la microcefalia ai fioeu.
El Virus Zika (ZIKV) a l'è on virus descovert per la prima volta in del 1946 in Uganda, e in di ultim agn el s'è spantegaa in tutt el mond.
Lo virus de Zika (ZIKV) es un virus del genre Flavivirus, de la familha Flaviviridae, grop IV de l'òrdre sens classificar.[1] A d'interès en medecina per produire la fèbre de Zika
La febre Zika es una malautiá relativament novèla, un membre de la familha Flaviviridae. Lo virus foguèt identificat pel primièr còp en 1947 dins los boscs de Zika, en Oganda e foguèt demostrat coma essent un vius per d'estudis serologics en 1952. Es conegut coma un virus comun de la classe Flaviviridae, subretot en l'Africa, mai en 2007 faguèt epidèmia per l'ocean Pacific, toquèt de païses coma Malàisia i Micronesia, ont i a las Illas Yap.[2] Una epièmia de fèbre Zika foguèt confirmat en abril de 2015, en Brasil, dins la vila de Salvador de Bahia, provat amb la tècnica de RT-PCR.[3]
Lo virus a son terren en l'Africa, mas existís tanben en Malàisia e Micronesia, comprenent l'illa Yap, d'abril en julhet de 2007. E en 2015, Brasil informèt oficialament los sieus primièrs 16 cases de la malautiá.[4]Lo primièr cas conegut de fèbre de Zika foguèt documentat dins un monard Rhesus (Macaca mulata), trobat dins un arbre del Bòsc Zika a Oganda en 1947. Foguèron notificats unas epidèmias en Africa tropicala e dins unas zonas del sud-èst asiatic.[5] La primièr apidèmia importanta, amb 185 cases confirmats, foguèt reportat en 2007 dins las Illas Yap dels Estats Federats de Micronesia. Foguèt lo primièr còp de fèbre de Zika reportat fòra d'Africa e Asia. En 1978 se descriguèt una pichona epidèmia de fèbre aguda a Indonesia a causa de l'infeccion pel virus de Zika.
Dins los Estats Federats de Micronèsia (FSM), d'abril a julhet de 2007, un total de 108 cases foguèron confirmats per PCR o mejançant una serologia, los 72 cases addicionals foguèron considerats coma suspèctes. Los simptòmas mai comuns foguèron erupcion, fèbre, artralgias e conjuntivitis, se notèt pas de mòrts. Es lo moissal Aedes hensilli, espècia predominanta identificada a Yap, que benlèu foguèt lo vector màger de transmission. Alara que lo biais d'introduccion del virus dins l'illa de Yap es totjorn incertan, benlèu arribèt amb de moissals infectats o un uman portaire.[6]
Lo 27 de novembre de 2015, l'OMS lancèt una alèrta per la possibla relacion d'aquel virus amb la microcefalia.[7] L'OMS detalhèt que fins lo 30 de novembre de 2015, èran detectats 1.248 cases de microcefalia dins 14 estats de Brasil, que s'estan estudiats. Segon l'informacion, dins aquel país l'incidéncia de microcefalia en nenous a aumentat de 20 còps dempuèi l'an 2010. Ongan, s'enregistrèt 5 cases cada 100 mil naissenças. Cinc ans mai tard s'èran enregistrat gaireben 100.
Las autoritats sanitàrias brasilianas comencèron a suspectar en novembre de 2015 que la causa d'aquela multiplicacion dels cases de microcefalia es lo virus de Zika. Lo 17 de novembre, l'Institut Osvaldo Cruz detectèt lo virus zika en doas femnas emprenhadas de Paraíba, dels fetus se diagnostiquèt de microcefalia.
Lo 28 de novembre de 2015, l'Institut Evandro Chagas, de las malautiás tropicalas, tornèt detectar lo virus de Zika dins la sang d'un nenon de l'estat de Pará, qu'aviá la microcefalia e d'autras anomalias, e que moriguèt cinc minutas après la naissença. Dins aquela escasença lo Ministèri de Santat de Brasil establiguèt pel primièr còp la relacion entre lo virus e la microcefalia, alara foguèt lançada l'alèrta per l'agéncia de Vigilància en Santat Publica. Lo meteis jorn, l'entitat notifiquèt tres mòrts associadas a l'infeccion pel virus de Zika, dos adults e un recent nascut. Lo primièr cas fatal es un adult, masculin sens problèma neurologic amb diagnostic de Lupus eritematós, istòria d'usatge cronic de corticoíds, artritis reumatoíd e alcoolisme. Foguèt sospechada la dengue, mas, lo diagnostic final en laboratòri confirmèt l'infeccion pel virus Zika amb la tecniciana RTp-PCR. Foguèt detectat lo genòma del virus de Zika dins mòstra de sang, cervèl, fetge, mèlsa e en un ensems de viscèras (ren, palmon e còr). En mai foguèt realizat una sequenciacion parciala del virus identificant lo zika. Lo segond cas fatal es de sèxe femenin, 16 ans d'edat, de la municipalitat de Benevides, dins l'estat de Pará. Presentèt pas problèma neurològic, intrada al servici espitalièr amb sospècha de dengue. Comencèron los simptòmas lo 29 de setembre de 2015 (cefalèa, nausèas e petequias) e moriguèt a la fin del mes d'octòbre. Foguèt confirmat l'infeccion per virus Zika amb tecnica RTp-PCR. Lo tresen cas fatal es lo recent nascut que lo cas es decriu mai naut.
Fins al 1èr de decembre de 2015, 9 Estats membres de l'Organizacion Panamericana de la Santat avián confirmat circulacion autoctòna del virus de Zika: Brasil, Chile (dins l'Illa de Pascas), Colómbia, Lo Salvador, Guatemala, Mexic, Paraguai, Surinam e Veneçuèla.[8] La primièra circulacion autoctòna de virus de Zika (ZIKV) per las Americas foguèt confirmada en febrièr de 2014 dins Illa de Pascas, Chile. La preséncia del virus se detectèt fins a junh d'aquel meteis an dins aquel airal.
En mai de 2015, se confirmèron los primièrs cases de transmission autoctòna al Brasil. Fins al 1èr de decembre de 2015 un total de 18 Estats confirmèron circulacion autoctòna del virus: Region Nòrd (Amazonas, Pará, Rondônia, Roraima e Tocantins), Region Nòrd-èst (Alagoas, Badia,Ceará, Maranhão, Paraíba, Pernambuco, Piauí e Rio Grand don Nòrd), Region Sud-èst (Espírito Santo, Rio de Janeiro e São Paulo), Centri-Oèst (Mato Grosso) e Region Sud (Paraná) (1).
En octòbre de 2015 las autoritats de santat de Colómbia notifiquèron la deteccion del primièr cas autoctòn d'infeccion pel virus de Zika dins lo departament de Bolívar. Fins a decembre de 2015, 26 de las 36 entitats territorialas confirmèron la circulacion autoctòna del virus. Colómbia es al cap de lista dels infectats amb 578 diagnosticats sus 3170 reportats dins la region, Nòrd de Santander repòrta la mai granda quantitat d'infectats amb 350 e 500 cases estudiats en genièr de 2016. E mai, en novembre de 2015, Salvador, Guatemala, Mexic, Paraguai, Surinam e Veneçuèla confirmèron de cases de transmission autoctòna.[8]
Se transmet après la fissada d'un moissal del genre Aedes, coma lo Aedes Aegypti, que causa la dengue.
Lo virus Zika se pòt identificar amb una pròva de RT-PCR sus de pacients grevament malauts e per serologia mejançant la deteccion d'anticosses IgM especifics a comptar del cinquen jorn aprés a l'apareission de la fèbre. Es possible que se presenten de reaccions serologicas crosadas amb d'autres flavivirus estretament ligats, coma la dengue.[9][10]
Lo virus Zika es un flavivirus transmés per moissals estretament pròche al virus de la dengue. Lo virus foguèt isolat pel primièr còp en 1947 a comptar d'un monard dins lo bòsc Zika, Oganda.
Es establit que lo virus se transmet pels moissals, qu'alara lo contraròtle del vector es un element essencial per reduire l'incidéncia de la malautiá.
Lo virus de Zika (ZIKV) es un virus del genre Flavivirus, de la familha Flaviviridae, grop IV de l'òrdre sens classificar. A d'interès en medecina per produire la fèbre de Zika
Virusi Zika (ZIKV) është anëtar i familjes së virusëve Flaviviridae të gjinisë Flavivirus, dhe transmetohet nga mushkonjat Aedes, si A. aegypti.
Te njerëzit, virusi shkakton një sëmundje të lehtë të njohur si ethet Zika, Zika, ose sëmundja Zika, e cila që nga vitet 1950 ka paraqitej brenda një rrethi të ngushtë ekuatorial nga Afrika në Azi. Në vitin 2014, virusi u përhap në drejtim të lindjes në të gjithë Oqeanin Paqësor në Polinezinë franceze, pastaj tek Ishulli i Pashkëve, dhe në vitin 2015 në Meksikë, Amerikën Qendrore, Karaibe dhe Amerikën e Jugut, ku 'shpërthimi' Zika ka arritur në nivele epidemike.[1]
Virusi Zika (ZIKV) është anëtar i familjes së virusëve Flaviviridae të gjinisë Flavivirus, dhe transmetohet nga mushkonjat Aedes, si A. aegypti.
Te njerëzit, virusi shkakton një sëmundje të lehtë të njohur si ethet Zika, Zika, ose sëmundja Zika, e cila që nga vitet 1950 ka paraqitej brenda një rrethi të ngushtë ekuatorial nga Afrika në Azi. Në vitin 2014, virusi u përhap në drejtim të lindjes në të gjithë Oqeanin Paqësor në Polinezinë franceze, pastaj tek Ishulli i Pashkëve, dhe në vitin 2015 në Meksikë, Amerikën Qendrore, Karaibe dhe Amerikën e Jugut, ku 'shpërthimi' Zika ka arritur në nivele epidemike.
Viris Zika a (oubyen lafyèv Zika oubyen maladi Zika) se yon maladi ki vin souvan de moustik. Pi fò ka yo pa gen okenn sentòm, men yo kap sanble ak lafyèv deng.
Yo kwè ke maladi a kap ale de manman a pitit nan matris la,[1] epi koze mikrosefali—yon tèt piti piti—nan fetis la.
Nan 2015, Brezil te remake 2400 ka kote fetis la te gen mikrosefali ak 29 te mouri.
Zika virus (ZIKV) je član virusne porodice Flaviviridae i roda Flavivirus, prenešenog preko Aedes komaraca aktivnih danju, kao na primjer vrste A. aegypti.
Kod ljudi, virus uzrokuje bolest poznatu kao Zika groznica, Zika, ili bolest Zika, za koju se od 1950-tih zna da se pojavljuje u ograničenom ekvatorijalnom pojasu od Afrike do Azije. Godine 2014., virus se raširio istočno preko Pacifika do Francuske Polinezije, zatim na Uskršnje ostrvo i u 2015. u Meksiko, Centralnu Ameriku, Karibe, i Južnu Ameriku, gdje je izbijanje Zike dostiglo pandemičan nivo.[1]
Zika virus (ZIKV) is a member o the Flaviviridae virus faimily an the Flavivirus genus. It ais transmittit bi daytime-active Aedes mosquitoes, such as A. aegypti.
Zika virus es un taxon.
Zika virus (ZIKV) je član virusne porodice Flaviviridae i roda Flavivirus, prenešenog preko Aedes komaraca aktivnih danju, kao na primjer vrste A. aegypti.
Kod ljudi, virus uzrokuje bolest poznatu kao Zika groznica, Zika, ili bolest Zika, za koju se od 1950-tih zna da se pojavljuje u ograničenom ekvatorijalnom pojasu od Afrike do Azije. Godine 2014., virus se raširio istočno preko Pacifika do Francuske Polinezije, zatim na Uskršnje ostrvo i u 2015. u Meksiko, Centralnu Ameriku, Karibe, i Južnu Ameriku, gdje je izbijanje Zike dostiglo pandemičan nivo.
S Zika-Virus isch e Virus us dr Gattig Flavivirus (Familie Flaviviridae). S isch zum erschte Mol anne 1947 isoliert woren us eme Rhesusaff, wu in ere Forschigsstation im Zika Forest z Entebbe, Uganda zum Uffinde vum Geelfiebervirus ghalte woren isch, un isch au derno no däm Ort gnännt wore.[1][2] S Virus chunnt endemisch z Afrika un z Sidoschtasie vor. Wel s syt 2015 all mee Infektione mit em Zika-Virus z Latynamerika git un mit em Virus bstimmti Folgechrankete un -schäden in e Zämmehang brocht wäre, het d Wältgsundhaitsorganisazion (WHO) am 1. Februar 2016 dr „Effetli Gsundhaitsnotstand vu internationalem Uusmaß“ uusgruefe.[3]
S git dr Verdacht, ass es e Zämmehang git zwischen ere Zika-Infäkzion bi Schwangeren im erschte Drittel vu dr Schwangerschaft[4] un ere Mikrozefaly bi Feten[5] un bi Neigeborene.[6] Derzue vermuetet mer e Zämmehang zwisch em versterkten Ufdrätte vu dr neurologische Chranket Guillain-Barré-Syndrom z Brasilie un Infäkzione mit em Zika-Virus.[7]
S Zika-Virus isch e Virus us dr Gattig Flavivirus (Familie Flaviviridae). S isch zum erschte Mol anne 1947 isoliert woren us eme Rhesusaff, wu in ere Forschigsstation im Zika Forest z Entebbe, Uganda zum Uffinde vum Geelfiebervirus ghalte woren isch, un isch au derno no däm Ort gnännt wore. S Virus chunnt endemisch z Afrika un z Sidoschtasie vor. Wel s syt 2015 all mee Infektione mit em Zika-Virus z Latynamerika git un mit em Virus bstimmti Folgechrankete un -schäden in e Zämmehang brocht wäre, het d Wältgsundhaitsorganisazion (WHO) am 1. Februar 2016 dr „Effetli Gsundhaitsnotstand vu internationalem Uusmaß“ uusgruefe.
S git dr Verdacht, ass es e Zämmehang git zwischen ere Zika-Infäkzion bi Schwangeren im erschte Drittel vu dr Schwangerschaft un ere Mikrozefaly bi Feten un bi Neigeborene. Derzue vermuetet mer e Zämmehang zwisch em versterkten Ufdrätte vu dr neurologische Chranket Guillain-Barré-Syndrom z Brasilie un Infäkzione mit em Zika-Virus.
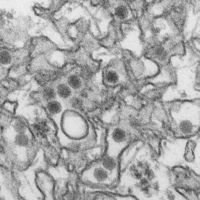
Elektronenmikroskopisk bil faan't Zika wiirus (40 nm, det san a jonk ponkter), apnimen faan't CDC
Süstemaatik Hoodkategorii: Wiiren Kategorii: nian Famile: Flaviviridae Skööl: Flavivirus Slach: Zika-wiirus Taksonomii Genoom: (+)ssRNA Baltimore-klas: Skööl 4 Sümetrii: ikosaedrisk Wiirusskan: as diar Wedenskapelk nööm Zika virus (ingelsk) Kurt nööm ZIKV FerwisangenAt Zika-wiirus as en wiirus uun det skööl Flavivirus faan't famile Flaviviridae. Hat as tuiarst bi aaben uun det wedenskapelk iinrachtang Zika Forest uun Uganda apdaaget.[1]
At Zika-wiirus woort faan magen auerdraanj an suragt för "Zika-fiiber". Bit daalang koon am diar ei föl jin maage. Det as för woksen minsken miast ei so slim, man för wüfen, diar en letj ütjdreeg. Det letj küd diar en skaas faan fu.
Magen, fööraal Aedes aegypti auerdreeg det wiirus.
Aanj 2015 as det wiirus fööraal uun Brasiilien ütjbreegen. Hoker diar hen raiset, skal ham fiks föörsä.
At Zika-wiirus as en wiirus uun det skööl Flavivirus faan't famile Flaviviridae. Hat as tuiarst bi aaben uun det wedenskapelk iinrachtang Zika Forest uun Uganda apdaaget.
At Zika-wiirus woort faan magen auerdraanj an suragt för "Zika-fiiber". Bit daalang koon am diar ei föl jin maage. Det as för woksen minsken miast ei so slim, man för wüfen, diar en letj ütjdreeg. Det letj küd diar en skaas faan fu.
Viris Zika a (oubyen lafyèv Zika oubyen maladi Zika) se yon maladi ki vin souvan de moustik. Pi fò ka yo pa gen okenn sentòm, men yo kap sanble ak lafyèv deng.
Yo kwè ke maladi a kap ale de manman a pitit nan matris la, epi koze mikrosefali—yon tèt piti piti—nan fetis la.
Nan 2015, Brezil te remake 2400 ka kote fetis la te gen mikrosefali ak 29 te mouri.
Zikas vėrosos (ZIKV) - vėrosos, sokelontis Zikas lėga. Vėrosa parneš kōsē. Vėrosos žėnuoms nug XX o. vėdorė, pėrma atsėrada Afrėkuo, bet dėdlē ėšplėta 2015 m. pabonguo, 2016 m. pradiuo Pėiū ė Centrėnės Amerėkas valstībies. Pėrma dėdliausē nokėntiejė Brazėlėjė. Zikas vėrosos dėdliausē pažēd nėštiuosės vaisiou, vakā gīmst so menkumo smegenuom ė mėnkuom makauliem. Pū ton vakā būn pruotėškā atsėlėkė.
Ο ιός Ζίκα (Zika, συντομογρ. ZIKV) είναι μέλος του γένους των φλαβοϊών (Flavivirus), που μεταδίδεται από τα ημερόβια κουνούπια του γένους αηδής (Aedes), όπως τον Aedes albopictus («κουνούπι-τίγρη»).
Στους ανθρώπους ο ιός αυτός προκαλεί μία ήπια ασθένεια γνωστή ως Ασθένεια του ιού Ζίκα, ασθένεια Ζίκα ή απλώς Ζίκα, η οποία από τη δεκαετία του 1950 είναι γνωστό ότι εμφανίζεται σε μία στενή ζώνη των τροπικών περιοχών στην Αφρική και την Ασία. Το 2014 ο ιός εξαπλώθηκε για πρώτη φορά προς τα ανατολικά, στη Γαλλική Πολυνησία, φθάνοντας μέχρι και το απομονωμένο Νησί του Πάσχα, και το 2015 στο Μεξικό, στην Καραϊβική, στην Κεντρική και Νότια Αμερική. Στην τελευταία, η αρρώστια που προκαλεί έφθασε στα επίπεδα πανδημίας[1]
Ο ιός Ζίκα, ως φλαβοϊός, σχετίζεται με τον ιό του δυτικού Νείλου, καθώς και με τους ιούς που προκαλούν τον δάγκειο και τον κίτρινο πυρετό και την ιαπωνική εγκεφαλίτιδα[2]. Η ασθένεια που προκαλεί είναι πράγματι παρόμοια με μία ήπια μορφή δάγγειου πυρετού[2] και δεν υπάρχει μέχρι σήμερα εμβόλιο για αυτή. Υπάρχει πιθανότατα σχέση ανάμεσα στον πυρετό Ζίκα και στην εμφάνιση μικροκεφαλίας σε νεογέννητα βρέφη από μετάδοση από τη μητέρα στο έμβρυο[3][4][5], καθώς και μια ισχυρότερη συσχέτιση με νευρολογικά σύνδρομα σε προσβαλλόμενους ενήλικες, όπως είναι το σύνδρομο Guillain-Barré[6].
Τον Ιανουάριο του 2016 τα Κέντρα για τον Έλεγχο και την Πρόληψη Ασθενειών (CDC) των ΗΠΑ εξέδωσαν μία ταξιδιωτική οδηγία για τις χώρες που έχει ανιχνευθεί ο ιός, με συστάσεις για αυξημένα μέτρα προστασίας και αποφυγή του ταξιδιού για έγκυες γυναίκες[7][8], ενώ άλλες χώρες ή υπηρεσίες υγείας εξέδωσαν και αυτές λίγο αργότερα παρόμοιες ταξιδιωτικές προειδοποιήσεις[9][10]. Η Κολομβία, η Δομινικανή Δημοκρατία, ο Ισημερινός, το Ελ Σαλβαδόρ και η Τζαμάικα συμβούλευσαν τις γυναίκες να αποφύγουν εγκυμοσύνες μέχρι την απόκτηση περισσότερων γνώσεων σχετικά με επιπτώσεις από την προσβολή από τον ιό στα έμβρυα[10][11].
Ο ιός Ζίκα, όπως και άλλοι ιοί της οικογενείας του, διαθέτει θύλακα και έχει σχήμα κανονικού εικοσαέδρου και μονό συνεχές γονιδίωμα από RNA. Συγγενεύει περισσότερο από όλους με τον ιό Spondweni, με τον οποίο έχει κοινή καταγωγή[12][13].
Ο ιός Ζίκα απομονώθηκε για πρώτη φορά τον Απρίλιο του 1947 από έναν πίθηκο μακάκο (rhesus macaque) που βρισκόταν μέσα σε κλουβί στο δάσος Ζίκα της Ουγκάντα, κοντά στη Λίμνη Βικτόρια, από επιστήμονες του Ερευνητικού Ινστιτούτου για τον Κίτρινο Πυρετό. Ακολούθησε μία δεύτερη απομόνωση, από το κουνούπι Aedes africanus, στην ίδια τοποθεσία τον Ιανουάριο του 1948.[14] Μόλις ο μακάκος εμφάνισε πυρετό, οι ερευνητές απομόνωσαν στο πλάσμα του έναν μεταδοτικό παράγοντα που περιγράφηκε για πρώτη φορά ως «ιός του Ζίκα» το 1952. Το 1968 απομονώθηκε για πρώτη φορά σε ανθρώπους, στη Νιγηρία[15]. Από το 1951 μέχρι το 1981 ενδείξεις για προσβολή του ανθρώπου από τον ιό αναφέρθηκαν και σε άλλες αφρικανικές χώρες, όπως οι Κεντροαφρικανική Δημοκρατία, Αίγυπτος, Γκαμπόν, Σιέρα Λεόνε, Τανζανία, αλλά και σε ασιατικές, όπως η Ινδία, η Ινδονησία, η Μαλαισία, οι Φιλιππίνες, η Ταϊλάνδη και το Βιετνάμ[15].
Διακρίνονται δύο καταγωγικοί τύποι (lineages) του ιού Ζίκα, η αφρικανική και η ασιατική[16]. Φυλογενετικές μελέτες υποδεικνύουν ότι ο ιός που εξαπλώθηκε στην Αμερική προήλθε μάλλον από τη Γαλλική Πολυνησία[16] Πλήρεις ακολουθίες του γονιδιώματος στελεχών του ιού Ζίκα έχουν δημοσιευθεί[17]. Πρόσφατα προκαταρκτικά ευρήματα αποκαλύπτουν μία πιθανή αλλαγή στη χρήση του κωδικονίου της μη δομικής πρωτεΐνης 1, που ίσως να αύξησε τον ρυθμό του πολλαπλασιασμού του μέσα στο ανθρώπινο σώμα[18].
Ο ιός Ζίκα μεταδίδεται από ημερόβια κουνούπια και έχει απομονωθεί από είδη του γένους αηδής (Aedes),πιθανον να μεταδίδεται και απο το
Aedes albopictus («κουνούπι-τίγρης»), όπως και από δενδρόβια κουνούπια όπως τα είδη Aedes africanus, A. apicoargenteus, A. furcifer, A. hensilli, A. luteocephalus και A. vitattus. Μελέτες δείχνουν ότι ο χρόνος εξωτερικής επωάσεως μέσα στα κουνούπια είναι περίπου 10 ημέρες[15]. Ο ιός μπορεί να μεταδοθεί από άνθρωπο σε άνθρωπο μέσω σεξουαλικών σχέσεων και δια του πλακούντα προσβάλλοντας έμβρυα.
Τα σπονδυλωτά ζώα που φιλοξενούν τον ιό είναι κυρίως οι πίθηκοι και οι άνθρωποι. Πριν από την τρέχουσα πανδημία, που άρχισε το 2007, ο ιός Ζίκα «σπανίως προκαλούσε μεταδοτικές προσβολές»[6].
Ο δυνητικός κίνδυνος από τον ιό Ζίκα προσδιορίζεται από την κατανομή των κουνουπιών-φορέων του. Η παγκόσμια κατανομή του συνηθέστερα ταυτιζόμενου φορέα του, του A. aegypti, επεκτείνεται διαρκώς εξαιτίας του παγκόσμιου εμπορίου και των ταξιδιών[19], και σήμερα είναι η ευρύτερη που έχει καταγραφεί ποτέ σε όλες τις ηπείρους[20]. Πληθυσμός κουνουπιών ικανών να μεταδώσουν τον ιό Ζίκα έχει βρεθεί στην Ουάσινγκτον με γενετικές ενδείξεις ότι έχουν επιβιώσει τουλάχιστον τους 4 τελευταίους χειμώνες εκεί[21]. Οι συγγραφείς της μελέτης συμπεραίνουν ότι τα κουνούπια προσαρμόζονται σε ψυχρότερες κλιματικές συνθήκες.
Πρόσφατες αναφορές στις ειδήσεις έχουν επιστήσει την προσοχή στη διάδοση του ιού Ζίκα στη Νότια Αμερική και την Καραϊβική[22]. Οι χώρες και τα εδάφη που έχουν ταυτοποιηθεί μέχρι στιγμής από τον Παναμερικανικό Οργανισμό Υγείας (PAHO) ως «τοπικής μεταδόσεως του ιού» είναι οι εξής: Μπαρμπάντος, Βολιβία, Βραζιλία, Κολομβία, Δομινικανή Δημοκρατία, Ισημερινός, Ελ Σαλβαδόρ, Γαλλική Γουιάνα, Γουαδαλούπη, Γουατεμάλα, Γουιάνα, Αϊτή, Ονδούρες, Μαρτινίκα, Μεξικό, Παναμάς, Παραγουάη, Πουέρτο Ρίκο, Σαιντ Μάρτιν, Σουρινάμ και Βενεζουέλα[23][24]
Το 2015, RNA του ιού ανιχνεύθηκε στο αμνιακό υγρό δύο εμβρύων, μία ένδειξη ότι είχε διαπεράσει τον φραγμό του πλακούντα και θα μπορούσε να μεταδοθεί από τη μητέρα στο έμβρυο[25].
Τον Δεκέμβριο του 2015 υπήρξαν υποψίες ότι η μετάδοση του ιού Ζίκα μέσα από τον πλακούντα στο έμβρυο μπορεί να προκαλεί μικροκεφαλία και εγκεφαλικές βλάβες[4][26]. τον ίδιο μήνα, το Ευρωπαϊκό Κέντρο για την Πρόληψη και τον Ελεγχο των Ασθενειών εξέδωσε μία περιεκτική ενημέρωση για τον πιθανό συσχετισμό του ιού με τη συγγενή μικροκεφαλία[27], ενώ το αμερικανικό CDC ανακοίνωσε: «`Εχουν υπάρξει αναφορές συγγενούς μικροκεφαλίας σε βρέφη μητέρων οι οποίες είχαν προσβληθεί από τον ιό Ζίκα όταν ήταν έγκυες. Οι προσβολές από τον ιό έχουν επιβεβαιωθεί σε πολλά βρέφη με μικροκεφαλία, αλλά δεν είναι γνωστό πόσες από τις περιπτώσεις μικροκεφαλίας συνδέονται με τη μόλυνση από τον ιό Ζίκα.»[28].
Στην επιδημία της Γαλλικής Πολυνησίας, 73 κρούσματα συνδρόμου Guillain-Barré και άλλες νευρολογικές παθήσεις καταγράφηκαν σε έναν πληθυσμό 270.000 και ίσως να αποτελούν επιπλοκές από τη μόλυνση με τον ιό Ζίκα[6].
Ο ιός Ζίκα (Zika, συντομογρ. ZIKV) είναι μέλος του γένους των φλαβοϊών (Flavivirus), που μεταδίδεται από τα ημερόβια κουνούπια του γένους αηδής (Aedes), όπως τον Aedes albopictus («κουνούπι-τίγρη»).
Στους ανθρώπους ο ιός αυτός προκαλεί μία ήπια ασθένεια γνωστή ως Ασθένεια του ιού Ζίκα, ασθένεια Ζίκα ή απλώς Ζίκα, η οποία από τη δεκαετία του 1950 είναι γνωστό ότι εμφανίζεται σε μία στενή ζώνη των τροπικών περιοχών στην Αφρική και την Ασία. Το 2014 ο ιός εξαπλώθηκε για πρώτη φορά προς τα ανατολικά, στη Γαλλική Πολυνησία, φθάνοντας μέχρι και το απομονωμένο Νησί του Πάσχα, και το 2015 στο Μεξικό, στην Καραϊβική, στην Κεντρική και Νότια Αμερική. Στην τελευταία, η αρρώστια που προκαλεί έφθασε στα επίπεδα πανδημίας
Зика — член на вирусното семејство Flaviviridae и родот Flavivirus, кој го пренесуваат комарците од родот Aedes, кои се активни дење, како што се A. aegypti и A. albopictus. Името му доаѓа од шумата Зика во Уганда, каде што вирусот за прв пат бил изолиран во 1947.[1]
Инфекцијата, позната како зика треска, често не предизвикува симптоми или само лесни симптоми, слични на блага форма на денга треска.[2]
Зика — член на вирусното семејство Flaviviridae и родот Flavivirus, кој го пренесуваат комарците од родот Aedes, кои се активни дење, како што се A. aegypti и A. albopictus. Името му доаѓа од шумата Зика во Уганда, каде што вирусот за прв пат бил изолиран во 1947.
Инфекцијата, позната како зика треска, често не предизвикува симптоми или само лесни симптоми, слични на блага форма на денга треска.
Зика вирус нь халдвартай шумуулаар дамжин хүнд халдварладаг вирус юм. Халдварын шинж тэмдэгт халууралт, үеэр өвдөх, арьсанд тууралт гарах, нүд улаах (нүдний салт бүрхүүлийн үрэвсэл) багтана.[1]
1947 онд анх илрүүлсэн Угандагийн Зика нэртэй ойн нэрээр нэрлэгдсэн вирус өвчний шалтгаан болдог. Зира вирус яаж тархдаг вэ?
Шумуул Зика вирусыг хүнээс хүнд дамжуулан халдварлуулдаг. Шумуул халдвартай хүний цусаар хооллох үед вирусыг авч, бусад хүнийг хазах үед вирусын халдварыг тараадаг.
Зика вирусын халдварыг тараадаг шумуул мөн dengue fever болон chikungunya вирусыг тараана. Энэ төрлийн вирусууд ихэвчлэн өдрийн цагаар хооллодог.
Ховор тохиолдолд эхээс урагт ихсээр дамжих болон төрөх үед цусаар дамжин халдварлана. Хөхний сүүгээр дамжин халдварладаггүй. Цус сэлбэх үед вирус дамжин халдварладаг баримт одоогоор бүртгэгдээгүй.
Зика вирусын хадвартай эрэгтэйгээс вирус бэлгийн хамтрагчид дамжин халдварлана. Вирус цусанд байхаас удаан хугацаагаар үрийн шингэнд хадгалагддаг, боловч хэр удаан хугацаагаар хадгалагддаг нь тогтоогдоогүй. Зика вирусын халдвартай эмэгтэйгээс бэлгийн хамтрагчид халдвар тархдгийг тогтоогоогүй.
2015 оноос өмнө Зика вирусын илрэл ихэвчлэн Африк, өмнөд ази, номхон далайн арлуудад бүртгэгдсэн. 2015 оны 5 сард вирус Вразилд анх илэрсэн.
Одоогийн байдлаар олон улсад тархаад байна. Үүнд:
АНУ-д өвчний тархалттай улсуудаар аяласан хүмүүсд вирусын халдвар илэрсэн. Гэвч шумуулаар дамжин хүнээс хүнд халдварласан тохиолдол бүртгэгдээгүй байна. Шинжээчид тун удахгүй халдварын тохиолдол илрэхийг сануулж байна.
Халдвар авсан 5 хүний зөвхөн 1 хүнд шинж тэмдэг илэрдэг. Энэ нь өөрөө мэдэхгүй Зика вирусын халдварыг авсан байх боломжтой гэсэн үг юм. Өвчний шинж тэмдгүүд шумууланд хазуулснаас хойш 2-7 хоног үргэлжлэнэ. Шинж тэмдгүүдэд:
Шинж тэмдэгүүд хөнгөн хэлбэрээр илэрч, цөөхөн хоног үргэлжлээд, ор мөхгүй алга болно.
Вирусын халдварын шинж тэмдэг илэрсэн болон вирусын тархалттай улсуудад аялсан бол эрүүл мэндийн байгууллагад цусны шинжилгээ өгөх боломжтой. Мөн шумуулаар халварладаг dengue and chikungunya зэрэг бусад вирусыг цусны шинжилгээгээр илрүүлэх боломтой.
Зика вирусын эмчлэх эмчилгээ байхгүй. Ханиадны вирустай адил өвчний шинж тэмдэг өөрөө арилна. Шинж тэмдэг бууруулах эмчилгээ хийж болно. Үүнд:
Бразилд Зика вирусын халдвартай эхээс хэвийнээс жижиг толгойн хэмжээтэй олон тооны хүүхэд төрсөн бөгөөд энэхүү ховор тохиолдох эмгэгийг микроцефали (Microcephaly) гэдэг. Энэхүү эмгэг хүүхдийн тархи эхийн хэвлий дотор болон төрсний дараа хэвийн бусаар өсөлт удааширсантай холбоотой.
Энэхүү төрөлхийн эмгэг ихэссэнтэй хобоотой Зика вирусын халдвартай эх болон микроцефалитай төрсөн хүүхдүүдийн хооронд хамаарал байна гэж үзэж байгаа юм. Энэ хамаарал одоогоор батлагдаагүй байгаа боловч шинжээчдийн ихэнх нь үүнийг үнэн гэдэгт итгэж байна. Вирус эхээс урагт хэрхэн дамжиж, яаж нөлөөлж байгаад хариулахаар нарийвчилсан судалгаа хийгдсээр байна.
Зика вирусын халдвар авсны дараа зарим хүмүүст Гуиллаин Барри хам шинж (Guillain-Barré syndrome) илэрдэг.
Зика варусын халдварын үеийн шинж тэмдэг илэрсэн бол эмчид хандаарай. Зика вирусын тархалттай улсад зорчисон бол эмчид заавал хэлээрэй. Эмч цусны шинжилгээ авах эсэхээ шийднэ.
Бэлгийн хамтрагч чинь Зика вирусын тархалттай улсад зорчисон болоод та өөрөө жирэмсэн эсвэл жирэмслэхээр төлөвлөж байгаа бол эмчид хандаарай.
Зика вирусын эсрэг урьчилан сэргийлэх тарилга одоогоор гараагүй. Зика вирусын халдвараас урьчилан сэргийлэх хамгийн сайн арга бол шумууланд хазуулахаас зайлсхийх юм. АНУ-ын Өвчний Хяналт, Урьдчилан Сэргийлэх Төв (US Centers for Disease Control and Prevention)-өөс вирусын тархалттай улсад зорчиж буй хүмүүст дараах зөвлөгөөг хүргэж байна:
Өвчний Хяналт, Урьдчилан Сэргийлэх Төв жирэмсэн эмэгтэйчүүдэд дараах зөвлөмжийг хүргүүлж байна:
Өвчний Хяналт, Урьдчилан Сэргийлэх Төвөөс жирэмслэхээр төлөвлөж байгаа эмэгтэйчүүдэд дараах зөвлөмжийг хүргүүлж байна:
Зика вирусын халдвар авсан бол бусдад тараахгүйн тулд шумууланд хазуулхаас залсхийх хэрэгтэй.
Зика вирус нь халдвартай шумуулаар дамжин хүнд халдварладаг вирус юм. Халдварын шинж тэмдэгт халууралт, үеэр өвдөх, арьсанд тууралт гарах, нүд улаах (нүдний салт бүрхүүлийн үрэвсэл) багтана.[1]
जिका विषाणु[1] फ्लाविविरिडए विषाणु परिवार से है। जो दिन के समय सक्रिय रहते हैं। इन्सानों में यह मामूली बीमारी के रूप में जाना जाता है, जिसे जिका बुखार, जिका या जिका बीमारी कहते हैं। 1947 [2] के दशक से इस बीमारी का पता चला। यह अफ्रीका से एशिया तक फैला हुआ है। यह 2014 में प्रशांत महासागर से फ्रेंच पॉलीनेशिया तक और उसके बाद 2015 में यह मेक्सिको, मध्य अमेरिका तक भी पहुँच गया।[3]
वर्ष 1947 में पीले बुखार का शोध कर रहे पूर्वी अफ्रीकी विषाणु अनुसंधान संस्थान के वैज्ञानिकों को जिका के जंगल में रीसस मकाक (एक प्रकार का लंगूर) को पिंजरे में रख कर अपना शोध कर रहे थे। उस बंदर को बुखार हो जाता है। 1952 में उसके संक्रामक घटक को जिका विषाणु नाम से बताया गया। यह इसके बाद नाइजीरिया में वर्ष 1954 में एक मानव से निकाला गया था।[4] इसके 2007 में खोज होने से पहले इससे संक्रमण के मामले अफ्रीका और दक्षिण पूर्व एशिया में बहुत कम थे।[5]
अप्रैल 2007 में इसका प्रभाव पहली बार अफ्रीका और एशिया के बाहर देखने को मिला। यप नामक एक द्वीप में लाल चकत्ते, नेत्रश्लेष्मलाशोथ, और जोड़ों के दर्द के रूप में इसका असर दिखा, जिसे सामान्यतः डेंगू या चिकनगुनिया समझा जा रहा था।[6] लेकिन जब बीमार लोगों के रक्त का परीक्षण किया गया तो उनके रक्त में जिका विषाणु का आरएनए पाया गया। अब तक इसके 49 मामलों की पुष्टि हो चुकी है और जबकि 59 मामले की पुष्टि नहीं हुई और किसी के भी मरने की या अस्पताल में रखने की जानकारी नहीं है।[7]
जिका बुखार, जिसे जिका वायरस रोग, के नाम से भी जाना जाता है, एक रुग्णता है जो जिका वायरस के कारण उत्पन्न होती है।[8] लक्षण डेंगू बुखार की ही तरह होते हैं।[8] अधिकांश मामलों (60 - 80 %) में कोई लक्षण नहीं दिखते।[9] यदि कुछ लक्षण दिखते हैं तो वे लक्षण अमूमन इस प्रकार के हो सकते हैं - बुखार, लाल आँखें, जोड़ों में दर्द, सिरदर्द लाल चकत्ते।[10][8] आम तौर पर लक्षण हल्के और 7 दिनों से भी कम रहते हैं।[11] वर्ष 2015 में इस आरंभिक संक्रमण से कोई मृत्यु नहीं हुई है।[9] संक्रमण को ग़ीयान-बारे संलक्षण Guillain–Barré सिंड्रोम से लिंक किया गया है।[9]
जिका बुखार मुख्यतया एडीज प्रकार के मच्छर के काटने से फैलता है।[11] शारीरिक संबंध बनाने और खून चढ़ाने से भी इसके फैलने की संभावना रहती है। [11] यह रोग गर्भवती माँ से गर्भस्थ शिशु में जा सकता है वर्टिकली ट्रांसमिटेड इंफेक्शन और शिशु के सिर के अपूर्ण विकास की वजह बन सकता है।[8][9] इस रोग की पहचान के लिए होने वाली जाँचों में रक्त, मूत्र या लार संबंधी परीक्षण शामिल हैं, जो बीमार व्यक्ति में इस वायरस के आरएनए के होने का पता लगाने के लिए की जाती हैं।[11][8]
रोकथाम में मच्छरों से बचाव शामिल है ताकि जिन क्षेत्रों में इस रोग के होने की संभावना है वहाँ मच्छरों द्वारा काटे जाने से बचा जा सके। [11] इनमें मच्छर भगाने वाले उपाय अमल में लाना, कपड़ों से शरीर का अधिकतम भाग ढँककर रखना, मच्छरदानी का प्रयोग, मच्छर पुनर्जनन रोकने हेतु ठहरे पानी को हटाना जैसी बातें शामिल होती हैं। [8] इसका कोई कारगर टीका नहीं है।[11] ब्राजील के स्वास्थ्य अधिकारियों ने 2015 में प्रकोप के कारण दंपत्तियों को गर्भधारण से बचने की सलाह दी थी, और गर्भवती महिलाओं को उन इलाकों में यात्रा करने से बचने की सलाह दी जहां प्रकोप फैला हो।[12][11] यद्यपि इसका कोई विशिष्ट उपचार नहीं है, तथापि पैरासिटामॉल (एसिटामिनोफेन) इन लक्षणों में मददगार हो सकती है।[11] अस्पताल में भर्ती होने की शायद ही कभी जरूरत पड़ती है।[9]
मुख्य तथ्य
जीका वायरस रोग मुख्य रूप से एडीज मच्छरों द्वारा प्रसारित एक वायरस के कारण होता है, जो दिन के दौरान काटता है।
लक्षण आम तौर पर हल्के होते हैं और इसमें बुखार, दाने, नेत्रश्लेष्मलाशोथ, मांसपेशियों और जोड़ों में दर्द, अस्वस्थता या सिरदर्द शामिल होते हैं। लक्षण आमतौर पर 2-7 दिनों तक रहते हैं। जीका वायरस संक्रमण वाले अधिकांश लोग लक्षण विकसित नहीं करते हैं।
गर्भावस्था के दौरान जीका वायरस का संक्रमण शिशुओं को जन्मजात जीका सिंड्रोम के रूप में जाने वाले माइक्रोसेफली और अन्य जन्मजात विकृतियों के साथ पैदा कर सकता है। जीका वायरस के साथ संक्रमण भी गर्भावस्था की अन्य जटिलताओं के साथ जुड़ा हुआ है, जिसमें प्रीटरम जन्म और गर्भपात शामिल हैं।
न्यूरोलॉजिकल जटिलताओं का एक बढ़ा जोखिम वयस्कों और बच्चों में जीका वायरस के संक्रमण से जुड़ा हुआ है, जिसमें गुइलेन-बैरे सिंड्रोम, न्यूरोपैथी और मायलाइटिस शामिल हैं।
जीका वायरस एक मच्छर जनित फ्लैविवायरस है जिसे पहली बार 1947 में बंदरों में पहचाना गया था। इसे बाद में 1952 में युगांडा और संयुक्त गणराज्य तंजानिया में मनुष्यों में पहचाना गया।
जीका वायरस की बीमारी का प्रकोप अफ्रीका, अमेरिका, एशिया और प्रशांत क्षेत्र में दर्ज किया गया है। 1960 से 1980 के दशक तक, अफ्रीका और एशिया में मानव संक्रमण के दुर्लभ छिटपुट मामले पाए गए, आमतौर पर हल्के बीमारी के साथ।
जीका वायरस की बीमारी का पहला रिकॉर्डेड प्रकोप 2007 में याप (फेडरेटेड स्टेट्स ऑफ माइक्रोनेशिया) के द्वीप से रिपोर्ट किया गया था। इसके बाद 2013 में फ्रेंच पोलिनेशिया और प्रशांत में अन्य देशों और क्षेत्रों में जीका वायरस के संक्रमण का बड़ा प्रकोप हुआ था। मार्च 2015 में, ब्राजील ने दाने की बीमारी के एक बड़े प्रकोप की सूचना दी, जिसे जल्द ही जीका वायरस संक्रमण के रूप में पहचाना गया, और जुलाई 2015 में, गुइलेन-बैरे सिंड्रोम से जुड़ा पाया गया।
अक्टूबर 2015 में, ब्राजील ने जीका वायरस के संक्रमण और माइक्रोसेफली के बीच सहयोग की सूचना दी। प्रकोप और संचरण के सबूत जल्द ही पूरे अमेरिका, अफ्रीका और दुनिया के अन्य क्षेत्रों में दिखाई दिए। आज तक, कुल 86 देशों और क्षेत्रों में मच्छरों से फैलने वाले जीका संक्रमण के प्रमाण मिले हैं।
संकेत और लक्षण
ज़ीका वायरस रोग के ऊष्मायन अवधि (लक्षणों के संपर्क से समय) 3-14 दिनों का अनुमान है। जीका वायरस से संक्रमित अधिकांश लोग लक्षण विकसित नहीं करते हैं। लक्षण आमतौर पर बुखार, दाने, नेत्रश्लेष्मलाशोथ, मांसपेशियों और जोड़ों के दर्द, अस्वस्थता और सिरदर्द सहित हल्के होते हैं, और आमतौर पर 2-7 दिनों तक रहते हैं।
जीका वायरस रोग की जटिलताऐं
गर्भावस्था के दौरान जीका वायरस संक्रमण विकासशील भ्रूण और नवजात शिशु में माइक्रोसेफली और अन्य जन्मजात असामान्यताओं का कारण है। गर्भावस्था में जीका संक्रमण के कारण गर्भावस्था में जटिलताएं होती हैं जैसे कि भ्रूण की हानि, स्टिलबर्थ और प्रीटरम जन्म।
जीका वायरस संक्रमण भी गुइलेन-बैर सिंड्रोम, न्यूरोपैथी और मायलाइटिस का एक ट्रिगर है, विशेष रूप से वयस्कों और बड़े बच्चों में।
गर्भावस्था के परिणामों पर जीका वायरस के संक्रमण, रोकथाम और नियंत्रण के लिए रणनीति और बच्चों और वयस्कों में अन्य न्यूरोलॉजिकल विकारों पर संक्रमण के प्रभाव की जांच करने के लिए अनुसंधान जारी है।
हस्तांतरण
जीका वायरस मुख्य रूप से एडीज जीन से संक्रमित मच्छर के काटने से फैलता है, मुख्यतः एडीज एजिप्टी, उष्णकटिबंधीय और उपोष्णकटिबंधीय क्षेत्रों में। एडीज मच्छर आम तौर पर दिन के दौरान काटते हैं, जो सुबह जल्दी और देर दोपहर / शाम को बढ़ते हैं। यह वही मच्छर है जो डेंगू, चिकनगुनिया और पीले बुखार को प्रसारित करता है।
जीका वायरस भी गर्भावस्था के दौरान मां से भ्रूण में, यौन संपर्क, रक्त और रक्त उत्पादों के आधान और अंग प्रत्यारोपण के माध्यम से प्रसारित होता है।
निदान
जीका वायरस के संक्रमण के साथ या जीका वायरस ट्रांसमिशन और / या एडीस मच्छर वैक्टर के साथ या उसके आसपास रहने वाले व्यक्तियों के लक्षणों के आधार पर संदेह हो सकता है। जीका वायरस संक्रमण का निदान केवल रक्त या शरीर के अन्य तरल पदार्थों जैसे कि मूत्र या वीर्य के प्रयोगशाला परीक्षणों द्वारा पुष्टि की जा सकती है।
इलाज
जीका वायरस के संक्रमण या इससे जुड़े रोगों के लिए कोई उपचार उपलब्ध नहीं है।
जीका वायरस के संक्रमण के लक्षण आमतौर पर हल्के होते हैं। बुखार, दाने या गठिया जैसे लक्षणों से पीड़ित लोगों को भरपूर आराम करना चाहिए, तरल पदार्थों का सेवन करना चाहिए और आम दवाओं के साथ दर्द और बुखार का इलाज करना चाहिए। यदि लक्षण बिगड़ते हैं, तो उन्हें चिकित्सा देखभाल और सलाह लेनी चाहिए।
जीका ट्रांसमिशन वाले क्षेत्रों में रहने वाली गर्भवती महिलाओं या जो जीका वायरस संक्रमण के लक्षण विकसित करते हैं, उन्हें प्रयोगशाला परीक्षण और अन्य नैदानिक देखभाल के लिए चिकित्सा ध्यान देना चाहिए।
निवारण
मच्छर
जीका वायरस के संक्रमण को रोकने के लिए दिन और शाम के समय मच्छरों के काटने से बचाव एक प्रमुख उपाय है। गर्भवती महिलाओं, प्रजनन आयु की महिलाओं और छोटे बच्चों के बीच मच्छरों के काटने की रोकथाम पर विशेष ध्यान दिया जाना चाहिए।
व्यक्तिगत सुरक्षा उपायों में कपड़े पहनना (अधिमानतः हल्के रंग का) शामिल है जो शरीर को जितना संभव हो उतना कवर करता है; विंडो स्क्रीन और बंद दरवाजे और खिड़कियों जैसे भौतिक बाधाओं का उपयोग करना; और उत्पाद लेबल के निर्देशों के अनुसार त्वचा या कपड़ों पर कीट विकर्षक लागू करना जिसमें DEET, IR3535 या आइकारिडिन शामिल हैं।
छोटे बच्चों और गर्भवती महिलाओं को मच्छरदानी के नीचे सोना चाहिए यदि दिन में या शाम को सोते हैं। यात्रियों और प्रभावित क्षेत्रों में रहने वाले लोगों को मच्छरों के काटने से खुद को बचाने के लिए ऊपर बताई गई वही बुनियादी सावधानी बरतनी चाहिए।
एडीज मच्छर घरों, स्कूलों और कार्य स्थलों के आसपास पानी के छोटे संग्रह में प्रजनन करते हैं। इन मच्छरों के प्रजनन स्थलों को खत्म करना महत्वपूर्ण है, जिनमें शामिल हैं: जल भंडारण कंटेनरों को ढंकना, फूलों के बर्तनों में खड़े पानी को निकालना, और कचरे को साफ करना और टायर का इस्तेमाल करना। मच्छरों के प्रजनन स्थलों को कम करने के लिए स्थानीय सरकार और सार्वजनिक स्वास्थ्य कार्यक्रमों का समर्थन करने के लिए सामुदायिक पहल आवश्यक है। मच्छरों की आबादी और बीमारी के प्रसार को कम करने के लिए स्वास्थ्य अधिकारी लार्विसाइड्स और कीटनाशकों के उपयोग की सलाह भी दे सकते हैं
जीका वायरस संक्रमण की रोकथाम या उपचार के लिए अभी तक कोई टीका उपलब्ध नहीं है। जीका वैक्सीन का विकास अनुसंधान का एक सक्रिय क्षेत्र बना हुआ है।
गर्भावस्था में संचरण
जीका वायरस को गर्भावस्था के दौरान मां से भ्रूण में स्थानांतरित किया जा सकता है, जिसके परिणामस्वरूप शिशु में माइक्रोसेफली (सामान्य सिर के आकार से छोटा) और अन्य जन्मजात विकृतियों को सामूहिक रूप से जन्मजात जीका सिंड्रोम के रूप में जाना जाता है।
माइक्रोसेफली अंतर्निहित असामान्य मस्तिष्क विकास या मस्तिष्क के ऊतकों के नुकसान के कारण होता है। मस्तिष्क क्षति की सीमा के अनुसार बच्चे के परिणाम भिन्न होते हैं।
जन्मजात जीका सिंड्रोम में अन्य विकृतियां शामिल हैं, जिसमें अंग के संकुचन, उच्च मांसपेशी टोन, आंखों की असामान्यताएं, और सुनवाई हानि शामिल है। गर्भावस्था में संक्रमण के बाद जन्मजात विकृतियों का जोखिम अज्ञात रहता है; गर्भावस्था के दौरान जीका वायरस से संक्रमित महिलाओं के लिए जन्मजात अनुमानित 5-15% शिशुओं में जीका से संबंधित जटिलताओं के प्रमाण हैं। जन्मजात विकृति लक्षण और स्पर्शोन्मुख संक्रमण दोनों के बाद होती है।
यौन संचरण
जीका वायरस संभोग के माध्यम से प्रेषित किया जा सकता है। जीका वायरस संक्रमण और प्रतिकूल गर्भावस्था और भ्रूण के परिणामों के बीच संबंध के कारण यह चिंता का विषय है।
जीका वायरस के सक्रिय संचरण वाले क्षेत्रों के लिए, जीका वायरस संक्रमण वाले सभी लोगों और उनके यौन साझेदारों (विशेष रूप से गर्भवती महिलाओं) को जीका वायरस के यौन संचरण के जोखिमों के बारे में जानकारी प्राप्त करनी चाहिए।
डब्ल्यूएचओ अनुशंसा करता है कि यौन सक्रिय पुरुषों और महिलाओं को सही ढंग से परामर्श दिया जाए और संभावित प्रतिकूल गर्भावस्था और भ्रूण के परिणामों को रोकने के लिए गर्भवती होने के बारे में एक सूचित विकल्प बनाने में सक्षम होने के लिए गर्भनिरोधक विधियों की एक पूरी श्रृंखला की पेशकश की जाए।
जिन महिलाओं ने असुरक्षित यौन संबंध बनाए हैं और जीका वायरस संक्रमण के बारे में चिंताओं के कारण गर्भवती होने की इच्छा नहीं रखती हैं, उन्हें आपातकालीन गर्भनिरोधक सेवाओं और परामर्श के लिए तैयार होना चाहिए। गर्भवती महिलाओं को कम से कम गर्भावस्था की पूरी अवधि के लिए सुरक्षित यौन क्रिया (कंडोम के सही और लगातार उपयोग सहित) या यौन गतिविधि से बचना चाहिए।
जीका वायरस के सक्रिय संचरण वाले क्षेत्रों के लिए, डब्ल्यूएचओ पुरुषों के लिए छह महीने की अवधि के लिए सुरक्षित यौन संबंध या संयम का अभ्यास करने की सलाह देता है और महिलाओं के लिए दो महीने तक जो अपने यौन साथियों के संक्रमण को रोकने के लिए सक्रिय जीका वायरस संचरण के क्षेत्रों से लौट रहे हैं। गर्भवती महिलाओं के यौन साथी, जीका वायरस के स्थानीय संचरण वाले क्षेत्रों में रहने वाले या वहां से लौटने के दौरान, गर्भावस्था के दौरान यौन क्रिया से सुरक्षित यौन संबंध बनाना चाहिए।
डब्ल्यूएचओ देशों को जीका स्ट्रैटजिक रिस्पांस फ्रेमवर्क में उल्लिखित कार्रवाई करके ज़ीका वायरस रोग को नियंत्रित करने के लिए समर्थन कर रहा है:
जीका वायरस संक्रमण और संबंधित जटिलताओं की रोकथाम, निगरानी और नियंत्रण में अनुसंधान को आगे बढ़ाना।
जीका वायरस संक्रमण और संबंधित जटिलताओं के लिए एकीकृत निगरानी प्रणाली का विकास, सुदृढ़ीकरण और कार्यान्वयन।
दुनिया भर में जीका वायरस संक्रमण के लिए परीक्षण करने के लिए प्रयोगशालाओं की क्षमता को मजबूत करना।
एडीज मच्छर आबादी को कम करने के उद्देश्य से वेक्टर नियंत्रण रणनीतियों को लागू करने और मॉनिटर करने के वैश्विक प्रयासों का समर्थन करना।
जीका संक्रमण की जटिलताओं से प्रभावित बच्चों और परिवारों की देखभाल और सहायता को मजबूत करना।
जिका विषाणु फ्लाविविरिडए विषाणु परिवार से है। जो दिन के समय सक्रिय रहते हैं। इन्सानों में यह मामूली बीमारी के रूप में जाना जाता है, जिसे जिका बुखार, जिका या जिका बीमारी कहते हैं। 1947 के दशक से इस बीमारी का पता चला। यह अफ्रीका से एशिया तक फैला हुआ है। यह 2014 में प्रशांत महासागर से फ्रेंच पॉलीनेशिया तक और उसके बाद 2015 में यह मेक्सिको, मध्य अमेरिका तक भी पहुँच गया।
জিকা ভাইৰাছ (Zika virus বা ZIKV) হৈছে ভাইৰাছ পৰিয়াল Flaviviridae আৰু গণ Flavivirus-ৰ অন্তৰ্গত এবিধ বীজাণু।[1] দিনত সক্ৰিয় থকা Aedes মহ যেনে A. aegyptiয়ে এই ভাইৰাছ বিয়পায়।[2] এই নামটো ১৯৪৭ চনত ভাইৰাছবিধ প্ৰথম ধৰা পৰা উগাণ্ডাৰ জিকা অৰণ্যৰ পৰা আহিছে।[3] জিকা ভাইৰাছৰ ডেংগি, পীত জ্বৰ, জাপানীজ এন্কেফেলাইটিছ আৰু ৱেষ্ট নাইল ভাইৰাছৰ লগত সম্পৰ্ক আছে।[4] ১৯৫০ চনমানৰে পৰা আফ্ৰিকা হৈ এছিয়া পৰ্যন্ত বিষুৱৰেখাৰ ওচৰে মাজৰে এই ৰোগ হোৱা বুলি জনা যায়। ২০০৭ চনৰ পৰা ২০১৬ লৈকে ভাইৰাছবিধ প্ৰশান্ত মহাসাগৰ পাৰ হৈ আমেৰিকালৈ বিয়পে আৰু ২০১৫-২০১৬ জিকা ভাইৰাছ মহামাৰীৰ সৃষ্টি কৰে।
জিকা জ্বৰ বা জিকা ভাইৰাছ ৰোগ বুলি কোৱা সংক্ৰমণে পাতলীয়া ডেংগি ৰোগৰ দৰে শূন্য বা নূন্যতম লক্ষণ উৎপন্ন কৰে।[5] বিশেষ চিকিৎসা নাই যদিও পাৰাচিটামল ঔষধ আৰু বিশ্ৰামে লক্ষণ পৰিশমৰ সহায় কৰে।[6] ২০১৬ চনলৈকে এই ৰোগ ঔষধ বা প্ৰতিষেধকেৰে প্ৰতিৰোধ কৰিব নোৱাৰি।[6] গৰ্ভৱতী মহিলাৰ পৰা সন্তানলৈ জিকা বিয়পিব পাৰে। ইয়াৰ ফলত মাইক্ৰ'চিফালি (সৰু আকাৰৰ মূৰ), মগজুৰ গুৰুতৰ ক্ষতি আৰু আন জন্মগত খুঁত হ'ব পাৰে।[7][8] প্ৰাপ্তবয়স্কত জিকা সংক্ৰমণে Guillain–Barré syndrome কৰিব পাৰিলেও সেয়া বিৰল।[9]২০১৬ চনৰ জানুৱাৰীত আমেৰিকা যুক্তৰাষ্ট্ৰৰ Centers for Disease Control and Prevention (CDC)-এ আক্ৰান্ত দেশসমূহত বিশেষ সাৱধানতাকে ধৰি কেতবোৰ ভ্ৰমণৰ নিৰ্দেশাৱলী প্ৰকাশ কৰে। গৰ্ভৱতী মহিলাৰ বাবে ভ্ৰমণ পিছুৱাই দিয়াৰ দৰে পৰামৰ্শও দিয়া হয়।[10][11] আন চৰকাৰ বা স্বাস্থ্য সন্থাই একে ধৰণৰ ভ্ৰমণ সতৰ্কবাণী দিয়ে,[12][13][14] যাৰ ভিতৰত কলম্বিয়া, ডমিনিকান ৰিপাব্লিক, পৰ্টে ৰিক', ইকুৱেডৰ, এল্ ছাল্ভাদৰ আৰু জামাইকাই অধিক তথ্য নজনালৈকে মহিলাক গৰ্ভধাৰণ পিছুৱানলৈ পৰামৰ্শ দিয়ে।[13][15] ২০১৭ চনৰ ১৫ মে'ত ভাৰত চৰকাৰৰ স্বাস্থ্য আৰু পৰিয়াল কল্যাণ মন্ত্ৰ্যালয়ে গুজৰাটৰ বাপুনগৰ অঞ্চলত তিনিজন জিকা ভাইৰাছ ৰোগী ধৰা পৰা বুলি নিশ্চিত কৰে।[16] জিকাক /ˈziːkə/ বা /ˈzɪkə/ বুলি উচ্চাৰণ কৰা হয়।[17][18]
জিকা ভাইৰাছ (Zika virus বা ZIKV) হৈছে ভাইৰাছ পৰিয়াল Flaviviridae আৰু গণ Flavivirus-ৰ অন্তৰ্গত এবিধ বীজাণু। দিনত সক্ৰিয় থকা Aedes মহ যেনে A. aegyptiয়ে এই ভাইৰাছ বিয়পায়। এই নামটো ১৯৪৭ চনত ভাইৰাছবিধ প্ৰথম ধৰা পৰা উগাণ্ডাৰ জিকা অৰণ্যৰ পৰা আহিছে। জিকা ভাইৰাছৰ ডেংগি, পীত জ্বৰ, জাপানীজ এন্কেফেলাইটিছ আৰু ৱেষ্ট নাইল ভাইৰাছৰ লগত সম্পৰ্ক আছে। ১৯৫০ চনমানৰে পৰা আফ্ৰিকা হৈ এছিয়া পৰ্যন্ত বিষুৱৰেখাৰ ওচৰে মাজৰে এই ৰোগ হোৱা বুলি জনা যায়। ২০০৭ চনৰ পৰা ২০১৬ লৈকে ভাইৰাছবিধ প্ৰশান্ত মহাসাগৰ পাৰ হৈ আমেৰিকালৈ বিয়পে আৰু ২০১৫-২০১৬ জিকা ভাইৰাছ মহামাৰীৰ সৃষ্টি কৰে।
জিকা জ্বৰ বা জিকা ভাইৰাছ ৰোগ বুলি কোৱা সংক্ৰমণে পাতলীয়া ডেংগি ৰোগৰ দৰে শূন্য বা নূন্যতম লক্ষণ উৎপন্ন কৰে। বিশেষ চিকিৎসা নাই যদিও পাৰাচিটামল ঔষধ আৰু বিশ্ৰামে লক্ষণ পৰিশমৰ সহায় কৰে। ২০১৬ চনলৈকে এই ৰোগ ঔষধ বা প্ৰতিষেধকেৰে প্ৰতিৰোধ কৰিব নোৱাৰি। গৰ্ভৱতী মহিলাৰ পৰা সন্তানলৈ জিকা বিয়পিব পাৰে। ইয়াৰ ফলত মাইক্ৰ'চিফালি (সৰু আকাৰৰ মূৰ), মগজুৰ গুৰুতৰ ক্ষতি আৰু আন জন্মগত খুঁত হ'ব পাৰে। প্ৰাপ্তবয়স্কত জিকা সংক্ৰমণে Guillain–Barré syndrome কৰিব পাৰিলেও সেয়া বিৰল।২০১৬ চনৰ জানুৱাৰীত আমেৰিকা যুক্তৰাষ্ট্ৰৰ Centers for Disease Control and Prevention (CDC)-এ আক্ৰান্ত দেশসমূহত বিশেষ সাৱধানতাকে ধৰি কেতবোৰ ভ্ৰমণৰ নিৰ্দেশাৱলী প্ৰকাশ কৰে। গৰ্ভৱতী মহিলাৰ বাবে ভ্ৰমণ পিছুৱাই দিয়াৰ দৰে পৰামৰ্শও দিয়া হয়। আন চৰকাৰ বা স্বাস্থ্য সন্থাই একে ধৰণৰ ভ্ৰমণ সতৰ্কবাণী দিয়ে, যাৰ ভিতৰত কলম্বিয়া, ডমিনিকান ৰিপাব্লিক, পৰ্টে ৰিক', ইকুৱেডৰ, এল্ ছাল্ভাদৰ আৰু জামাইকাই অধিক তথ্য নজনালৈকে মহিলাক গৰ্ভধাৰণ পিছুৱানলৈ পৰামৰ্শ দিয়ে। ২০১৭ চনৰ ১৫ মে'ত ভাৰত চৰকাৰৰ স্বাস্থ্য আৰু পৰিয়াল কল্যাণ মন্ত্ৰ্যালয়ে গুজৰাটৰ বাপুনগৰ অঞ্চলত তিনিজন জিকা ভাইৰাছ ৰোগী ধৰা পৰা বুলি নিশ্চিত কৰে। জিকাক /ˈziːkə/ বা /ˈzɪkə/ বুলি উচ্চাৰণ কৰা হয়।
জিকা ভাইৰাছ আৰু জিকা জ্বৰৰ এটা ভিডিঅ' বিৱৰণ।ਜ਼ੀਕਾ ਵਾਇਰਸ ਵਾਇਰਸਾਂ ਦੇ ਫ਼ਲੈਵੀਵਿਰੀਡੀ ਪਰਵਾਰ ਅਤੇ ਫ਼ਲੈਵੀਵਾਇਰਸ ਜੀਨਸ ਦਾ ਜੀਅ ਹੈ ਜੋ ਦਿਨ ਵੇਲੇ ਸਰਗਰਮ ਏਡੀਜ਼ ਮੱਛਰਾਂ, ਜਿਵੇਂ ਕਿ ਏਡੀਜ਼ ਏਜੀਪਟਾਈ ਅਤੇ ਏਡੀਜ਼ ਐਲਬੋਪਿਕਟਸ, ਵੱਲੋਂ ਫੈਲਾਇਆ ਜਾਂਦਾ ਹੈ। ਇਹਦਾ ਨਾਂ ਯੁਗਾਂਡਾ ਦੇ ਜ਼ੀਕਾ ਜੰਗਲ ਤੋਂ ਆਇਆ ਹੈ ਜਿੱਥੋਂ 1947 ਵਿੱਚ ਇਹਨੂੰ ਸਭ ਤੋਂ ਪਹਿਲਾਂ ਵੱਖਰਾ ਕੀਤਾ ਗਿਆ ਸੀ।[1]
ਇਹਦੇ ਤੋਂ ਹੁੰਦੇ ਰੋਗ, ਜੋ ਜ਼ੀਕਾ ਬੁਖ਼ਾਰ ਅਖਵਾਉਂਦਾ ਹੈ, ਦੇ ਲੱਛਣ ਨਾ-ਮਾਤਰ ਜਾਂ ਬਹੁਤ ਹਲ਼ਕੇ ਹੁੰਦੇ ਹਨ। 1950 ਦੇ ਦਹਾਕੇ ਤੋਂ ਲੈ ਕੇ ਇਹ ਅਫ਼ਰੀਕਾ ਤੋਂ ਏਸ਼ੀਆ ਤੱਕ ਪਸਰੀ ਤੰਗ ਭੂ-ਮੱਧ ਰੇਖਾਈ ਪੱਟੀ ਵਿੱਚ ਮਿਲਦਾ ਆਇਆ ਹੈ। 2014 ਵਿੱਚ ਇਹ ਵਾਇਰਸ ਪਰਸ਼ਾਂਤ ਮਹਾਂਸਮੁੰਦਰ ਪਾਰ ਕਰ ਕੇ ਪੂਰਬ ਵੱਲ ਫੈਲ ਗਿਆ ਅਤੇ ਨਤੀਜੇ ਵਜੋਂ ਫ਼ਰਾਂਸੀਸੀ ਪਾਲੀਨੇਸ਼ੀਆ, ਫੇਰ ਈਸਟਰ ਟਾਪੂ ਅਤੇ 2015 ਵਿੱਚ ਮੈਕਸੀਕੋ, ਕੇਂਦਰੀ ਅਮਰੀਕਾ ਅਤੇ ਦੱਖਣੀ ਅਮਰੀਕਾ ਤੱਕ ਪੁੱਜ ਗਿਆ ਜਿੱਥੇ ਜ਼ੀਕਾ ਦੇ ਹੱਲੇ ਨੇ ਮਹਾਂਮਾਰੀ ਦਾ ਰੂਪ ਅਖਤਿਆਰ ਲਿਆ ਹੈ।[2]
ଜିକା ଭୁତାଣୁ (ZIKV)ଫ୍ଲାଭିଭିରିଡି ଭୁତାଣୁ ପରିବାର ଓ ଫ୍ଲାଭିଭୁତାଣୁ ଜେନସ୍ର ଏକ ସଦସ୍ୟ ଓ ଏହା ଦିବା ସକ୍ରିୟ ଏଡିସ ମଶା ପରିବାରର ଏଡିସ୍ ଇଜିପ୍ଟି ମଶାଦ୍ୱାରା ବ୍ୟାପିଥାଏ ।
ଡିସେମ୍ବର ୨୦୧୫ରେ ଏହି ଭୁତାଣୁର ପ୍ଲାସେଣ୍ଟା ମାଧ୍ୟମ ସଞ୍ଚାର ହୋଇ ଶିଶୁର ଛୋଟ ମୁଣ୍ଡ ବା ମାଇକ୍ରୋସେଫାଲି (microcephaly) ହେବା ସହିତ ମସ୍ତିଷ୍କ କ୍ଷତିଗ୍ରସ୍ତ ହେବା ସମ୍ଭାବନା ସନ୍ଦେହ କରାଯାଉଛି ।[୧]
ମାନବ ଶରୀରରେ ଏହା ସାମାନ୍ୟ ଅସୁସ୍ଥତା ସୃଷ୍ଟି କରେ ଯାହାକୁ ଜିକା ଜ୍ୱର, ଜିକା ବା ଜିକା ରୋଗ କୁହାଯାଏ ଓ ଏହି ରୋଗ ସନ ୧୯୫୦ରୁ ଆଫ୍ରିକାରୁ ଏସିଆ ପର୍ଯ୍ୟନ୍ତ ଏକ ଅଣଓସାରିଆ ବିଷୁବ ମଣ୍ଡଳୀୟ ଇଲାକାରେ ହେଉଥିବା ଜଣାଯାଏ । ସନ ୨୦୧୪ରେ ଏହା ପୂର୍ବଦିଗକୁ ପ୍ରଶାନ୍ତ ମହାସାଗରକୁ ଟପି ଫ୍ରେଞ୍ଚ ପଲିନେସିଆ, ଇସ୍ଟର ଦ୍ୱୀପକୁ ବ୍ୟାପିଗଲା ଓ ସନ ୨୦୧୫ରେ ମେକ୍ସିକୋ, ମଧ୍ୟ ଆମେରିକା, ୱେଷ୍ଟଇଣ୍ଡିଜ ଓ ଦକ୍ଷିଣ ଆମେରିକା ପର୍ଯ୍ୟନ୍ତ ଗତିକରି ପାଣ୍ଡେମିକ ବା ମହାମାରୀ ସ୍ତରକୁ ଚାଲିଗଲା ।[୨]1947 ମସିହାରେ ଉଗାଣ୍ଡାରେ କେତେକ ଲୋକଙ୍କ ଦେହରେ ଜିକା ପ୍ରଭାବିତ କୋଷ ଥିବା ଜଣାପଡ଼ିଥିଲା । ତେଣୁ ସେମାନେ ପୂର୍ବରୁ ଜିକାଦ୍ୱାରା ସଂକ୍ରମିତ ହୋଇଥିଲେ । ଏହା ପରେ ସାରା ଆଫ୍ରିକାରେ ବ୍ୟାପିଥିଲା ଜିକା । ତେବେ ନାଇଜିରିଆରେ ପ୍ରଥମ ସଂକ୍ରମିତ ରୋଗୀଙ୍କ ସଂପର୍କରେ ଜଣା ପଡ଼ିଥିଲା ପ୍ରାୟ ଗୋଟିଏ ଦଶନ୍ଧିପରେ, 1960 ମସିହାରେ । ଏହା ପରେ ପ୍ରାୟ 10-12 ଜଣ ରୋଗୀଙ୍କୁ ଏ ସଂକ୍ରମଣ ହୋଇଥିଲା । 1966 ମସିହାରେ ଦକ୍ଷିଣ ପୂର୍ବ ଏସିଆକୁ ଫେରିଲା ଏ ଭୂତାଣୁ । ଦକ୍ଷିଣ ପୂର୍ବ ଏସିଆର ପ୍ରଥମ ମାମଲା ପଦାକୁ ଆସିଲା । ଏହା ସହ ଭାରତ, ପାକିସ୍ତାନ, ମାଲେସିଆ, ଅଣ୍ଡୋନେସିଆ ଆଦି ଦେଶରେ ଅନେକ ସଂକ୍ରମିତ ମାମଲା ପଦାକୁ ଆସିଲା । ତେବେ ଏ ସମସ୍ତ ଅଞ୍ଚଳରେ ଜିକା ଏକ ମହାମାରୀରେ ପରିଣତ ହୋଇନଥିଲା । 2007ରେ ମାଇକ୍ରୋନେସିଆର ୟାପ୍ ଦ୍ୱୀପରେ ଏହା ଜିକା ମହାମାରୀରର ରୂପ ନେଲା । ୟାପ୍ର ଜନସଂଖ୍ୟା ଅତି ଅଳ୍ପ ଥିଲା । ଏହା ମଧ୍ୟରୁ ଜିକାଦ୍ୱାରା ସଂକ୍ରମିତ ହୋଇଥିଲେ 200ରୁ ଅଧିକ । 2013ରେ ଫ୍ରେଞ୍ଚ ପଲିନେସିଆରେ ଜିକାର ପ୍ରକୃତ ରୂପ ପଦାକୁ ଆସିଲା । ସଂକ୍ରମିତଙ୍କ ସଂଖ୍ୟା ଥିଲା 35,000 । ଏହା ମଧ୍ୟରୁ କେତେକ ପକ୍ଷାଘାତରେ ମଧ୍ୟ ପୀଡ଼ିତ ଥିଲେ । ପରବର୍ତ୍ତୀ ସମୟରେ କେତେକ ଗବେଷଣାରୁ ଜଣାପଜଡ଼ିଛି ଏହା ପରେ ମାଇକ୍ରୋ ସେଫାଲି ବା କ୍ଷୁଦ୍ର ମସ୍ତିଷ୍କ ଥିବା ଶିଶୁମାନେ ମଧ୍ୟ ଜନ୍ମ ହୋଇଥିଲେ । 2014 ଫୁଟ୍ବଲ ବିଶ୍ୱକପ୍ ସମୟରେ ହିଁ ପହଁଚିଥିଲା ଜିକା । ପ୍ରଥମେ ଉତ୍ତର ବ୍ରାଜିଲରେ ଜିକା ସଂକ୍ରମିତ ଘଟଣା ସାମ୍ନାକୁ ଆସିଲା । ତେବେ ସେହି ସମୟରେ ଆର୍ଜେଣ୍ଟନାର ରିଓ-ଡି-ଜେନିରୋରେ ହେଉଥିବା ବିଶ୍ୱ ନୌଚାଳନା ପ୍ରତିଯୋଗିତା ସମୟରେ ଜିକା ପହଁଚିଥିଲା ଦକ୍ଷିଣ ଆମେରିକାରେ । କାରଣ ଏଥିରେ ଭାଗ ନେଇଥିଲେ ପ୍ରଶାନ୍ତ ମହାସାଗରୀୟ ଦ୍ୱୀପର ଅନେକ ଅଧିବାସୀ । ବର୍ଷେ କାଳ ଏହା ବ୍ରାଜିଲରେ ଧୀରେ ଧୀରେ ବ୍ୟାପିବାରେ ଲାଗିଲା । ତେବେ 21 ଅକଟୋବର 2015ରେ ବ୍ରାଜିଲ ବାହାରେ ପ୍ରଥମ ମାମଲା ପଦାକୁ ଆସିଲା କଲମ୍ବିଆରେ । ଏହା ପରେ ନଭେମ୍ବର ସୁଦ୍ଧା ସୁରିନାମ, ଏଲ-ସାଲଭାଡର, ଗୁଏଟମାଲା ଆଦି ଦେଶରେ ଗୋଟିଏ ପରେ ଗୋଟିଏ ଘଟଣା ସାମ୍ନାକୁ ଆସିଲା । ଡିସେମ୍ବର ପ୍ରଥମ ଭାଗରେ ଏହା ମେକ୍ସିକୋକୁ ବ୍ୟାପିଲା । ଏହାପରେ ଯୁକ୍ତରାଷ୍ଟ୍ର, ପାରାଗୁଏ, ଭେନେଜୁଏଲା ଓ ପାନାମାରେ ଆତଙ୍କ ସୃଷ୍ଟି ହେଲା । ଜାନୁଆରୀରେ ଏହା ହଣ୍ଡୁରାସ, ପର୍ଟୋରିକୋ, ଫ୍ରେଞ୍ଚ ଗୁଏନା, ମାର୍ଟିନିକରେ ମଧ୍ୟ ବ୍ୟାପିଲା ଜିକା । ଗତ ସପ୍ତାହରେ ଗୁଏନା, ବାର୍ବାଡସ, ଇକ୍ୱେଡର, ବଲିଭିଆ, ହାଇତି ଓ ଡୋମିନିକାନ ରିପବ୍ଲିକରେ ମଧ୍ୟ ଜିକା ବ୍ୟାପିଲା । ଏହା ବାଦ ଯୁକ୍ତରାଷ୍ଟ୍ର ଆମେରିକା, ଯୁକ୍ତରାଜ୍ୟ, ଡେନମାର୍କ ଓ ଜର୍ମାନୀରେ ମଧ୍ୟ କେତେକ ଜିକା ସଂକ୍ରମିତ ମାମଲା ଜଣାପଡ଼ିଛି । ତେବେ ବିଶେଷଜ୍ଞଙ୍କ କହିବା କଥା ଏସବୁ ପର୍ଯ୍ୟଟକଙ୍କଦ୍ୱାରା ବ୍ୟାପିଛି ।
ଡେଙ୍ଗୁ, ୟେଲୋ ଫିଭର, ଜାପାନୀ ଏନକେଫାଲାଇଟିସ ଓ ୱେଷ୍ଟ ନାଇଲ ଭୁତାଣୁ ସହିତ ଜିକା ଭୁତାଣୁର ସମ୍ପର୍କ ଅଛି ।[୩] ସାମାନ୍ୟ ଧରଣର ଡେଙ୍ଗୁ ଜ୍ୱର ସହିତ ଜିକା ଜ୍ୱର ପ୍ରାୟ ସମାନ,[୩] ବିଶ୍ରାମହିଁ ଏହାର ଚିକିତ୍ସା,[୪] ଓ ଏହା ନିମନ୍ତେ ଔଷଧ ବା ଟିକା ବାହାରି ନାହିଁ ।[୪] ଏହି ଜିକା ଜ୍ୱର ସହ ମାଇକ୍ରୋକେଫାଲି ସମ୍ପର୍କ ଥିବା ସମ୍ଭାବନା ଅଛି ଯାହା ମାଆଠାରୁ ଶିଶୁ ସଂକ୍ରମିତ ପ୍ରଲମ୍ବ ସଞ୍ଚାର (vertical transmission) ହୁଏ,[୫][୧][୬] ଓ ସଂକ୍ରମିତ ବୟଃପ୍ରାପ୍ତ ଲୋକଙ୍କର ସ୍ନାୟୁଜିନିତ ରୋଗ ଓ ଗଲେନ-ବାରି ସିଣ୍ଡ୍ରୋମ ସହିତ ସମ୍ପର୍କ ଥିବା ଜଣାଯାଏ । ଜାନୁଆରୀ ୨୦୧୬ରେ ଯୁକ୍ତରାଷ୍ଟ୍ର ଆମେରିକାର ରୋଗ ନିୟନ୍ତ୍ରଣ ଓ ପ୍ରତିଷେଧ ସଂସ୍ଥା Centers for disease control and prevention ତରଫରୁ ଏହି ଭୁତାଣୁ ଠାରୁ ସୁରକ୍ଷିତ ରହିବାପାଇଁ ଏହାଦ୍ୱାରା ସଂକ୍ରମିତ ଦେଶମାନଙ୍କର ସୂଚନା, ଏହାର ଲକ୍ଷଣ ଓ ପ୍ରତିରୋଧକ ବିଷୟରେ ସୂଚନାପତ୍ର ଜାରି କରାଯାଇ ଏଥିରେ ବର୍ଭବତୀ ମହିଳାଙ୍କୁ ରୋଗ ପ୍ରବଣ ଇଲାକାର ଭ୍ରମଣକୁ ବିଳମ୍ବିତ କରିବାକୁ କୁହାଯାଇଛି ।[୭][୮] ଅନ୍ୟ ସରକାରମାନେ ଓ ସ୍ୱାସ୍ଥ୍ୟ ସଂଗଠନଗୁଡ଼ିକ ଏହିଭଳି ଚେତାବନୀ ଦେଇଛନ୍ତି,[୯][୧୦][୧୧] ଅନ୍ୟ ପକ୍ଷରେ ଡୋମିନିଆନ ରିପବ୍ଲିକ, ଇକୁଏଡର, ଏଲ ସାଲଭାଡର ଓ ଜାମାଇକାରେ ଏହାର ସଙ୍କଟ ବିଷୟରେ ସଠିକ ଧାରଣା ମିଳିବା ପର୍ଯ୍ୟନ୍ତ ଗର୍ଭାଧାନ ବିଳମ୍ବିତ କରିବାକୁ ପରାମର୍ଶ ଦିଆଯାଇଛି । [୧୦][୧୨] ଫେବ୍ରୁଆରୀ ୨ ତାରିଖ ଦିନ ଯୁକ୍ତରାଷ୍ଟ୍ର ଆମେରିକାର ଡଲାସ କାଉଣ୍ଟି ହେଲ୍ଥ ଆଣ୍ଡ ହ୍ୟୁମାନ ସର୍ଭିସେସ ଏହି ରୋଗର ପ୍ରଥମ ସଞ୍ଚାର ବିଷୟରେ ସୂଚନା ଦେଇଥିଲେ । [୧୩] [୧୪]
ଜିକା ଭୁତାଣୁ ସାଧାରଣତଃ ଦିନବେଳେ ଦେଖାଯାଉଥିବା ମଶା ମାନଙ୍କଦ୍ୱାରା ସଂକ୍ରମିତ ହୋଇଥାଏ । ଏହି ଭୁତାଣୁ ଦିବା-ସକ୍ରିୟ ଏଡିସ୍ ଜାତିର ମଶା ଯେପରିକି ଏଡିସ୍ ଇଜିପ୍ଟି ଓ ଆର୍ବୋରିଆଲ ମଶା ଯେପରିକି ଏ ଆଫ୍ରିକାନସ୍ ଦେହରୁ ମିଳିଛି । [୧୫]
ଏ ଭୂତାଣୁ ସଂକ୍ରମଣ ହେଲେ ସାଧାରଣ ଭାବେ କୁଣ୍ଡାଇ ହେବା, ଥଣ୍ଡା ଧରିବା, ଛିଙ୍କ ହେବା, ଆଖି ଲାଲ ପଡ଼ିବା, ଆଣ୍ଠୁ ଗଣ୍ଠି ଦରଜ ହେବା ଭଳି ଲକ୍ଷଣ ଦେଖାଦିଏ । ତେବେ 80 ଭାଗ କ୍ଷେତ୍ରରେ ଏହା ଅଳ୍ପ ଦିନରେ ସ୍ୱତଃ ଭଲ ହୋଇଯାଇଥାଏ । କିନ୍ତୁ ଏହାର ମାରାତ୍ମକ ଦିଗ ହେଉଛି ଏହା ସହଜରେ ଏହି ଭୂତାଣୁ ସଂକ୍ରମଣଦ୍ୱାରା ଶିକାର ମହିଳାମାନଙ୍କଠାରୁ ଜନ୍ମ ଶିଶୁମାନଙ୍କଠାରେ ମସ୍ତିଷ୍କର ଆକାର ଅପେକ୍ଷାକୃତ ଛୋଟ ହେଇଥାଏ । ଅଧିକାଂଶ ସଂକ୍ରମିତ ଲୋକ ପକ୍ଷାଘାତର ଶିକାର ହୋଇଥାନ୍ତି । ତାଛଡ଼ା ଅନ୍ୟ ସ୍ନାୟବିକ ସମସ୍ୟା ମଧ୍ୟ ଦେଖାଦିଏ । ଜିକା ସଂକ୍ରମଣ ରୋକିବାକୁ କୌଣସି ଟୀକା ତିଆରି ହୋଇନି ବା ଏହାର ଉପଚାର ଲାଗି କୌଣସି ଔଷଧ ମଧ୍ୟ ନାହିଁ ବୋଲି କହିଛି କାଉନସିଲ । ତେଣୁ ପ୍ରତିଷେଧକ ହେଉଛି ଏଡିସ ମଶାକୁ ବ୍ୟାପିବାରୁ ରୋକିବା । ଏହି ମଶା ସଫା ପାଣିରେ ହିଁ ବଂଶବିସ୍ତାର କରେ । ।
|accessdate= (help) ଜିକା ଭୁତାଣୁ (ZIKV)ଫ୍ଲାଭିଭିରିଡି ଭୁତାଣୁ ପରିବାର ଓ ଫ୍ଲାଭିଭୁତାଣୁ ଜେନସ୍ର ଏକ ସଦସ୍ୟ ଓ ଏହା ଦିବା ସକ୍ରିୟ ଏଡିସ ମଶା ପରିବାରର ଏଡିସ୍ ଇଜିପ୍ଟି ମଶାଦ୍ୱାରା ବ୍ୟାପିଥାଏ ।
ଡିସେମ୍ବର ୨୦୧୫ରେ ଏହି ଭୁତାଣୁର ପ୍ଲାସେଣ୍ଟା ମାଧ୍ୟମ ସଞ୍ଚାର ହୋଇ ଶିଶୁର ଛୋଟ ମୁଣ୍ଡ ବା ମାଇକ୍ରୋସେଫାଲି (microcephaly) ହେବା ସହିତ ମସ୍ତିଷ୍କ କ୍ଷତିଗ୍ରସ୍ତ ହେବା ସମ୍ଭାବନା ସନ୍ଦେହ କରାଯାଉଛି ।
ମାନବ ଶରୀରରେ ଏହା ସାମାନ୍ୟ ଅସୁସ୍ଥତା ସୃଷ୍ଟି କରେ ଯାହାକୁ ଜିକା ଜ୍ୱର, ଜିକା ବା ଜିକା ରୋଗ କୁହାଯାଏ ଓ ଏହି ରୋଗ ସନ ୧୯୫୦ରୁ ଆଫ୍ରିକାରୁ ଏସିଆ ପର୍ଯ୍ୟନ୍ତ ଏକ ଅଣଓସାରିଆ ବିଷୁବ ମଣ୍ଡଳୀୟ ଇଲାକାରେ ହେଉଥିବା ଜଣାଯାଏ । ସନ ୨୦୧୪ରେ ଏହା ପୂର୍ବଦିଗକୁ ପ୍ରଶାନ୍ତ ମହାସାଗରକୁ ଟପି ଫ୍ରେଞ୍ଚ ପଲିନେସିଆ, ଇସ୍ଟର ଦ୍ୱୀପକୁ ବ୍ୟାପିଗଲା ଓ ସନ ୨୦୧୫ରେ ମେକ୍ସିକୋ, ମଧ୍ୟ ଆମେରିକା, ୱେଷ୍ଟଇଣ୍ଡିଜ ଓ ଦକ୍ଷିଣ ଆମେରିକା ପର୍ଯ୍ୟନ୍ତ ଗତିକରି ପାଣ୍ଡେମିକ ବା ମହାମାରୀ ସ୍ତରକୁ ଚାଲିଗଲା ।1947 ମସିହାରେ ଉଗାଣ୍ଡାରେ କେତେକ ଲୋକଙ୍କ ଦେହରେ ଜିକା ପ୍ରଭାବିତ କୋଷ ଥିବା ଜଣାପଡ଼ିଥିଲା । ତେଣୁ ସେମାନେ ପୂର୍ବରୁ ଜିକାଦ୍ୱାରା ସଂକ୍ରମିତ ହୋଇଥିଲେ । ଏହା ପରେ ସାରା ଆଫ୍ରିକାରେ ବ୍ୟାପିଥିଲା ଜିକା । ତେବେ ନାଇଜିରିଆରେ ପ୍ରଥମ ସଂକ୍ରମିତ ରୋଗୀଙ୍କ ସଂପର୍କରେ ଜଣା ପଡ଼ିଥିଲା ପ୍ରାୟ ଗୋଟିଏ ଦଶନ୍ଧିପରେ, 1960 ମସିହାରେ । ଏହା ପରେ ପ୍ରାୟ 10-12 ଜଣ ରୋଗୀଙ୍କୁ ଏ ସଂକ୍ରମଣ ହୋଇଥିଲା । 1966 ମସିହାରେ ଦକ୍ଷିଣ ପୂର୍ବ ଏସିଆକୁ ଫେରିଲା ଏ ଭୂତାଣୁ । ଦକ୍ଷିଣ ପୂର୍ବ ଏସିଆର ପ୍ରଥମ ମାମଲା ପଦାକୁ ଆସିଲା । ଏହା ସହ ଭାରତ, ପାକିସ୍ତାନ, ମାଲେସିଆ, ଅଣ୍ଡୋନେସିଆ ଆଦି ଦେଶରେ ଅନେକ ସଂକ୍ରମିତ ମାମଲା ପଦାକୁ ଆସିଲା । ତେବେ ଏ ସମସ୍ତ ଅଞ୍ଚଳରେ ଜିକା ଏକ ମହାମାରୀରେ ପରିଣତ ହୋଇନଥିଲା । 2007ରେ ମାଇକ୍ରୋନେସିଆର ୟାପ୍ ଦ୍ୱୀପରେ ଏହା ଜିକା ମହାମାରୀରର ରୂପ ନେଲା । ୟାପ୍ର ଜନସଂଖ୍ୟା ଅତି ଅଳ୍ପ ଥିଲା । ଏହା ମଧ୍ୟରୁ ଜିକାଦ୍ୱାରା ସଂକ୍ରମିତ ହୋଇଥିଲେ 200ରୁ ଅଧିକ । 2013ରେ ଫ୍ରେଞ୍ଚ ପଲିନେସିଆରେ ଜିକାର ପ୍ରକୃତ ରୂପ ପଦାକୁ ଆସିଲା । ସଂକ୍ରମିତଙ୍କ ସଂଖ୍ୟା ଥିଲା 35,000 । ଏହା ମଧ୍ୟରୁ କେତେକ ପକ୍ଷାଘାତରେ ମଧ୍ୟ ପୀଡ଼ିତ ଥିଲେ । ପରବର୍ତ୍ତୀ ସମୟରେ କେତେକ ଗବେଷଣାରୁ ଜଣାପଜଡ଼ିଛି ଏହା ପରେ ମାଇକ୍ରୋ ସେଫାଲି ବା କ୍ଷୁଦ୍ର ମସ୍ତିଷ୍କ ଥିବା ଶିଶୁମାନେ ମଧ୍ୟ ଜନ୍ମ ହୋଇଥିଲେ । 2014 ଫୁଟ୍ବଲ ବିଶ୍ୱକପ୍ ସମୟରେ ହିଁ ପହଁଚିଥିଲା ଜିକା । ପ୍ରଥମେ ଉତ୍ତର ବ୍ରାଜିଲରେ ଜିକା ସଂକ୍ରମିତ ଘଟଣା ସାମ୍ନାକୁ ଆସିଲା । ତେବେ ସେହି ସମୟରେ ଆର୍ଜେଣ୍ଟନାର ରିଓ-ଡି-ଜେନିରୋରେ ହେଉଥିବା ବିଶ୍ୱ ନୌଚାଳନା ପ୍ରତିଯୋଗିତା ସମୟରେ ଜିକା ପହଁଚିଥିଲା ଦକ୍ଷିଣ ଆମେରିକାରେ । କାରଣ ଏଥିରେ ଭାଗ ନେଇଥିଲେ ପ୍ରଶାନ୍ତ ମହାସାଗରୀୟ ଦ୍ୱୀପର ଅନେକ ଅଧିବାସୀ । ବର୍ଷେ କାଳ ଏହା ବ୍ରାଜିଲରେ ଧୀରେ ଧୀରେ ବ୍ୟାପିବାରେ ଲାଗିଲା । ତେବେ 21 ଅକଟୋବର 2015ରେ ବ୍ରାଜିଲ ବାହାରେ ପ୍ରଥମ ମାମଲା ପଦାକୁ ଆସିଲା କଲମ୍ବିଆରେ । ଏହା ପରେ ନଭେମ୍ବର ସୁଦ୍ଧା ସୁରିନାମ, ଏଲ-ସାଲଭାଡର, ଗୁଏଟମାଲା ଆଦି ଦେଶରେ ଗୋଟିଏ ପରେ ଗୋଟିଏ ଘଟଣା ସାମ୍ନାକୁ ଆସିଲା । ଡିସେମ୍ବର ପ୍ରଥମ ଭାଗରେ ଏହା ମେକ୍ସିକୋକୁ ବ୍ୟାପିଲା । ଏହାପରେ ଯୁକ୍ତରାଷ୍ଟ୍ର, ପାରାଗୁଏ, ଭେନେଜୁଏଲା ଓ ପାନାମାରେ ଆତଙ୍କ ସୃଷ୍ଟି ହେଲା । ଜାନୁଆରୀରେ ଏହା ହଣ୍ଡୁରାସ, ପର୍ଟୋରିକୋ, ଫ୍ରେଞ୍ଚ ଗୁଏନା, ମାର୍ଟିନିକରେ ମଧ୍ୟ ବ୍ୟାପିଲା ଜିକା । ଗତ ସପ୍ତାହରେ ଗୁଏନା, ବାର୍ବାଡସ, ଇକ୍ୱେଡର, ବଲିଭିଆ, ହାଇତି ଓ ଡୋମିନିକାନ ରିପବ୍ଲିକରେ ମଧ୍ୟ ଜିକା ବ୍ୟାପିଲା । ଏହା ବାଦ ଯୁକ୍ତରାଷ୍ଟ୍ର ଆମେରିକା, ଯୁକ୍ତରାଜ୍ୟ, ଡେନମାର୍କ ଓ ଜର୍ମାନୀରେ ମଧ୍ୟ କେତେକ ଜିକା ସଂକ୍ରମିତ ମାମଲା ଜଣାପଡ଼ିଛି । ତେବେ ବିଶେଷଜ୍ଞଙ୍କ କହିବା କଥା ଏସବୁ ପର୍ଯ୍ୟଟକଙ୍କଦ୍ୱାରା ବ୍ୟାପିଛି ।
இசீக்கா தீநுண்மம் (Zika virus, ZIKV) அல்லது ஜிகா வைரஸ் ஃபிளாவி தீநுண்மப் பேரினத்தின் ஃபிளாவிவிரிடே தீநுண்மக் குடும்பத்தைச் சேர்ந்த நச்சுயிரி ஆகும்; இதனை ஏடீசுக் கொசுவினக் கொசுக்கள் பரப்புகின்றன. மனிதர்களில், இது இசீக்கா காய்ச்சல் என்ற மிதமான நோயை உருவாக்குகின்றன. இந்த நோய் 1950களிலிருந்து ஆப்பிரிக்கா முதல் ஆசியா வரையான குறுகிய நிலநடுகோட்டு மண்டலத்தில் ஏற்பட்டு வந்தது. 2014இல் இந்த தீநுண்மம் கிழக்குநோக்கி பரவி அமைதிப் பெருங்கடலின் பிரெஞ்சு பொலினீசியாவிற்கும், பின்னர் ஈஸ்டர் தீவுக்கும் பரவியது. 2015இல் மத்திய அமெரிக்கா, கரீபியன் மற்றும் தென் அமெரிக்காவிற்கு பரவியது. தற்போது இது உலகம் பரவும் நோயாக கருதப்படுகின்றது.[1] இந்தக் காய்ச்சல் மிதமான டெங்குக் காய்ச்சல் போன்றுள்ளது.[2] இது ஓய்வு மூலமே குணப்படுத்தப்படுகின்றது;[3] இந்நோய்க்கு மருந்துகளோ தடுப்பு மருந்துகளோ இல்லை.[3] இசீக்கா நோய் பூச்சிவழிப் பரவும் ஃபிளாவி தீநுண்மங்களால் ஏற்படும் மஞ்சள் காய்ச்சலுடனும் மேற்கு நைல் நோயுடனும் தொடர்புடையது.[2] இசீக்கா நோயுற்ற கர்ப்பிணிப் பெண்களுக்குப் பிறந்த குழந்தைகளுக்கு குறுந்தலை ஏற்பட வாய்ப்புள்ளதாக தற்போது கருதப்படுகின்றது.[4][5] சனவரி 2016இல் ஐக்கிய அமெரிக்காவின் நோய்க் கட்டுப்பாடு மற்றும் தடுப்பு மையங்கள் (CDC) பாதிக்கப்பட்டுள்ள நாடுகளுக்கு பயணம் செல்வது குறித்த எச்சரிக்கையையும் எடுத்துக்கொள்ள வேண்டிய பாதுகாப்பு நடவடிக்கைகளையும் கர்ப்பிணிப் பெண்களுக்கான அறிவுரைகளையும் வெளியிட்டுள்ளன.[6][7] மற்ற அரசுகளும் நலவாழ்வு முகமைகளும் இதேபோன்ற பயண எச்சரிக்கைகளை வெளியிட்டுள்ளன.[8][9][10][11] கொலொம்பியா, எக்குவடோர், எல் சால்வடோர், ஜமேக்கா மற்றும் பிரேசில் [12]போன்ற நாடுகள் இந்நோயால் ஏற்படும் தீவாய்ப்புகளைக் குறித்து முழுமையாக அறியப்படும் வரை கருவுறுவதை தள்ளிப்போடுமாறு அறிவுறுத்தி உள்ளன.[9][13]
இக்குடும்பத்தின் மற்ற தீநுண்மங்களைப் போலவே இசீக்கா தீநுண்மமும் உறை கொண்டுள்ள பிரிவுகளில்லா ஒரே இழை இருபதுமுக முக்கோணக நேர்மறை ரைபோ கருவமில மரபணுத்தொகுதி ஆகும். இது இசுபான்டுவெனி தீநுண்மக் கிளையின் இரு தீநுண்மங்களில் ஒன்றாகும்.[14][15]
இத்தீநுண்மம் முதன்முதலாக 1947இல் உகாண்டாவின் இசீக்கா காட்டில் செம்முகக் குரங்கு ஒன்றிலிருந்து பிரித்தெடுக்கப்பட்டது; எனவேதான் இது இசீக்கா தீநுண்மம் என்று பெயரிடப்பட்டது. 1968இல் நைஜீரியாவில் முதன்முறையாக மனிதரிலிருந்து பிரித்தெடுக்கப்பட்டது.[16] 1951 முதல் 1981 வரை மத்திய ஆப்பிரிக்கக் குடியரசு, எகிப்து, காபோன், சியேரா லியோனி, தன்சானியா, உகாண்டா நாடுகளில் மனிதருக்கு தொற்றியிருந்திருக்கக்கூடிய சான்றுகள் உள்ளன. தவிரவும் இந்தியா, இந்தோனேசியா, மலேசியா, பிலிப்பீன்சு, தாய்லாந்து, வியட்நாம் போன்ற ஆசியப் பகுதிகளிலும் இருந்துள்ளது.[16]
நோய்தோன்றுவிதமாக நுழைந்தவிடத்திற்கு அருகிலுள்ள கிளையி உயிரணுக்களை தொற்றி பின்னர் நிணநீர்க்கணுக்களுக்கும் குருதியோட்டத்திலும் பரவுவதாக கருதுகோள் முன்வைக்கப்படுகின்றது.[14] ஃபிளாவி தீநுண்மங்கள் பொதுவாக திசுப் பாய்மத்தில் மறுவுருவாக்கம் பெறுகின்றன; ஆனால் இசீக்கா தீநுண்ம அயற்பொருட்கள் திசுவறை உட்கருவிலும் காணப்பட்டுள்ளன.[17]
இசீக்கா தீநுண்மம் ஒரு கடுமையான நரம்பியல் கோளாறுக்கு வழிவகுக்கும் என்றும், அதனால் பக்கவாதமும் உயிரிழப்பும்கூட ஏற்படலாம் என்றும் இந்த தீநுண்மத்தின் தாக்கம் தொடர்பில் தி லான்சட்டு மருத்துவமனையில் நடத்தப்பட்ட புதிய ஆய்வு கூறுகிறது.[18]
இசீக்கா தீநுண்மம் (Zika virus, ZIKV) அல்லது ஜிகா வைரஸ் ஃபிளாவி தீநுண்மப் பேரினத்தின் ஃபிளாவிவிரிடே தீநுண்மக் குடும்பத்தைச் சேர்ந்த நச்சுயிரி ஆகும்; இதனை ஏடீசுக் கொசுவினக் கொசுக்கள் பரப்புகின்றன. மனிதர்களில், இது இசீக்கா காய்ச்சல் என்ற மிதமான நோயை உருவாக்குகின்றன. இந்த நோய் 1950களிலிருந்து ஆப்பிரிக்கா முதல் ஆசியா வரையான குறுகிய நிலநடுகோட்டு மண்டலத்தில் ஏற்பட்டு வந்தது. 2014இல் இந்த தீநுண்மம் கிழக்குநோக்கி பரவி அமைதிப் பெருங்கடலின் பிரெஞ்சு பொலினீசியாவிற்கும், பின்னர் ஈஸ்டர் தீவுக்கும் பரவியது. 2015இல் மத்திய அமெரிக்கா, கரீபியன் மற்றும் தென் அமெரிக்காவிற்கு பரவியது. தற்போது இது உலகம் பரவும் நோயாக கருதப்படுகின்றது. இந்தக் காய்ச்சல் மிதமான டெங்குக் காய்ச்சல் போன்றுள்ளது. இது ஓய்வு மூலமே குணப்படுத்தப்படுகின்றது; இந்நோய்க்கு மருந்துகளோ தடுப்பு மருந்துகளோ இல்லை. இசீக்கா நோய் பூச்சிவழிப் பரவும் ஃபிளாவி தீநுண்மங்களால் ஏற்படும் மஞ்சள் காய்ச்சலுடனும் மேற்கு நைல் நோயுடனும் தொடர்புடையது. இசீக்கா நோயுற்ற கர்ப்பிணிப் பெண்களுக்குப் பிறந்த குழந்தைகளுக்கு குறுந்தலை ஏற்பட வாய்ப்புள்ளதாக தற்போது கருதப்படுகின்றது. சனவரி 2016இல் ஐக்கிய அமெரிக்காவின் நோய்க் கட்டுப்பாடு மற்றும் தடுப்பு மையங்கள் (CDC) பாதிக்கப்பட்டுள்ள நாடுகளுக்கு பயணம் செல்வது குறித்த எச்சரிக்கையையும் எடுத்துக்கொள்ள வேண்டிய பாதுகாப்பு நடவடிக்கைகளையும் கர்ப்பிணிப் பெண்களுக்கான அறிவுரைகளையும் வெளியிட்டுள்ளன. மற்ற அரசுகளும் நலவாழ்வு முகமைகளும் இதேபோன்ற பயண எச்சரிக்கைகளை வெளியிட்டுள்ளன. கொலொம்பியா, எக்குவடோர், எல் சால்வடோர், ஜமேக்கா மற்றும் பிரேசில் போன்ற நாடுகள் இந்நோயால் ஏற்படும் தீவாய்ப்புகளைக் குறித்து முழுமையாக அறியப்படும் வரை கருவுறுவதை தள்ளிப்போடுமாறு அறிவுறுத்தி உள்ளன.
జికా వైరస్ దోమ కాటు మనుషులకు వలన వ్యాప్తి చెందుతుంది.దూకుడుగా ఉండే ఈడిస్ ఈజిప్ట్ దోమ ద్వారా ఈ వైరస్ సోకుతుంది. నిజానికి ఎల్లో ఫీవర్, వెస్ట్నైల్ చికన్గన్యా, డెంగ్యూ వంటి వైరస్ల కుటుంబానికి చెందినదే జికా. ఆఫ్రికాలో బయలుదేరిన ఈ వైరస్. క్రమంగా లాటిన్ అమెరికా, పలు యూరప్ దేశాలకు విస్తరించింది.జికా వైరస్ సోకిన రోగికి వ్యాధి నయం చేసే మందులు లేవు. ఎబోలా వైరస్ సృష్టించిన బీభత్సం మర్చిపోకముందే కొన్ని తరాలను ప్రభావితం చేయగల ఒక వైరస్ ఇప్పుడు ప్రపంచాన్ని వణికిస్తున్నది.దోమల ద్వారా వ్యాపించే జికా అనే మహమ్మారి ఇప్పటికే 25 దేశాల్లో విస్తరించింది. దాదాపు 4వేల మంది అప్పుడే పుట్టిన శిశువుల భవితవ్యాన్ని అంధకారం చేసింది. వారిలో దాదాపు 50 మంది చిన్నారులు చనిపోయారు కూడా[1].
ప్రపంచాన్ని వణికిస్తున్న జికా వైరస్ పై భారత దేశ కేంద్రప్రభుత్వ ఆరోగ్యశాఖ అప్రమత్తం అయింది. ఇప్పటికి ప్రాథమిక అంచనాల ప్రకారం ఈ వైరస్ నలభై లక్షల మందికి సోకే ప్రమాదం ఉందనే ఆందోళన వ్యక్తం అవుతోంది. ప్రధానంగా గర్భిణీలు తేలిగ్గా ఈ వైరస్ బారిన పడే ప్రమాదం ఉందని చెబుతున్నారు. ధోమల కారణంగా ఈ వైరస్ వ్యాప్తి అవుతుందని ప్రపంచ ఆరోగ్య సంస్థ ప్రకటించింది.. ఫిబ్రవరి 1న కూడా ప్రపంచ ఆరోగ్య సంస్థ అత్యవసర సమావేశం ఏర్పాటు చేసింది.. భారత్ లోకి ఈ వైరస్ వస్తే తీసుకోవాల్సిన చర్యలపై కేంద్ర ఆరోగ్య శాఖ ఉన్నతస్థాయి సమావేశం ఏర్పాటు చేసింది.జికా వైరస్ రూపంలో ప్రపంచాన్ని వణికిస్తున్న వ్యాధి కారకం గురించి మొదట్లో ఎవరికీ తెలియదు. ఇది బ్రెజిల్లో గత ఏడాది వ్యాపించింది.2015 మార్చి నాటికి అంతు చిక్కని వ్యాధిగా గుర్తింపు పొందింది[2].
ప్రత్యేకించి లాటిన్ అమెరికాలో ఈ వైరస్ విస్తృతంగా వ్యాపిస్తున్నది.బొలీవియా, బ్రెజిల్, కేప్ వెర్డే, కొలంబియా, పరాగ్వే, అమెరికా వర్జిన్ ఐలాండ్స్, వెనిజులా, పోర్టెరికో తదితర దేశాల్లో ఇప్పటికే వ్యాపించింది.జికా వైరస్ నేపథ్యంలో కరీబియన్ దేశాలకు వెళ్లే ప్రయాణికులు, పర్యాటకులకు అమెరికా సెంటర్ ఫర్ డిసీజ్ కంట్రోల్, కెనడా ప్రభుత్వం హెచ్చరికలు జారీ చేశాయి.అతి త్వరలో ఈ వైరస్ చిలీ, కెనడా మినహా మొత్తం రెండు అమెరికా ఖండాలకూ విస్తరించే అవకాశం ఉందని ప్రపంచ ఆరోగ్య సంస్థ (డబ్ల్యూహెచ్వో) హెచ్చరించింది.ఇప్పటికే వైరస్ ఉన్న దేశాల్లోని మహిళలు కనీసం మరో రెండేండ్ల వరకూ గర్భం దాల్చవద్దని ఆయా దేశాలు హెచ్చరించాయి[1]. న్యూయార్క్లో మొదటి జీకా ఇన్ఫెక్షన్ను 2013 డిసెంబరులో కనిపెట్టారు. ఇప్పుడు ఈ వైరస్ లక్షలాది మందిని కబళించే అవకాశం ఉందని శాస్త్రవేత్తలు చెప్తున్నారు. ప్రస్తుతం33దేశాల్లో జికా వ్యాపించిందంటున్నారు[2].
ఈ వైరస్ సోకిన మహిళ గర్భం దాల్చితే పుట్టబోయే బిడ్డలు అసాధారణమైన రీతిలో చిన్న తలలతో (మైక్రోసిఫలే) పుడతారని, కొన్ని సందర్భాల్లో శిశువుకు వృద్ధిపరమైన సమస్యలు తలెత్తుతాయని, మరింత తీవ్రతరమైతే మృతశిశువులే మిగులుతాయని పేర్కొంటున్నారు.ఇప్పటికే పలు కేసులలో ఉమ్మ నీరు ద్వారా గర్భంలోని చిన్నారులకు ఈ వైరస్ సోకింది. ఒక్క బ్రెజిల్లోనే 4వేల మంది గర్భిణులు చిన్న తలలతో కూడిన బిడ్డలకు జన్మనిచ్చారు.మైక్రోసిఫలే అనే ఈ వ్యాధి లక్షణానికి చికిత్స కూడా లేదు.గర్భిణులకు ఈ వైరస్ సోకిందీ లేనిదీ తెలుసుకోవడం కూడా అసాధ్యం[1]. కొలంబియాలో ఇప్పటివరకు 3,100మంది గర్భిణులకు సోకినట్లు ఆ దేశ అధ్యక్షుడు జువాన్ మాన్యుయేల్ సాంటోస్ శనివారం తెలియజేశారు. జికా వైరస్ కారణంగా పుట్టబోయే బిడ్డల యొక్క తలలు పూర్తి పరిమాణంలో అభివృద్ధి చెందవు.కొలంబియాలో మొత్తం 25,645 మంది జికా వైరస్ బారిన పడ్డారని, అందులో 3,177 మంది గర్భిణులు ఉన్నట్లు సాంటోస్ వివరించారు[3]
ఈడిస్ దోమ ఈ వైరస్కు వాహకంగా పనిచేస్తుంది.లైంగిక సంపర్కం ద్వారా కూడా ఈ వైరస్ వ్యాప్తి చెందుతుందనే హెచ్చరికలు ఉన్నప్పటికీ దీన్ని ధ్రువీకరించేందుకు ఇప్పటి వరకూ కేవలం రెండే కేసులు ఉదాహరణగా ఉన్నాయి. రక్తమార్పిడి ద్వారా కూడా ఈ వైరస్ సోకుతుంది.ఈ వైరస్ సోకినవారికి జ్వరం, తలనొప్పి, వంటి మీద దద్దుర్లు, కండ్లు ఎర్రబారడం వంటి సాధారణ లక్షణాలు ఉంటాయి. దీనితో పరిస్థితి ముదిరిపోయేదాకా దీనిని గుర్తించడం కష్టమవుతుంది[1].అధిక ఉష్ణోగ్రతలు ఉన్న చోట జికా వైరస్ అధికంగా వ్యాప్తి చెందుతున్నట్లు శాస్త్రవేత్తలు చెబుతున్నారు. ఇలా ఇప్పుడే చెప్పడం తొందరపాటే అయినప్పటికీ చాలా సందర్భాల్లో వైరస్ల వ్యాప్తిలో వాతావరణం కీలక పాత్ర పోషిస్తుందంటున్నారు. అధిక ఉష్ణోగ్రతతో దోమ మరిన్ని దోమల్ని ఉత్పత్తి చేస్తుందని వారు చెబుతున్నారు.
చాలామందిలో బయటకు ఎటువంటి లక్షణాలు కన్పించకపోవచ్చును.కాకపోతే కొద్దిపాటి జ్వరం, వంటిపై దద్దుర్లు, కీళ్ళనొప్పులు, కళ్ళకలక (కళ్ళుఎర్రబడటం) వంతివి కనబడతాయి.కొంతమందికి కండరాలనొప్పులు కనిపించ వచ్చును. కొందరిలో తలనొప్పి ఉంటుంది.ఓకసారి వైరస్ సోకాక లక్షణాలు కనిపించటానికి కొద్ది రోజులు మొదలుకొని కొన్ని వారాలు పట్టవచ్చును.వైరస్ సోకితే అది వ్యాధికి గురైన వారి రక్తంలో కొన్ని రోజులు మొదలుకొని, కొన్నాళ్ళవరకు ఉండవచ్చును.అంటే లక్షణాలు బయటకు కనిపించకపోయినా, వ్యాధి వ్యాపింపచేసె పరిస్థితిలో వారుంటారు.
వ్యాధి సోకినపుడు ఏర్పడె వ్యాధి లక్షణాలు ప్రాణాంతకం కాదు, సాధారణ తలనొప్పులు, వళ్లునొప్పులే, అయితే వ్యాధిసోకిన తర్వాత కలిగే దశలు చాలా ప్రమాదకరమైనవి.అవి సరీర/దేహ రోగనిరోధక వ్యవస్థను దెబ్బతీసేఆటో ఇమ్మ్యూన్ వ్యాధులను కలగజేయవచ్చును.ఆతరువాత రోగికి గులియన్ బ్యారీ సిండ్రోమ్, మొదడు కుంచించుకుపోయే మైక్రోసెఫాలీ వంటి ప్రమాదకరమైన పరిస్థితులు ఏర్పడ వచ్చును.
ప్రపంచ దేశాలను వణికిస్తున్న జికా వైరస్ లైంగిక చర్య ద్వారా కూడా వ్యాప్తి చెందుతోంది. టెక్సాస్లో ఈ విధంగా జికా సోకిన తొలి కేసు నమోదైంది.ఈ మేరకు అమెరికా ఆరోగ్య విభాగ వర్గాలు ధ్రువీకరించాయి.ఇప్పటివరకూ ఈ వైరస్ దోమల ద్వారానే సోకుతుందని భావించారు. తాజాగా వైరస్ సోకిన వారితో లైంగిక చర్య ద్వారా కూడా సోకుతుందని తేలింది.ఈ మేరకు అమెరికా సెంటర్స్ ఫర్ డిసీజ్ కంట్రోల్ అండ్ ప్రివెన్షన్ డెరైక్టర్ డాక్టర్ టామ్ ఫ్రీడెన్ ఓ ఈ మెయిల్లో స్పష్టం చేశారు[4].
జికా వైరస్ గర్భిణుల పాలిట శాపంగా పరిణమిస్తోంది. ఈ వైరస్ గర్భిణుల నుంచి పిల్లలకు సోకి ఆందోళన కలిగిస్తోందని ప్రపంచ ఆరోగ్య సంస్థ (డబ్ల్యూహెచ్వో) తెలిపింది. ఈ వైరస్తో సంభవించే మైక్రోసెఫలీ అనే వ్యాధి పుట్టబోయే పిల్లల మెదడు ఎదుగుదలపై తీవ్ర ప్రభావం చూపుతోంది. జికా ప్రభావిత ప్రాంతాల్లో పర్యటించవద్దని గర్భిణులకు డబ్ల్యూహెచ్వో సూచిస్తోంది[4].
వ్యాధిసోకిన తరువాత నిర్దిష్త చికిత్స ప్రక్రియ లేదు.ఇతర వైరల్ జబ్బుల విషయంలో ఇచ్చే మందులే దీనికి ఇస్తారు.ఇప్పటివరకు జికా వైరస్కి ప్రత్యేకంగా మందులు కానీ, వ్యాక్సిన్లు కానీ లేవు. బాగా విశ్రాంతి తీసుకోవాలి. శరీరం డీ హైడ్రేషన్కి గురికాకుండా ద్రవపదార్థాలు ఎక్కువగా తీసుకోవాలి.జ్వరం, నొప్పులను తగ్గించే మందులు వాడాలి.యాస్ప్రిన్ గానీ, ఇంకా ఇతర నాన్ స్టిరాయిడల్ యాంటీ ఇన్ఫ్లమేటరీ డ్రగ్స్ అంటే ఇబుప్రొఫెన్, న్యాప్రాక్సెన్ లాంటివి వాడకూడదు. డెంగ్యూ, జికా లక్షణాలు లేవని తేలేవరకు ఈ మందులను వాడకూడదు. అలా వాడితే రక్తస్రావం ప్రమాదం ఉంటుంది.మరేదైనా అనారోగ్యానికి మందులు వాడుతున్నవారు కూడా డాక్టరుని సంప్రదించాకే మందులు వేసుకోవాలి.జికా లక్షణాలున్నవారికి ఒక వారం వరకు మళ్లీ మళ్లీ దోమలు కుట్టకుండా జాగ్రత్తపడాలి. ఎందుకంటే ఇన్ఫెక్షన్ సోకిన మొదటివారంలో రక్తంలో జికా వైరస్ ఉంటుంది. దోమలు మళ్లీ కుట్టినపుడు ఆ వైరస్ వాటి ద్వారా తిరిగి మరొక వ్యక్తికి సంక్రమించవచ్చు. ఇన్ఫెక్షన్కి కారణమయ్యే వైరస్ని మోసుకువెళ్లే దోమ అది కుట్టినవారికి దాన్నివ్యాపింపచేస్తుంది[5].
తగినంత విశ్త్రాంతి తీసుకోవాలి.ద్రవ ఆహారాని ఎక్కువ తీసుకోవడం వలన డిహైడ్రెసన్ తగ్గించవచ్చును.జ్వరాన్ని తగ్గించూ అసిటమినొపెన్ (acetaminophen) వంటి మందుమాత్రలు వాడాలి.అస్ప్రిన్, నాన్ స్టెరీయోడల్ (non-steroidal), నొప్పినివారణమందులు (anti-inflammatory ) వాడరాదు[6].
జికా వైరస్ను గుర్తించడం కూడా చాలా ఆశ్చర్యకరంగా జరిగింది. బ్రెజిల్ డాక్టర్లు వైద్య శాస్త్రానికి అంతుబట్టని వ్యాధి ఏదో ప్రబలుతోందని గమనించారు. అంతకుముందు కనిపించని లక్షణాలు కనిపిస్తున్నాయని గుర్తించారు. గుర్తించడం కూడా చాలా ఆశ్చర్యకరంగా జరిగింది. బ్రెజిల్ డాక్టర్లు వైద్య శాస్త్రానికి అంతుబట్టని వ్యాధి ఏదో ప్రబలుతోందని గమనించారు. అంతకుముందు కనిపించని లక్షణాలు కనిపిస్తున్నాయని గుర్తించారు.నవజాత శిశువుల ముఖాలు సాధారణంగానే ఉంటున్నా, నుదుటి భాగం వింతగా ఉంటోందని, అయినప్పటికీ వీరు ఆరోగ్యంగానే ఉంటున్నారని పరిశీలనగా చూసి తెలుసుకున్నారు. దీనిని మైక్రోసెఫలీ అని పేర్కొన్నారు. డాక్టర్లు తాము చూసిన ఇటువంటి పిల్లల గురించి ఒకరికొకరు చెప్పుకున్నారు. అయితే ఇదంతా భారీ ప్రభంజనానికి కారణమవుతుందని వారికి తెలియదు. దోమల ద్వారా జికా వైరస్ ఓ ఏడాది నుంచి బ్రెజిల్లో వ్యాపిస్తోందని వారికి సమాచారం లేదు. ఈ శిశువులకు ఏమైందో తెలుసుకోవడానికి చేసిన ప్రయత్నాలే జీకా వైరస్ గురించి తెలుసుకోగలిగేలా చేశాయి.డాక్టర్లు మొదట్లో ఈ వ్యాధిని స్వల్ప స్థాయిలో డెంగ్యూ అని అభిప్రాయపడ్డారు. కానీ పరీక్షల్లో అది నిజం కాదని తేలడంతో ఏదో తెలియనిది వ్యాపిస్తోందని భావించి అప్రమత్తమయ్యారు.2015మార్చి నాటికి ఇది నిర్లక్ష్యం చేయడానికి వీల్లేని వ్యాధి స్థాయికి ఎదిగింది. ఇది ఎలర్జీ అని డాక్టర్లు భావించారు. కలుషిత నీటి వల్ల వ్యాపిస్తూ ఉండొచ్చని కొందరు అనుకున్నారు. సాల్వడార్లోని బహియా విశ్వవిద్యాలయంలో వైరాలజిస్ట్ డాక్టర్ గుబియో సోర్స్ మాత్రం ఇది దోమల ద్వారా వ్యాపిస్తోందేమోనని అనుమానించారు. తన కొలీగ్ డాక్టర్ సిల్వియా సర్దితో కలిసి రక్త నమూనాలను పరీక్షించారు. ఇతర వైద్యులు కూడా ఇదే విధంగా పరీక్షలు చేశారు. మొత్తం 6800బ్లడ్ శాంపిల్స్ను పరీక్షించారు. చివరికి డాక్టర్ గుబియో సోర్స్డాక్టర్, సిల్వియా సర్ది కచ్చితమైన ఫలితాలను సాధించారు.2015 ఏప్రిల్లో జికా వైరస్ను కనుగొన్నారు[2].
ఉగాండాలో 1947లో ఈ వైరస్ పుట్టిందని ఆ దేశ శాస్త్రవేత్తలు చెబుతున్నారు. మొదట కోతుల్లో దీన్ని గుర్తించారు. మనుషులకు అంత ప్రమాదకరం కాదులే అనుకున్నారు. కానీ చాలా వైరస్లు కాలక్రమేణా తమ జన్యువుల్లో మార్పులు సంతరించుకున్నట్టే జికా వైరస్లో కూడా మార్పులు వచ్చాయి. ఇప్పుడు ఈ వైరస్ మనుషులకు హాని తలపెట్టే స్థాయిలో బలపడింది. 1960లో ఆఫ్రికాలో మొట్ట మొదట దీన్ని మనిషికి సోకినట్టుగా గుర్తించారు. ఇప్పుడిది అమెరికా, ఆఫ్రికా దేశాలకే కాక ప్రపంచవ్యాప్తంగా వ్యాప్తి చెందింది. 2014లో బ్రెజిల్లో గుర్తించగా ఇప్పు డక్కడ వందల కేసులు నమోదు అవుతున్నాయి. కొలంబియా, సాల్వేడార్, పరాగ్వే వెనిజులా, పనామా, ఫ్రంచ్ గయానా, ఈక్వెడార్, కరేబియన్ దీవులు, బొలీవియా, హైతీ…ఈ వరుస పెరిగి పెరిగి…ప్రస్తుతం ప్రపంచ వ్యాప్తంగా 40లక్షల వరకు జికా వైరస్ బాధితులు ఉన్నట్టుగా సమాచారం[5].
హైదరాబాద్కు చెందిన భారత్ బయోటెక్ సంస్థ దీనికి టీకా/వ్యాక్సిన్ కనుగొన్నట్లుగా చెప్పుచున్నది.అయితే అది ఇంకా ప్రీ-కికికల్ ప్రయోగ దశలో ఉందనీ, చాలాత్వరలో అందుబాటులోకి రానుందని తెలిపారు.రెండున్నరేళ్లుగా జికా వైరస్ నిరోధక వ్యాక్సిన్పై పరిశోధనలు చేస్తున్నట్లు భారత్ బయోటెక్ వెల్లడించింది. డబ్ల్యూహెచ్వో, ప్రభుత్వ అనుమతితో ఈ వ్యాక్సిన్ వినియోగంలోకి రావడానికి రెండున్నరేళ్ల సమయం పడుతుందని ప్రకటించింది.ఇక రెండున్నరేళ్లుగా చేస్తున్న పరిశోధనల్లో ఫలితాలు కనిపించాయన్నారు. ప్రయోగశాల పరిశోధనల్లోనూ వ్యాక్సిన్తో జికా వైరస్ను నిరోధించగలిగామని స్పష్టం చేసింది. జికా వ్యాక్ పేరుతో వ్యాక్సినేషన్ను అందుబాటులోకి తెస్తామని పేర్కొంది[7]
ဇီကာဗိုင်းရပ်စ် (အင်္ဂလိပ်: Zika virus; အတိုကောက် ZIKV) သည် ဗိုင်းရပ်စ် မျိုးရင်း Flaviviridae တွင် ပါဝင်သော မျိုးစိတ် Flavivirus အုပ်စုဝင်ဖြစ်သည်။ ဇီကာဗိုင်းရပ်စ်သည် နေ့အချိန်တွင် လှုပ်ရှားသွားလာသည့် အေးဒီးစ် ခြင်ကြောင့် ကူးစက်ပြန့်ပွားသည်။
လူများတွင် ဇီကာအဖျားရောဂါ အမည်ရှိ မပြင်းထန်သည့် အဖျားရောဂါကို ဖြစ်ပွားစေသည်။ ၁၉၅၀ ခုနှစ်များဝန်းကျင်တွင် အာဖရိကနှင့် အာရှအကြား အီကွေတာ ခါးပတ်အနီးတဝိုက်တွင် စတင်ဖြစ်ပွားခဲ့သည်။ ၂၀၁၄ ခုနှစ်တွင် ဗိုင်းရပ်စ်သည် ပစိဖိတ်သမုဒ္ဒရာကို ဖြတ်ပြီး ပြင်သစ်ပိုလီနီးရှားနှင့် အီစတာကျွန်းသို့ လည်းကောင်း၊ ၂၀၁၅ တွင် မက္ကဆီကို၊ ဗဟိုအမေရိက၊ ကာရစ်ဘီယံနှင့် တောင်အာဖရိကသို့ ကူးစက်ပြန့်ပွားလာကာ ကမ္ဘာအနှံ့တွင် ဖြစ်ပွားသည့် ကပ်ရောဂါအသွင် ဆောင်လာနေသည်။[၁]
ဇီကာဗိုင်းရပ်စ်သည် သွေးလွန်တုပ်ကွေး၊ အဝါရောင်အဖျားရောဂါ၊ ဂျပန်ဦးနှောက်အမြှေးရောင်ရောဂါ၊ နှင့် West Nile ဗိုင်းရပ်စ်များနှင့် ဆက်စပ်လျက်ရှိသည်။[၂] အဖျားရောဂါသည် သွေးလွန်တုပ်ကွေး အပျော့စားနှင့် ဆင်တူကာ[၂] အနားယူခြင်းဖြင့် သက်သာပျောက်ကင်းနိုင်ပြီး[၃] ကာကွယ်ရန် ဆေးများ၊ ကာကွယ်ဆေးများ မရှိသေးပေ။[၃] မိခင်မှ ကလေးသို့း ကူးစက်ခြင်းကြောင့် ဇီကာအဖျားရောဂါနှင့် ဦးနှောက်မဖွံ့ဖြိုးပြီး ဦးခေါင်းသေးငယ်သည့် ကလေးများ မွေးဖွားခြင်းတို့ ဆက်စပ်နိုင်ဖွယ်ရာရှိသည်ဟု ယူဆထားပြီး[၄][၅][၆] လူကြီးတွင် ကူးစက်ခံရပါက Guillain–Barré syndrome ကဲ့သို့သော အာရုံကြောဆိုင်ရာ ရောဂါများ ဖြစ်ပွားနိုင်သည်။[၇]
ဇန်နဝါရီ ၂၀၁၆ တွင် အမေရိကန်နိုင်ငံ ဗဟိုရောဂါထိန်းချုပ်ရေးနှင့် ကာကွယ်ရေးဗဟိုဌာန (CDC) က ရောဂါဖြစ်ပွားလျက်ရှိသော နိုင်ငံများသို့ ခရီးသွားလာခြင်းနှင့် ပတ်သက်ပြီး သတိပေးထားသည်။ ကိုယ်ဝန်ဆောင်အမျိုးသမီးများကိုလည်း ခရီးသွားလာမှု ရွေ့ဆိုင်းထားရန် အကြံပြုထားသည်။[၈][၉] အခြားသော အစိုးရနှင့် ကျန်းမာရေးအဖွဲ့များကလည်း အလားတူ သတိပေးချက်များ ထုတ်ပြန်ထားသည်။[၁၀][၁၁][၁၂] ကိုလံဘီယာ၊ ဒိုမီနီကန်၊ အီကွေဒေါ၊ အယ်ဆာဗေဒိုနှင့် ဂျာမေးကားနိုင်ငံများတွင် အမျိုးသမီးများအား ကိုယ်ဝန်ယူခြင်းကို ရွေ့ဆိုင်းထားရန် အကြံပြုထားသည်။[၁၁][၁၃]
ဧပြီ ၁၉၄၇ တွင် Yellow Fever Research Institute မှ သိပ္ပံပညာရှင်များက ယူဂန်းဒါးနိုင်ငံ ဇီကာတောအုပ်တွင်းရှိ မျောက်စပ်တစ်ကောင်မှတဆင့် ဗိုင်းရပ်စ်ကို ရှာဖွေခွဲထုတ်နိုင်ခဲ့သည်။ ဇန်နဝါရီ ၁၉၄၈ တွင် ၎င်းနေရာ၌ပင် ဗိုင်းရပ်စ်ကို အေးဒီးစ် အာဖရိကနပ် ခြင်မှ ခွဲထုတ်နိုင်ခဲ့သည်။[၁၄][၁၅] မျောက်တွင် အဖျားရောဂါ ဖြစ်ပွားလာသောအခါ သုတေသနပညာရှင်များသည် မျောက်၏ သွေးရည်ကြည်ထဲရှိ ကူးစက်နိုင်သော ဗိုင်းရပ်စ်ကို ၁၉၅၂ တွင် ခွဲထုတ်နိုင်ခဲ့ပြီး ဇီကာဗိုင်းရပ်စ်ဟု စတင်ခေါ်ဝေါ်ခဲ့သည်။ ၁၉၆၈ တွင် နိုင်ဂျီးရီးယားနိုင်ငံ၌ လူတွင် ဇီကာဗိုင်းရပ်စ်ကို စတင်တွေ့ရှိခဲ့သည်။[၁၆] ၁၉၅၁ ခုနှစ်မှ ၁၉၈၁ ခုနှစ်အထိ လူတွင် ရောဂါဖြစ်ပွားမှုသည် ဗဟိုအာဖရိကနိုင်ငံ၊ အီဂျစ်နိုင်ငံ၊ ဂါဘွန်နိုင်ငံ၊ ဆီရာလီယွန်နိုင်ငံ၊ တန်ဇန်းနီးယားနိုင်ငံနှင့် ယူဂန်းဒါးနိုင်ငံ အစရှိသော အာဖရိကနိုင်ငံများနှင့် အိန္ဒိယနိုင်ငံ၊ အင်ဒိုနီးရှားနိုင်ငံ၊ မလေးရှားနိုင်ငံ၊ ဖိလစ်ပိုင်နိုင်ငံ၊ ထိုင်းနိုင်ငံနှင့် ဗီယက်နမ်နိုင်ငံစသော အာရှနိုင်ငံများတွင် ဖြစ်ပွားခဲ့ကြောင်း တွေ့ရှိရသည်။[၁၆]
ဇီကာဗိုင်းရပ်စ်တွင် အာဖရိက မျိုးနွယ်နှင့် အာရှမျိုးနွယ်ဟူ၍ နှစ်မျိုးရှိသည်။[၁၇] မျိုးဗီဇလေ့လာမှုများအရ အမေရိကတွင် ဖြစ်ပွားသည့် ဗိုင်းရပ်စ်မှာ အာရှမျိုးနွယ်နှင့် ဆင်တူပြီး ၂၀၁၃ ခုနှစ် ပြင်သစ်ပိုလီနီးရှားတွင် ဖြစ်ပွားခဲ့ရာမှ ရောက်ရှိလာသည်ဟု ညွှန်ပြနေသည်။[၁၈][၁၇]
ဇီကာဗိုင်းရပ်စ်သည် နေ့အချိန်တွင် ပျံသန်းလှုပ်ရှားသော ခြင်မှတဆင့် ကူးစက်ပြန့်ပွားသည်။ ဗိုင်းရပ်စ်ကို အေးဒီးစ် မျိုးစုခြင်များဖြစ်သည့် A. aegypti, နှင့် သစ်ပင်များပေါ်နေသည့် ခြင်များဖြစ်သည့်A. africanus, A. apicoargenteus, A. furcifer, A. hensilli, A. luteocephalus နှင့် A. vitattus တို့တွင် တွေ့ရှိရသည်။ ခြင်တွင် ရောဂါပိုးပေါက်ဖွားမှုမှာ ၁၀ ရက်ဖြစ်သည်။[၁၆]
ဗိုင်းရပ်စ်ကို သယ်ဆောင်သည့် ကျောရိုးရှိ သတ္တဝါများအနေဖြင့် လူနှင့် မျောက် တို့မှာ အဓိကဖြစ်သည်။[၇]
ဗိုင်းရပ်စ်ကူးစက်ခံရပါက ခံစားရသည့် လက္ခဏာများမှာ မပြင်းထန်သော ခေါင်းကိုက်ခြင်း၊ အနီစက်အကွက်များ ထခြင်း၊ ဖျားခြင်း၊ မအီမသာဖြစ်ခြင်း၊ မျက်စိနာခြင်းနှင့် အရိုးအဆစ်များ နာကျင်ခြင်းတို့ ဖြစ်သည်။ ဇီကာဗိုင်းရပ်စ်ကို စတင်ဖော်ပြခဲ့သည်မှာ ၁၉၆၄ ခုနှစ်တွင် ဖြစ်ပြီး မပြင်းထန်သည့် ခေါင်းကိုက်ခြင်းဖြင့် စတင်ကာ အနီစက်အကွက်များ ထခြင်း၊ ဖျားခြင်းနှင့် နောက်ကျောကိုက်ခဲခြင်းတို့ ဖြစ်လာသည်။ ထို့နောက် နှစ်ရက်အတွင်း အနီစက်အကွက်များ စတင်မှေးမှိန်လာပြီး သုံးရက်အတွင်း အဖျားပျောက်ပြီး အနီစက်အကွက်များသာ ကျန်ရစ်သည်။ ထို့ကြောင့် လက်ရှိ သိရှိရသလောက် ဇီကာဗိုင်းရပ်စ်သည် ရောဂါလက္ခဏာ မပြင်းထန်ပဲ ငါးဦးတွင် တစ်ဦးသာ လက္ခဏာပြတတ်ပြီး သေဆုံးမှု မရှိသေးပေ။ သို့သော် ရောဂါ၏ အမှန်တကယ် ဖြစ်ပွားနိုင်စွမ်းကိုကား မသိရှိရသေးပေ။[၁၆]
၂၀၁၆ ခုနှစ်အထိ ဇီကာဗိုင်းရပ်စ်အတွက် ကာကွယ်ဆေး မရှိသေးပေ။ ရောဂါလက္ခဏာများကို အနားယူခြင်း၊ အရည်ဖြည့်တင်းခြင်းနှင့် ပါရာစီတမောကို သောက်သုံးနိုင်ပြီး သွေးလွန်တုပ်ကွေးပုံစံ သွေးယိုစီးမှု ဖြစ်ပွားနိုင်ခြေ လျော့ကျစေရန်သာ အက်စပရင်နှင့် အခြားသော စတီးရွိုက်မပါသည့် အရောင်ကျဆေးများကို သောက်သုံးသင့်သည်။[၁၉]
ဒီဇင်ဘာ ၂၀၁၅ တွင် မိခင်မှ သန္ဓေသားသို့ ရောဂါပိုးကူးစက်မှုကြောင့် သန္ဓေသားတွင် ဦးနှောက်ထိခိုက်မှုနှင့် ဦးခေါင်းသေးငယ်ခြင်း ဖြစ်ပွားနိုင်စေသည်ဟု သံသယရှိထားသည်။[၅][၂၀] အမေရိကန် CDC အနေဖြင့် "ကိုယ်ဝန်ဆောင်နေစဉ်အတွင်း ဇီကာဗိုင်းရပ်စ် ကူးစက်ခံရမှုကြောင့် မွေးဖွားလာသည့် ကလေးငယ်များတွင် မွေးရာပါ ဦးနှောက်နှင့် ဦးခေါင်းသေးငယ်ခြင်း ဖြစ်ပွားကြောင်း အစီရင်ခံချက်များ ရရှိထားသည်။ များစွာသော ဦးခေါင်းသေးငယ်သည့် microcephaly ကလေးငယ်များတွင် ဇီကာဗိုင်းရပ်စ် ကူးစက်ခံထားရကြောင်းကို အတည်ပြုထားပြီး microcephaly မည်ရွေ့မည်မျှသည် ဇီကာဗိုင်းရပ်စ်နှင့် ဆက်စပ်မှုရှိနေကြောင်းကိုမူကား မသိရှိရသေး။" ဟု ထုတ်ပြန်ထားသည်။[၂၁]
ဇီကာရောဂါအတွက် ကာကွယ်ဆေးမရှိသေးပါ။ ရောဂါလက္ခဏာ သက်သာရန် အတွက်သာ ကုသပေးနိုင်ပါသည်။ အနားယူခြင်း၊ ရေလုံလောက်စွာ သောက်သုံးခြင်း၊ ဆေးမြီးတိုများနှင့် အခြား အကိုက်အခဲပျောက်ဆေးများကို မသောက်ရန်နှင့် ပါရာစီတမောကိုသာ အညွှန်းအတိုင်း သောက်သုံးရန်နှင့် ဇီကာရောဂါ လက္ခဏာများတွေ့ရှိပါက နီးစပ်ရာ ကျန်းမာရေးဌာန၊ ဆေးရုံ/ဆေးခန်းများသို့ သွားရောက်ပြသ၍ စစ်ဆေးကုသမှု ခံယူရန်လိုအပ်ပါသည်။
ရောဂါကူးစက်ဖြစ်ပွားမှုမရှိစေရေးအတွက် အကောင်းဆုံး ကာကွယ်နည်း မှာ ခြင်ကျား ပိုးလောက်လမ်း နှိမ်နင်းရေးနှင့် ခြင်ကိုက် ခံရခြင်း မရှိအောင် နေထိုင်ရေးဖြစ်ပါသည်။ အိမ်တိုင်း၊ ကျောင်းတိုင်း၊ ရုံးဌာနတိုင်း၌ ခြင်ကျားလောက်လမ်း တကောင်မျှ မရှိစေရေး အတွက် အောက်ပါတို့ကိုဆောင်ရွက်ရပါမည်။
ထို့ပြင် ခြင်ကိုက်မခံရစေရန် ခြင်ဆေးလိမ်းခြင်း၊ အကျႌ လက်ရှည်နှင့် ဘောင်းဘီရှည်များ ဝတ်ဆင်ခြင်း၊ နေအိမ်၌ ခြင်လုံ ဆန်ခါတပ်ခြင်း စသည်တို့ဆောင်ရွက်ရန် လိုအပ်ပါသည်။
ခြင်ကျားလောက်လမ်း တကောင်မှ မရှိစေရေးအတွက် ဖုံး၊ သွန်၊ လဲ၊ စစ် စသည့် ပိုးလောက်လမ်းနှိမ်နင်းရေး လုပ်ငန်းများကို လူတိုင်းပါဝင် ဆောင်ရွက်ခြင်းအားဖြင့် ဇီကာရောဂါ အပါအဝင် သွေးလွန် တုပ်ကွေးရောဂါ ကူးစက်ဖြစ်ပွားမှု မရှိအောင် ကာကွယ်နှိမ်နင်းနိုင် မည်ဖြစ်ပါကြောင်း အသိပေး နှိုးဆော်အပ်ပါသည်။ [၂၂]
ဇီကာဗိုင်းရပ်စ် (အင်္ဂလိပ်: Zika virus; အတိုကောက် ZIKV) သည် ဗိုင်းရပ်စ် မျိုးရင်း Flaviviridae တွင် ပါဝင်သော မျိုးစိတ် Flavivirus အုပ်စုဝင်ဖြစ်သည်။ ဇီကာဗိုင်းရပ်စ်သည် နေ့အချိန်တွင် လှုပ်ရှားသွားလာသည့် အေးဒီးစ် ခြင်ကြောင့် ကူးစက်ပြန့်ပွားသည်။
လူများတွင် ဇီကာအဖျားရောဂါ အမည်ရှိ မပြင်းထန်သည့် အဖျားရောဂါကို ဖြစ်ပွားစေသည်။ ၁၉၅၀ ခုနှစ်များဝန်းကျင်တွင် အာဖရိကနှင့် အာရှအကြား အီကွေတာ ခါးပတ်အနီးတဝိုက်တွင် စတင်ဖြစ်ပွားခဲ့သည်။ ၂၀၁၄ ခုနှစ်တွင် ဗိုင်းရပ်စ်သည် ပစိဖိတ်သမုဒ္ဒရာကို ဖြတ်ပြီး ပြင်သစ်ပိုလီနီးရှားနှင့် အီစတာကျွန်းသို့ လည်းကောင်း၊ ၂၀၁၅ တွင် မက္ကဆီကို၊ ဗဟိုအမေရိက၊ ကာရစ်ဘီယံနှင့် တောင်အာဖရိကသို့ ကူးစက်ပြန့်ပွားလာကာ ကမ္ဘာအနှံ့တွင် ဖြစ်ပွားသည့် ကပ်ရောဂါအသွင် ဆောင်လာနေသည်။
ზიკაშ ვირუსი (ინგლ. Zika virus, ZIKV) — Flavivirus ტიპიშ ვირუსიშ გვარობა (ფანია Flaviviridae), ნამუთ Aedes ტიპიშ კოღოეფს გინმუღუნა. ადამიერეფს ალახენს კინ თე ჯოხოდვალაშ ლახარათ, ნამუშოთ დჷმახასიათაფალი რე გიმორღვაფა, უჭყანობა, დუდიშ დო სახსარეფიშ ჭუა, სინჩხეშ მეჩამა, სახსარეფიშ შინაფა. ვირუსის მაართაშე მიოგორედს 1947 წანას, ნამუშ უკული 60 წანაშ გოძვენა, ხვალე 15 მოხვალამა რდჷ ეჭარილი თე ვირუსით დალახებაშ გეშა აფრიკას დო ობჟათე-ბჟაეიოლ აზიას. 2007 წანას, იაპიშ კოკეფშე ვირუსიქ გიფაჩჷ ბჟაეილჸურე რჩქალი ოკიანეშით. 2014 წანას, ვირუსიქ გიფაჩჷ ახალ კალედონიას, კუკიშ კოკეფს, საფრანგეთიშ პოლინეზიას, 2015 წანას — თანაფაშ კოკის დო ობჟათე ამერიკას, ცენტრალური ამერიკას, ვესტ-ინდოეთის. ასეიან ბორჯიშო ვირუსის პანდემიაშ სტატუსი უღუ. ზიკაშ ვირუიშ ლახარა მოგენს დენგეშ ლახარაშ ქექე ფორმას, თაშნეშე ჸვინთელ ლახარას დო ბჟადალი ნილოსიშ ლახარას. ვირუსიშ სააწმარენჯო სპეციფიკური წამალეფი ვარდა ვაქცინეფი ვა არსებენს.
Virusê zika (tıb de ZIKV nusiyeno) viruso ke keyeyê Flaviviridaei ra cınsê Flavivirus de ca gêno. Merduman miyan de Adırê zika ya zi nêweşiya Zika rê raye keno a, beno sebeb. Eno virus serra 2015ıne de veroc u miyanê Amerika de ame halê pandemiki.[1]
Virusê zika (tıb de ZIKV nusiyeno) viruso ke keyeyê Flaviviridaei ra cınsê Flavivirus de ca gêno. Merduman miyan de Adırê zika ya zi nêweşiya Zika rê raye keno a, beno sebeb. Eno virus serra 2015ıne de veroc u miyanê Amerika de ame halê pandemiki.
Al Vìrus Zika l'è 'n RNA vìrus dla famìja Filoviridae iśulâ par la prima vòlta in dal 1974 in Ugànda in dla furèsta Zika anc s'adès al s è stramnâ in tut al mónd, anc in Europa.
In di ès'r umàṅ al fà vgnir la févra Zika, un mâł ch'al sumìlia dimóndi a la dengue, a la févra śala, a l'encefalît dal Nîl ucidentàł e a l'encefalît giapunéśa. Al s ciàpa c'n al murśgàdi dal sinsàli, specialmènt qvéli dal gènar Aedes cuma la sinsàla tigra o l'Aedes aegypti. A s è vdû anc di caś in dua la gint la s è bcada la Zika insém a la Dengue e a la Chikungunya.
Al vìrus al viṿ in dal còrp di óm, dal simi e ad soquànt mamìfar, pò a gh pénsa la sinsàla a purtàr-'l in gir.
La févra Zika la n è minga 'n mâł ch'al faga patìr tròp però a n gh'è minga na cura, a gh'è sōl da spétar ch'al pasa da par lò dòp soquànt dè. Al pōl far vgnir dal maci rósi in sla pèla diti rash, na févra alśēra, mâł a la tèsta e la cungiuntivìte. Al 25% di malâ però al n gh fà gnanc a mènt.
A s pénsa ch'al vìrus Zika al pòsa ès'r un perìcul p'r al dóni ch'i gh'aṅ 'd avér fiōl parchè i putèṅ i pōlan nàsar c'n al sarvèl pìcul o dasfurmâ. In dal 2015 in Braśìl a 'n è nâ trimìla-òtsènt[1].
Al Vìrus Zika l'è 'n RNA vìrus dla famìja Filoviridae iśulâ par la prima vòlta in dal 1974 in Ugànda in dla furèsta Zika anc s'adès al s è stramnâ in tut al mónd, anc in Europa.
In di ès'r umàṅ al fà vgnir la févra Zika, un mâł ch'al sumìlia dimóndi a la dengue, a la févra śala, a l'encefalît dal Nîl ucidentàł e a l'encefalît giapunéśa. Al s ciàpa c'n al murśgàdi dal sinsàli, specialmènt qvéli dal gènar Aedes cuma la sinsàla tigra o l'Aedes aegypti. A s è vdû anc di caś in dua la gint la s è bcada la Zika insém a la Dengue e a la Chikungunya.
Al vìrus al viṿ in dal còrp di óm, dal simi e ad soquànt mamìfar, pò a gh pénsa la sinsàla a purtàr-'l in gir.
La févra Zika la n è minga 'n mâł ch'al faga patìr tròp però a n gh'è minga na cura, a gh'è sōl da spétar ch'al pasa da par lò dòp soquànt dè. Al pōl far vgnir dal maci rósi in sla pèla diti rash, na févra alśēra, mâł a la tèsta e la cungiuntivìte. Al 25% di malâ però al n gh fà gnanc a mènt.
A s pénsa ch'al vìrus Zika al pòsa ès'r un perìcul p'r al dóni ch'i gh'aṅ 'd avér fiōl parchè i putèṅ i pōlan nàsar c'n al sarvèl pìcul o dasfurmâ. In dal 2015 in Braśìl a 'n è nâ trimìla-òtsènt.
Zika virus (ZIKV; pronounced /ˈziːkə/ or /ˈzɪkə/[3][4]) is a member of the virus family Flaviviridae.[5] It is spread by daytime-active Aedes mosquitoes, such as A. aegypti and A. albopictus.[5] Its name comes from the Ziika Forest of Uganda, where the virus was first isolated in 1947.[6] Zika virus shares a genus with the dengue, yellow fever, Japanese encephalitis, and West Nile viruses.[6] Since the 1950s, it has been known to occur within a narrow equatorial belt from Africa to Asia. From 2007 to 2016, the virus spread eastward, across the Pacific Ocean to the Americas, leading to the 2015–2016 Zika virus epidemic.[7]
The infection, known as Zika fever or Zika virus disease, often causes no or only mild symptoms, similar to a very mild form of dengue fever.[5] While there is no specific treatment, paracetamol (acetaminophen) and rest may help with the symptoms.[8] As of April 2019, no vaccines have been approved for clinical use, however a number of vaccines are currently in clinical trials.[9][10][11] Zika can spread from a pregnant woman to her baby. This can result in microcephaly, severe brain malformations, and other birth defects.[12][13] Zika infections in adults may result rarely in Guillain–Barré syndrome.[14]
In January 2016, the United States Centers for Disease Control and Prevention (CDC) issued travel guidance on affected countries, including the use of enhanced precautions, and guidelines for pregnant women including considering postponing travel.[15][16] Other governments or health agencies also issued similar travel warnings,[17][18][19] while Colombia, the Dominican Republic, Puerto Rico, Ecuador, El Salvador, and Jamaica advised women to postpone getting pregnant until more is known about the risks.[18][20]
Zika virus belongs to the family Flaviviridae and the genus Flavivirus, thus is related to the dengue, yellow fever, Japanese encephalitis, and West Nile viruses. Like other flaviviruses, Zika virus is enveloped and icosahedral and has a nonsegmented, single-stranded, 10 kilobase, positive-sense RNA genome. It is most closely related to the Spondweni virus and is one of the two known viruses in the Spondweni virus clade.[21][22][23][24][25]

A positive-sense RNA genome can be directly translated into viral proteins. As in other flaviviruses, such as the similarly sized West Nile virus, the RNA genome encodes seven nonstructural proteins and three structural proteins in the form of a single polyprotein ().[27] One of the structural proteins encapsulates the virus. This protein is the flavivirus envelope glycoprotein, that binds to the endosomal membrane of the host cell to initiate endocytosis.[28] The RNA genome forms a nucleocapsid along with copies of the 12-kDa capsid protein. The nucleocapsid, in turn, is enveloped within a host-derived membrane modified with two viral glycoproteins. Viral genome replication depends on the making of double-stranded RNA from the single-stranded, positive-sense RNA (ssRNA(+)) genome followed by transcription and replication to provide viral mRNAs and new ssRNA(+) genomes.[29][30]
A longitudinal study shows that 6 hours after cells are infected with Zika virus, the vacuoles and mitochondria in the cells begin to swell. This swelling becomes so severe, it results in cell death, also known as paraptosis. This form of programmed cell death requires gene expression. IFITM3 is a trans-membrane protein in a cell that is able to protect it from viral infection by blocking virus attachment. Cells are most susceptible to Zika infection when levels of IFITM3 are low. Once the cell has been infected, the virus restructures the endoplasmic reticulum, forming the large vacuoles, resulting in cell death.[31]
There are two Zika lineages: the African lineage and the Asian lineage.[32] Phylogenetic studies indicate that the virus spreading in the Americas is 89% identical to African genotypes, but is most closely related to the Asian strain that circulated in French Polynesia during the 2013–2014 outbreak.[32][33][34]
The Asian strain appears to have first evolved around 1928.[35]
The vertebrate hosts of the virus were primarily monkeys in a so-called enzootic mosquito-monkey-mosquito cycle, with only occasional transmission to humans. Before 2007, Zika "rarely caused recognized 'spillover' infections in humans, even in highly enzootic areas". Infrequently, however, other arboviruses have become established as a human disease and spread in a mosquito–human–mosquito cycle, like the yellow fever virus and the dengue fever virus (both flaviviruses), and the chikungunya virus (a togavirus).[36] Though the reason for the pandemic is unknown, dengue, a related arbovirus that infects the same species of mosquito vectors, is known in particular to be intensified by urbanization and globalization.[37] Zika is primarily spread by Aedes aegypti mosquitoes,[38] and can also be transmitted through sexual contact[39] or blood transfusions.[40] The basic reproduction number (R0, a measure of transmissibility) of Zika virus has been estimated to be between 1.4 and 6.6 .[41]
In 2015, news reports drew attention to the rapid spread of Zika in Latin America and the Caribbean.[42] At that time, the Pan American Health Organization published a list of countries and territories that experienced "local Zika virus transmission" comprising Barbados, Bolivia, Brazil, Colombia, the Dominican Republic, Ecuador, El Salvador, French Guiana, Guadeloupe, Guatemala, Guyana, Haiti, Honduras, Martinique, Mexico, Panama, Paraguay, Puerto Rico, Saint Martin, Suriname, and Venezuela.[43][44][45] By August 2016, more than 50 countries had experienced active (local) transmission of Zika virus.[46]
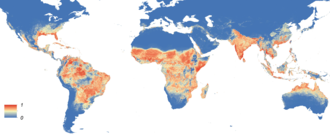
Zika is primarily spread by the female Aedes aegypti mosquito, which is active mostly in the daytime.[47][48] The mosquitos must feed on blood to lay eggs.[49]: 2 The virus has also been isolated from a number of arboreal mosquito species in the genus Aedes, such as A. africanus, A. apicoargenteus, A. furcifer, A. hensilli, A. luteocephalus, and A. vittatus, with an extrinsic incubation period in mosquitoes around 10 days.[24]
The true extent of the vectors is still unknown. Zika has been detected in many more species of Aedes, along with Anopheles coustani, Mansonia uniformis, and Culex perfuscus, although this alone does not incriminate them as vectors.[48] To detect the presence of the virus usually requires genetic material to be analysed in a lab using the technique RT-PCR. A much cheaper and faster method involves shining a light at the head and thorax of the mosquito, and detecting chemical compounds characteristic of the virus using near-infrared spectroscopy.[50]
Transmission by A. albopictus, the tiger mosquito, was reported from a 2007 urban outbreak in Gabon, where it had newly invaded the country and become the primary vector for the concomitant chikungunya and dengue virus outbreaks.[51] New outbreaks can occur if a person carrying the virus travels to another region where A. albopictus is common.[52]
The potential societal risk of Zika can be delimited by the distribution of the mosquito species that transmit it. The global distribution of the most cited carrier of Zika, A. aegypti, is expanding due to global trade and travel.[53] A. aegypti distribution is now the most extensive ever recorded – on parts of all continents except Antarctica, including North America and even the European periphery (Madeira, the Netherlands, and the northeastern Black Sea coast).[54] A mosquito population capable of carrying Zika has been found in a Capitol Hill neighborhood of Washington, DC, and genetic evidence suggests they survived at least four consecutive winters in the region. The study authors conclude that mosquitos are adapting for persistence in a northern climate.[55] Zika virus appears to be contagious via mosquitoes for around a week after infection. The virus is thought to be infectious for a longer period of time after infection (at least 2 weeks) when transmitted via semen.[56][57]
Research into its ecological niche suggests that Zika may be influenced to a greater degree by changes in precipitation and temperature than dengue, making it more likely to be confined to tropical areas. However, rising global temperatures would allow for the disease vector to expand its range further north, allowing Zika to follow.[58]
Zika can be transmitted from men and women to their sexual partners; most known cases involve transmission from symptomatic men to women.[39][59][60] As of April 2016, sexual transmission of Zika has been documented in six countries – Argentina, Australia, France, Italy, New Zealand, and the United States – during the 2015 outbreak.[14] ZIKV can persist in semen for several months, with viral RNA detected up to one year.[61] The virus replicates in the human testis, where it infects several cell types including testicular macrophages, peritubular cells and germ cells, the spermatozoa precursors.[62] Semen parameters can be altered in patients for several weeks post-symptoms onset, and spermatozoa can be infectious.[63] Since October 2016, the CDC has advised men who have traveled to an area with Zika should use condoms or not have sex for at least six months after their return as the virus is still transmissible even if symptoms never develop.[64]
Zika virus can spread by vertical (or "mother-to-child") transmission, during pregnancy or at delivery.[12][65] An infection during pregnancy has been linked to changes in neuronal development of the unborn child.[66] Severe progressions of infection have been linked to the development of microcephaly in the unborn child, while mild infections potentially can lead to neurocognitive disorders later in life.[67][68][69] Congenital brain abnormalities other than microcephaly have also been reported after a Zika outbreak.[70] Studies in mice have suggested that maternal immunity to dengue virus may enhance fetal infection with Zika, worsen the microcephaly phenotype and/or enhance damage during pregnancy, but it is unknown whether this occurs in humans.[71][72]
As of April 2016, two cases of Zika transmission through blood transfusions have been reported globally, both from Brazil,[40] after which the US Food and Drug Administration (FDA) recommended screening blood donors and deferring high-risk donors for 4 weeks.[73][74] A potential risk had been suspected based on a blood-donor screening study during the French Polynesian Zika outbreak, in which 2.8% (42) of donors from November 2013 and February 2014 tested positive for Zika RNA and were all asymptomatic at the time of blood donation. Eleven of the positive donors reported symptoms of Zika fever after their donation, but only three of 34 samples grew in culture.[75]
Zika virus replicates in the mosquito's midgut epithelial cells and then its salivary gland cells. After 5–10 days, the virus can be found in the mosquito's saliva. If the mosquito's saliva is inoculated into human skin, the virus can infect epidermal keratinocytes, skin fibroblasts in the skin and the Langerhans cells. The pathogenesis of the virus is hypothesized to continue with a spread to lymph nodes and the bloodstream.[21][76] Flaviviruses replicate in the cytoplasm, but Zika antigens have been found in infected cell nuclei.[77]
The viral protein numbered NS4A can lead to small head size (microcephaly) because it disrupts brain growth by hijacking a pathway which regulates growth of new neurons.[78] In fruit flies, both NS4A and the neighboring NS4B restrict eye growth.[79]
Zika fever (also known as Zika virus disease) is an illness caused by Zika virus.[80] Around 80% of cases are estimated to be asymptomatic, though the accuracy of this figure is hindered by the wide variance in data quality, and figures from different outbreaks can vary significantly.[81] Symptomatic cases are usually mild and can resemble dengue fever.[80][82] Symptoms may include fever, red eyes, joint pain, headache, and a maculopapular rash.[80][83][84] Symptoms generally last less than seven days.[83] It has not caused any reported deaths during the initial infection.[82] Infection during pregnancy causes microcephaly and other brain malformations in some babies.[12][13] Infection in adults has been linked to Guillain–Barré syndrome (GBS) and Zika virus has been shown to infect human Schwann cells.[82][85]
Diagnosis is by testing the blood, urine, or saliva for the presence of Zika virus RNA when the person is sick.[80][83] In 2019, an improved diagnostic test, based on research from Washington University in St. Louis, that detects Zika infection in serum was granted market authorization by the FDA.[86]
Prevention involves decreasing mosquito bites in areas where the disease occurs, and proper use of condoms.[83][87] Efforts to prevent bites include the use of DEET or picaridin - based insect repellent, covering much of the body with clothing, mosquito nets, and getting rid of standing water where mosquitoes reproduce.[80] There is no vaccine.[83] Health officials recommended that women in areas affected by the 2015–2016 Zika outbreak consider putting off pregnancy and that pregnant women not travel to these areas.[83][88] While no specific treatment exists, paracetamol (acetaminophen) and rest may help with the symptoms.[83] Admission to a hospital is rarely necessary.[82]
It is advised, for an affected person with the zika virus, to drink a lot of water to stay hydrated, to lie down, and to treat the fever and agony with liquid solutions; taking drugs like acetaminophen or paracetamol helps to relieve fever and pain. Referring to the US CDC it is not recommended to take anti-inflammatory and non-steroid drugs like aspirin for example.[89] If the patient affected is already taking treatment for another medical condition it is advisable to inform your attending physician before taking any other drug or additional treatment;[90]
The World Health Organization has suggested that priority should be to develop inactivated vaccines and other nonlive vaccines, which are safe to use in pregnant women.[91]
As of March 2016, 18 companies and institutions were developing vaccines against Zika, but they state a vaccine is unlikely to be widely available for about 10 years.[91][92]
In June 2016, the FDA granted the first approval for a human clinical trial for a Zika vaccine.[93] In March 2017, a DNA vaccine was approved for phase-2 clinical trials. This vaccine consists of a small, circular piece of DNA, known as a plasmid, that expresses the genes for the Zika virus envelope proteins. As the vaccine does not contain the full sequence of the virus, it cannot cause infection.[94] As of April 2017, both subunit and inactivated vaccines have entered clinical trials.[95]


The virus was first isolated in April 1947 from a rhesus macaque monkey placed in a cage in the Ziika Forest of Uganda, near Lake Victoria, by the scientists of the Yellow Fever Research Institute.[99] A second isolation from the mosquito A. africanus followed at the same site in January 1948.[100] When the monkey developed a fever, researchers isolated from its serum a "filterable transmissible agent" which was named Zika in 1948.[101]
Zika was first known to infect humans from the results of a serological survey in Uganda, published in 1952.[102] Of 99 human blood samples tested, 6.1% had neutralizing antibodies. As part of a 1954 outbreak investigation of jaundice suspected to be yellow fever, researchers reported isolation of the virus from a patient,[103] but the pathogen was later shown to be the closely related Spondweni virus.[104] Spondweni was also determined to be the cause of a self-inflicted infection in a researcher reported in 1956.[105]
Subsequent serological studies in several African and Asian countries indicated the virus had been widespread within human populations in these regions.[101] The first true case of human infection was identified by Simpson in 1964,[106] who was himself infected while isolating the virus from mosquitoes.[101] From then until 2007, there were only 13 further confirmed human cases of Zika infection from Africa and Southeast Asia.[107] A study published in 2017 showed that the Zika virus, despite only a few cases were reported, has been silently circulated in West Africa for the last two decades when blood samples collected between 1992 and 2016 were tested for the ZIKV IgM antibodies.[108]
In April 2007, the first outbreak outside of Africa and Asia occurred on the island of Yap in the Federated States of Micronesia, characterized by rash, conjunctivitis, and arthralgia, which was initially thought to be dengue, chikungunya, or Ross River disease.[109] Serum samples from patients in the acute phase of illness contained RNA of Zika. There were 49 confirmed cases, 59 unconfirmed cases, no hospitalizations, and no deaths.[110]
After October 2013 Oceania's first outbreak showed an estimated 11% population infected for French Polynesia that also presented with Guillain–Barre syndrome (GBS). The spread of ZIKV continued to New Caledonia, Easter Island, and the Cook Islands and where 1385 cases were confirmed by January 2014. During the same year, Easter Island acknowledged 51 cases. Australia began seeing cases in 2012. Research showed it was brought by travelers returning from Indonesia and other infected countries. New Zealand also experienced infections rate increases through returning foreign travelers. Oceania countries experiencing Zika today are New Caledonia, Vanuatu, Solomon Islands, Marshall Islands, American Samoa, Samoa, and Tonga.[111]
Between 2013 and 2014, further epidemics occurred in French Polynesia, Easter Island, the Cook Islands, and New Caledonia.[4]

There was an epidemic in 2015 and 2016 in the Americas. The outbreak began in April 2015 in Brazil, and spread to other countries in South America, Central America, North America, and the Caribbean. In January 2016, the WHO said the virus was likely to spread throughout most of the Americas by the end of the year;[112] and in February 2016, the WHO declared the cluster of microcephaly and Guillain–Barré syndrome cases reported in Brazil – strongly suspected to be associated with the Zika outbreak – a Public Health Emergency of International Concern.[6][113][114][115] It was estimated that 1.5 million people were infected by Zika in Brazil,[116] with over 3,500 cases of microcephaly reported between October 2015 and January 2016.[117]
A number of countries issued travel warnings, and the outbreak was expected to significantly impact the tourism industry.[6][118] Several countries have taken the unusual step of advising their citizens to delay pregnancy until more is known about the virus and its impact on fetal development.[20] With the 2016 Summer Olympics hosted in Rio de Janeiro, health officials worldwide voiced concerns over a potential crisis, both in Brazil and when international athletes and tourists returned home and possibly would spread the virus. Some researchers speculated that only one or two tourists might be infected during the three-week period, or approximately 3.2 infections per 100,000 tourists.[119] In November 2016, the World Health Organization declared that Zika virus was no longer a global emergency while noting that the virus still represents "a highly significant and a long-term problem".[120]
As of August 2017 the number of new Zika virus cases in the Americas had fallen dramatically.[121]
On May 15, 2017, three cases of Zika virus infection in India were reported in the state of Gujarat.[122][123] By late 2018, there had been at least 159 cases in Rajasthan and 127 in Madhya Pradesh.[124]
In July 2021, the first case of Zika virus infection in the Indian state of Kerala was reported. After the first confirmed case, 19 other people who had previously presented symptoms were tested, and 13 of those had positive results, showing that Zika had been circulating in Kerala since at least May 2021.[125] By August 6th 2021, there had been 65 reported cases in Kerala.[126]
On October 22, 2021, an officer in the Indian Air Force in Kanpur tested positive for Zika virus, making it the first reported case in the Indian state of Uttar Pradesh.[127]
On 22 March 2016, Reuters reported that Zika was isolated from a 2014 blood sample of an elderly man in Chittagong in Bangladesh as part of a retrospective study.[128] Zika is also occurring in Tanzania as of 2016.[129]
Between August and November 2016, 455 cases of Zika virus infection were confirmed in Singapore.[130][131]
In 2017, Angola reported two cases of Zika fever.[132]
{{cite journal}}: CS1 maint: DOI inactive as of December 2022 (link) ![]() This article incorporates public domain material from websites or documents of the Centers for Disease Control and Prevention.
This article incorporates public domain material from websites or documents of the Centers for Disease Control and Prevention.
Zika virus (ZIKV; pronounced /ˈziːkə/ or /ˈzɪkə/) is a member of the virus family Flaviviridae. It is spread by daytime-active Aedes mosquitoes, such as A. aegypti and A. albopictus. Its name comes from the Ziika Forest of Uganda, where the virus was first isolated in 1947. Zika virus shares a genus with the dengue, yellow fever, Japanese encephalitis, and West Nile viruses. Since the 1950s, it has been known to occur within a narrow equatorial belt from Africa to Asia. From 2007 to 2016, the virus spread eastward, across the Pacific Ocean to the Americas, leading to the 2015–2016 Zika virus epidemic.
The infection, known as Zika fever or Zika virus disease, often causes no or only mild symptoms, similar to a very mild form of dengue fever. While there is no specific treatment, paracetamol (acetaminophen) and rest may help with the symptoms. As of April 2019, no vaccines have been approved for clinical use, however a number of vaccines are currently in clinical trials. Zika can spread from a pregnant woman to her baby. This can result in microcephaly, severe brain malformations, and other birth defects. Zika infections in adults may result rarely in Guillain–Barré syndrome.
In January 2016, the United States Centers for Disease Control and Prevention (CDC) issued travel guidance on affected countries, including the use of enhanced precautions, and guidelines for pregnant women including considering postponing travel. Other governments or health agencies also issued similar travel warnings, while Colombia, the Dominican Republic, Puerto Rico, Ecuador, El Salvador, and Jamaica advised women to postpone getting pregnant until more is known about the risks.
El virus del Zika[1] (ZIKV) es un virus del género Flavivirus, de la familia Flaviviridae, grupo IV del orden sin clasificar[2] que se transmite por la picadura de mosquitos vectores del género Aedes.
En los seres humanos se produce la fiebre del Zika o enfermedad de Zika, la cual se conoce desde la década de 1950 como proveniente de la región ecuatorial que abarca de África a Asia. Su nombre proviene del bosque Zika, cerca de Entebbe (en Uganda), donde se aisló por primera vez este virus, en 1947.[3]
En 2014 el virus se propagó al este a través del océano Pacífico hacia la Polinesia Francesa, y después hacia la isla de Pascua para llegar en 2015 y 2016 a América Central, el Caribe y América del Sur, donde el brote epidémico del Zika ha alcanzado niveles pandémicos.[4][5] La enfermedad produce síntomas similares a formas leves de dengue,[6] su tratamiento consiste básicamente en el reposo,[7] y en la actualidad no existen medicamentos o vacunas para su prevención.[7] La fiebre del Zika está relacionada con otras enfermedades similares, como la fiebre amarilla y la fiebre del Nilo Occidental, las cuales también son producidas por otros Flavivirus transmitidos por mosquitos.[6] Hay vínculo entre la fiebre del Zika y la microcefalia en recién nacidos de madres infectadas como sucedió en el año 2016 en Brasil.[8][9]
Existen dos linajes de virus del Zika, el linaje africano y el linaje asiático.[10] Algunos estudios filogenéticos indican que el virus que está expandiéndose por el continente americano está más estrechamente relacionado con cepas provenientes de la Polinesia Francesa.[10] Ya se han publicado las secuencias completas del genoma del virus.[11] Algunos estudios preliminares de estos hallazgos demuestran un posible cambio en el funcionamiento del codón de la proteína no estructural 1, lo cual podría aumentar la tasa de replicación viral en humanos.[12]
Con el objetivo inicial de estudiar el ciclo silvestre del virus de la fiebre amarilla, en el año 1946 se localizó un grupo centinela de monos Rhesus en el bosque de Zika, cerca de Entebbe, la capital de Uganda, en una zona infestada por mosquitos de la especie Aedes africanus. Se tomaron muestras de sangre de uno de los monos que presentó un pico de fiebre, las que fueron inyectadas en ratones por vía intraperitoneal e intracerebral con el fin de aislar e identificar al agente causal del cuadro febril. Al virus aislado del cerebro de los ratones inoculados con las muestras de sangre por vía intracerebral se lo denominó Zika. Posteriormente, en enero de 1948, se efectuó una captura de mosquitos en el mismo bosque, cerca del área donde se había efectuado el aislamiento original en monos, detectándose la presencia del mismo virus en los extractos preparados a partir de ejemplares de Aedes africanus. Más adelante, en la misma región, se efectuaron nuevos aislamientos en mosquitos en 1958, y entre 1962 y 1963.[13][14]
El primer caso clínico de infección humana adjudicada al virus Zika se describió en 1952 en Nigeria, en una niña de 10 años que presentaba un cuadro de fiebre y cefalea. Al mismo tiempo que se aisló el virus que infectó a la niña, se presentaron dos hombres con ictericia transitoria y anticuerpos séricos contra el mismo agente viral, el cual fue identificado inicialmente como la cepa Chuku del virus Zika[15]. Sin embargo, estudios posteriores demostraron que la cepa Chuku pertenecía en realidad a una especie viral diferente, aunque estrechamente relacionada con Zika, el virus Spondweni. Boletín de la Organización Mundial de la Salud 2016;94:711-711A. Actualmente ambos virus, Zika y Spondweni, que producen cuadros clínicos prácticamente indistinguibles, son considerados como especies diferentes.
Mientras no se han registrado infecciones por virus Spondweni fuera del ámbito del África sub-sahariana (Boletín de la Organización Mundial de la Salud 2016;94:711-711A), el virus Zika se ha diseminado fuera del continente africano, primero hacia la Micronesia (2007), luego a la Polinesia francesa (2013-2014), y finalmente a Sudamérica, América Central y el Caribe, donde emergió con un brote epidémico de gran magnitud entre 2015 y 2016. Actualmente, el virus se ha diseminado por todo el planeta, excediendo el ámbito geográfico de dispersión de los mosquitos vectores, debido a su capacidad de transmitirse directamente entre humanos por vía sexual.[16][17]
El virión de Zika posee un genoma de ARN monocatenario, no segmentado, con sentido positivo y de un tamaño de 10.794 nt. El genoma está incluido en una cápside de simetría de tipo icosaédrico, constituida por una única subunidad polipeptídica, la proteína C. En la envoltura de la partícula viral inmadura se encuentra la proteína precursora prM, que mediante proteólisis se transforma en la proteína M del virión maduro. La glicoproteína E también se localiza en la envoltura, formando dímeros que, en el virión maduro, se ubican de forma paralela a la membrana lipídica, adoptando una simetría de tipo icosaédrica. El virión maduro tiene forma esférica y un tamaño aproximado de 50 nm.[18]
El genoma del virus Zika contiene un único marco de lectura abierto (ORF), flanqueado entre regiones 3’ y 5’ no codificantes. El extremo 5 'del genoma tiene una estructura de tipo “cap”, cuya función es promover su traducción inmediata luego del desnudamiento. Por otro lado, el extremo 3' no está poliadenilado, pero forma una estructura de bucle con propiedades regulatorias de la producción de ARNs funcionales no codificantes. El genoma se traduce en una única poliproteína, que posteriormente se escinde por acción de proteasas virales y celulares, lo que resulta en la producción de siete proteínas no estructurales, y las tres estructurales mencionadas anteriormente, C, prM/M y E. Las proteínas no estructurales (NS1, NS2A, NS2B, NS3, NS4A, NS4B y NS5) participan en la replicación, el ensamblaje de los viriones y el antagonismo de la respuesta innata de las células hospederas. La proteína NS5 presenta actividad de ARN polimerasa. Por otro lado, las proteínas estructurales forman la cápside (C), la matriz de la envoltura (M, derivada de la proteólisis del precursor prM) y la envoltura (glicoproteína E, involucrada en la adsorción y penetración virales).[19][20] Se ha descripto que, durante su replicación, los flavivirus como el virus Zika producen al menos dos ARN funcionales no codificantes: el ARN subgenómico de flavivirus (sfARN) y un posible miARN (KUN-miR -1). La formación de sfARN se produce a través de la degradación incompleta del ARN genómico por parte de la 5’-3’ exoribonucleasa-1 celular (XRN1) . El sfARN es esencial para la patogenicidad ya que se ha demostrado que su acumulación dentro de las células infectadas influye en el ciclo de vida de los flavivirus al menos de 3 formas distintas : (i) antagoniza la señalización inmune innata del huésped y, por lo tanto, subvierte la defensa del mismo ; (ii) inhibe la actividad de XRN1 y altera la homeostasis del ARNm del huésped ; y (iii) interactúa directamente con el complejo de replicación viral (RC) para modular su actividad. El segundo ARN no codificante funcional, KUN-miR-1, facilita la replicación del virus en mosquitos.[18]
El ciclo de replicación del virus Zika es similar al de otros virus del mismo género Flavivirus. El virión se une a los receptores de la membrana de la célula hospedera a través de la glicoproteína E de la envoltura, que induce la endocitosis del virión. A continuación, luego de la acidificación del endosoma, se produce la fusión de la envoltura del virus con la membrana endosomal, la nucleocápside se desintegra y el genoma del virus se libera en el citoplasma. El genoma es transportado a los ribosomas, donde se traduce en la poliproteína que se escinde co- y post-traduccionalmente en las 10 proteínas citadas precedentemente.
El genoma del Virus Zika se replica a través de la transcripción a un intermediario de ARN simple cadena de polaridad negativa en el citoplasma de la célula, en una reacción catalizada por la ARN polimerasa viral. Luego de esa primera transcripción se inducen evaginaciones del retículo endoplasmático, que dan lugar a paquetes de vesículas, en las cuales el ARN de polaridad negativa se transcribe al ARN viral de polaridad positiva por acción de la ARN polimerasa viral. Estas vesículas reclutan las proteínas del virión, que luego son transportadas, junto con el genoma viral, al aparato de Golgi en donde se ensamblarán para luego ser liberados por exocitosis, previa maduración del virión por proteólisis de prM.[21]
Numerosos estudios sugieren que tanto las proteínas estructurales, como algunas proteínas no estructurales, son responsables de los diversos efectos citopáticos observados en las células infectadas por el virus Zika.[22] La expresión de estas proteínas restringe la proliferación celular, provocando la hipertrofia inducida o el estrés oxidativo que conducen a la muerte celular. En este sentido, se ha descripto que la expresión de prM se asocia al bloqueo del ciclo celular en G1, mientras que C, M, E y NS4A bloquean el ciclo en la etapa G2/M. Además, como consecuencia de la replicación viral, el aparato de Golgi y el retículo endoplasmático de las células infectadas aparecen alterados. La morfología nuclear también se modifica para formar una estructura en forma de riñón debido a la acumulación de retículo endoplasmático.[23]
Se cree que la patogénesis viral comienza con la infección de las células dendríticas cercanas al sitio de la inoculación, seguido por la diseminación a los nódulos linfáticos y el torrente sanguíneo.[24] Generalmente, los Flavivirus se replican en el citoplasma, pero se han encontrado antígenos de virus del Zika dentro del núcleo celular.[25]

El virus del Zika es transmitido por mosquitos con actividad diurna y ha sido aislado a partir de varias especies en el género Aedes, como el A. aegypti, además de mosquitos arborícolas como el A. africanus, A. apicoargenteus, A. furcifer, A. hensilli, A. luteocephalus, y A. vitattus. Los estudios muestran que el periodo de incubación extrínseco en los mosquitos es aproximadamente de 10 días.[26] Los huéspedes vertebrados del virus son principalmente monos y seres humanos.[27]
El potencial del riesgo de infección con el virus del Zika puede estar limitado a la distribución de las especies de mosquitos que lo transmiten (su vector epidemiológico). La distribución mundial del portador más conocido del virus Zika, el Aedes aegypti, se está expandiendo debido al comercio global y los viajes.[28] La distribución del Aedes aegypti es ahora la más extensa jamás registrada, prácticamente en todos los continentes, incluidas América del Norte y la periferia de Europa.[29]
En 2009, Brian Foy, un biólogo de la Universidad Estatal de Colorado en los Estados Unidos, transmitió sexualmente el virus del Zika a su esposa. Foy había visitado Senegal para estudiar las poblaciones de mosquitos, y le picaron en varias ocasiones. Pocos días después de regresar a los Estados Unidos, contrajo fiebre del Zika, pero no antes de tener relaciones sexuales sin protección con su esposa. Después de esto, ella también mostraría los síntomas de la infección, incluso fotosensibilidad. Foy es la primera persona de la que se sabe que transmitió por contacto sexual un virus que requiere ser transportado por vectores a otro ser humano.[30][31]
En 2015, se detectó el ARN del virus del Zika en el líquido amniótico de dos fetos, lo que indica que habría cruzado la placenta y podría causar la transmisión vertical de la enfermedad de una madre a su hijo no nato.[32] El 20 de enero del 2016, científicos del estado de Paraná en Brasil detectaron material genético del virus del Zika en la placenta de una mujer que abortó a su feto debido a microcefalia, lo cual confirma que el virus es capaz de cruzar la barrera placentaria.[33]
Los síntomas más comunes de la infección con el virus incluyen dolores de cabeza leves, eflorescencia o erupciones maculopapulares, fiebre, malestar general, conjuntivitis y dolores articulares. El primer caso bien documentado por infección del virus del Zika se describió en 1964; comenzó con un dolor de cabeza leve y progresó hasta convertirse en un sarpullido maculopapular junto con fiebre y dolor de espalda. En dos días, el sarpullido comenzó a disminuir y al tercer día la fiebre cedió para solo quedar las erupciones. La fiebre del Zika se considera una enfermedad relativamente leve y limitada, y solo 1 de cada 5 personas desarrollarán los síntomas sin llegar a ser fatal, aunque el verdadero potencial como agente viral causante de enfermedad es desconocido.[26]
No existen vacunas o medicamentos preventivos para el virus del Zika. Los síntomas pueden ser tratados con analgésicos como el paracetamol, ya que otros AINES como la aspirina solo deberían ser utilizados tras descartar infección por dengue u otros Flavivirus, con el fin de reducir el riesgo de sangrado.[34]
Durante la epidemia en la Polinesia Francesa, se confirmaron 73 casos de síndrome de Guillain–Barré y otros padecimientos neurológicos, y se sospecha que podrían ser complicaciones del virus, aunque no hay estudios que lo confirmen.[27]
La microcefalia es la degeneración o malformación del cerebro que determina el nacimiento de niños con una cabeza de tamaño más pequeño que el normal y que en ocasiones provoca la muerte a los 10 días de vida. En diciembre del 2015, el Centro Europeo para la Prevención y Control de Enfermedades (ECDC) publicó un aviso sobre la posible asociación del virus del Zika con microcefalia congénita.[35] Los datos sugieren que en los fetos de las mujeres infectadas por el virus durante el primer trimestre del embarazo existe un riesgo alto de microcefalia;[36] otras investigaciones indican que además de ese síndrome este tipo de transmisión vertical podría causar daño cerebral.[37][38]
Según pruebas realizadas con ratones, Uraki y colaboradores, afirman en 2017[39] que el virus disminuye los niveles de testosterona y reduce significativamente el tamaño de los testículos.[40][41]
En la actualidad, existen vacunas efectivas contra muchos Flavivirus. Por ejemplo, las vacunas contra la fiebre amarilla, la encefalitis japonesa y la encefalitis transmitida por garrapatas se introdujeron en la década de 1930, mientras que la vacuna contra el dengue lo ha sido recientemente.[42][43]
Los trabajos hacia el desarrollo de una vacuna contra el virus del Zika ya habrían comenzado, según el doctor Anthony Fauci, director del Instituto Nacional de Alergia y Enfermedades Infecciosas de los Estados Unidos (NIAID).[44] Los investigadores del NIAID ya han tenido experiencia previa al trabajar en vacunas contra enfermedades similares como el virus del Nilo Occidental, el virus chikungunya y el dengue.[44] El 2017 se informó de buenas resultados en estudios preclínicos utilizando vacunas de ARN mensajero.[45]
El tiempo necesario para desarrollar una vacuna efectiva, certificarla y ponerla en producción es largo y complejo. Los primeros pasos se llevan a cabo en el laboratorio e incluyen pruebas en animales, ensayos clínicos y las licencias de aplicación y aprobación requeridas.[46] Se estima que podría llevar al menos unos 10 a 12 años el tener una vacuna efectiva contra el virus del Zika disponible para su uso.[47]
|número-autores= (ayuda) El virus del Zika (ZIKV) es un virus del género Flavivirus, de la familia Flaviviridae, grupo IV del orden sin clasificar que se transmite por la picadura de mosquitos vectores del género Aedes.
En los seres humanos se produce la fiebre del Zika o enfermedad de Zika, la cual se conoce desde la década de 1950 como proveniente de la región ecuatorial que abarca de África a Asia. Su nombre proviene del bosque Zika, cerca de Entebbe (en Uganda), donde se aisló por primera vez este virus, en 1947.
En 2014 el virus se propagó al este a través del océano Pacífico hacia la Polinesia Francesa, y después hacia la isla de Pascua para llegar en 2015 y 2016 a América Central, el Caribe y América del Sur, donde el brote epidémico del Zika ha alcanzado niveles pandémicos. La enfermedad produce síntomas similares a formas leves de dengue, su tratamiento consiste básicamente en el reposo, y en la actualidad no existen medicamentos o vacunas para su prevención. La fiebre del Zika está relacionada con otras enfermedades similares, como la fiebre amarilla y la fiebre del Nilo Occidental, las cuales también son producidas por otros Flavivirus transmitidos por mosquitos. Hay vínculo entre la fiebre del Zika y la microcefalia en recién nacidos de madres infectadas como sucedió en el año 2016 en Brasil.
Existen dos linajes de virus del Zika, el linaje africano y el linaje asiático. Algunos estudios filogenéticos indican que el virus que está expandiéndose por el continente americano está más estrechamente relacionado con cepas provenientes de la Polinesia Francesa. Ya se han publicado las secuencias completas del genoma del virus. Algunos estudios preliminares de estos hallazgos demuestran un posible cambio en el funcionamiento del codón de la proteína no estructural 1, lo cual podría aumentar la tasa de replicación viral en humanos.
Zika viirus(Zika virus; lüh ZIKV) on viiruseliik Flaviviridae sugukonnas.
Zika viiruse klassifikatsioon ei ole lõplik, osade allikate kohaselt on viiruse alamliigiks Spondweni virus (SPOV)[1], kes algselt identfitseeriti Zika viirusena, kuid teiste autorite arvates moodustavad nimetatud viirused viiruse perekonna Flavivirus klaadi.
Zika viirus on üheahelaline RNA-viirus (ssRNA)[2], lipiidse kestaga ja diameetriga 18-45 nm.
Zika viirusel on kaks geneetilist varianti: Aafrika ja Aasia.[3]
Hiljutiste Zika-viirushaiguste põhjustajaks peetakse viiruse Aasia liini.[4]
Looduslikult levib Zika viirus teatud sääseliikide (Aedes aegypti ja Aedes albopictus)[5] hammustuse vahendusel ja võib inimestel esile kutsuda sääselevitatava viiruspalaviku Zika-viirusinfektsiooni.
Zika-viirusinfektsioon on koondnimetus peamiselt inimestel ja mitmetel ahviliikidel tuvastatud nakkavate ja palavikuga kulgevate infektsioonhaiguste kohta, mida põhjustavad Zika viiruse mitmed tüved.
Zika viiruse esimene teadaolev kandja oli tõenäoliselt Ugandas paiknevas Zika metsas puuri asetatud reesusmakaak (Macaca mulatta). Rhesus 766 viidi laboratooriumi ja tema seerumit inokuleeriti intratserebraalselt hiirtesse - 10 päeva möödudes haigestusid ka nemad; nende peaajust eraldati 'nakkuslik element', mis nimetati Zika viiruseks. 1948. aastal eraldati ZIKV ka samas metsas elavatelt Aedes africanus sääskedelt. Seroloogilised uuringud näitasid, et viirus võib nakatada ka inimesi.[6]
Zika viirus(Zika virus; lüh ZIKV) on viiruseliik Flaviviridae sugukonnas.
Zika birusa (ZIKV) gizakia eta primate batzuk infektatzen dituen birusa da. Flaviviridae familian sailkatutakoa, zika sukarra eragiten du. Birusa 1947an deskribatu zen estreinakoz, Ugandako tximino batean (Zika eskualdean).
Flavibirusak RNA birusak dira: bere material genetikoa polaritate positiboko RNA kate bakarrez osatuta dago. Horren gainetik kapside ikosaedrikoa dute.
Zika birusak senidetasuna konpartitzen du denge eta sukar horiaren birusekin. Hirurak eltxo beraren ziztadaren bitartez (Aedes generoko eltxoaren bitartez) transmititzen dira.
Ugandako makako batean aurkitu zuten lehenbizikoz zientzialariek zika birusa, 1947an. 1952an Ugandan eta Tanzanian birus honen lehenengo giza infektatuak agertu ziren. Birusak Afrika tropikalean urte luzeetan iraun zuen, harik eta 2007an Asiako Mikronesian agertu arte. 2015an, aldiz, lehenengo kasuak agertu ziren Amerikan ere (Brasilen), eta kontinente honetan hedatzen ari da orain (Erdi eta Hego Amerikan zehar).
Flaviviridae familiako birus guztiak Aedes eltxoaren ziztadaren bidez transmititzen dira. Aedes aegypti da gaitzaren ohiko bektorea. Zika sukarraren prebentzioa eltxo bektorearen kontrolean eta intsektizida eta uxagarrien erabileran datza. Epidemiologoen ustez, baina, eltxo bektorearen erabateko suntsipena oso korapilatsua da, ia ezinezkoa, Aedesek aparteko moldagarritasuna izaten baitu.
Zika sukarra, orokorrean, gaixotasun arina da, egun gutxitan berez sendatzen dena. Infektatuen artean hiru laurdenek (%75-ak) ez dute inongo sintomarik garatzen, eta infekzioak ez die gaixotasunik eragiten.
Beste laurdenak, aldiz, sintoma arinak ditu: sukar txikia, larruazaleko erupzioa, artralgiak, buruko mina eta konjuntibitisa. Hainbat kasutan digestio-aparatua ere kaltetuta suertatzen da, gorakoak eta beherakoak agertuz.
Eskuarki arrisku maila txikikoa izan arren, zika birusaren infekzioak -kasu gutxi batzuetan- ondorio gaiztoak ekar ditzake: Guillain-Barré sindromea piztu, adibidez [1]. Bestalde, 2015eko Brasileko izurritean bertako osasun-agintariek birus honen infekzioa haur jaioberriaren mikrozefaliarekin lotu zuten. Antza, haurdun dauden emakumeengan birusak karena zeharkatuko luke eta kalte neurologiko larriak sortuko lituzke umekiarengan [2].
Oraingoz ez dago tratamendurik, ezta txertorik ere, gaitzari aurre egiteko.
Zika birusa (ZIKV) gizakia eta primate batzuk infektatzen dituen birusa da. Flaviviridae familian sailkatutakoa, zika sukarra eragiten du. Birusa 1947an deskribatu zen estreinakoz, Ugandako tximino batean (Zika eskualdean).
Zikavirus on keltakuumehyttysen välityksellä leviävä virus. Sen epäillään aiheuttavan ihmisissä sikiöiden kehityshäiriöitä ja Guillain-Barrén tautia, mutta yhteyttä ei ole vielä tieteellisesti vahvistettu.[1] Tauti on kuitenkin yleensä hyvin lievä.[2] Virus levisi loppuvuoden 2015 aikana nopeasti Latinalaisessa Amerikassa, ja samaan aikaan sitä esiintyi myös Afrikassa, osassa Aasiaa ja Ranskan Polynesiassa. Yhdysvaltain tartuntatautivirasto kehotti tällöin raskaana olevia matkailijoita varovaisuuteen näillä alueilla. Suomessa Terveyden ja hyvinvoinnin laitos kehotti matkustajia suojautumaan hyttysiltä Latinalaisessa Amerikassa liikuttaessa. [3]
Tapauksia todettiin myös Euroopassa, mutta ne olivat yleensä peräisin Etelä-Amerikasta.[4] Suomessa todettiin ensimmäinen zikavirustapaus kesäkuussa 2015. Kyseessä oli lieväoireinen, Malediiveiltä lähtöisin oleva tautitapaus.[5] Viruksen yleisin leviämistapa on tropiikissa elävän keltakuumehyttysen välityksellä, mutta myös ihmisestä toiseen tapahtuvia tartuntoja tunnetaan[6]. Virus on aiemminkin aiheuttanut epidemioita Aasiassa ja Afrikassa.[7]
Noin 80 prosenttia tartunnan saaneista on oireettomia. Tartunnan oireita ovat lievä kuume, lihaskipu ja silmätulehdukset. Vain harva joutuu sairaalahoitoon. Virus on vaarallinen raskaana oleville, sillä se saattaa aiheuttaa lapselle pienipäisyyttä ja kehitysvammaisuutta. Muille se on haitattomampi kuin kausi-influenssa.[8]
Virus eristettiin ensimmäisen kerran vuonna 1947 Ugandassa kuumeisesta reesusmakakista. Virus nimettiin löytöpaikan, Zika-nimisen metsän, mukaan.[8] Ihmisellä tartunta todettiin ensimmäistä kertaa Nigeriassa vuonna 1954.[2] Ensimmäinen epidemia-aalto havaittiin vuonna 2007 Micronesiassa Yapin atollilla, jolloin 180 ihmistä sai tartunnan. Vuonna 2013 Ranskan Polynesiassa oli epidemia. Vuoden 2015 toukokuussa zikavirus havaittiin Brasiliassa, minkä jälkeen se levisi Latinalaisessa Amerikassa epidemiaksi. Yhteys sikiöiden kehitysvaurioon havaittiin Brasiliassa marraskuussa 2015.[8][9]
Zikavirus on keltakuumehyttysen välityksellä leviävä virus. Sen epäillään aiheuttavan ihmisissä sikiöiden kehityshäiriöitä ja Guillain-Barrén tautia, mutta yhteyttä ei ole vielä tieteellisesti vahvistettu. Tauti on kuitenkin yleensä hyvin lievä. Virus levisi loppuvuoden 2015 aikana nopeasti Latinalaisessa Amerikassa, ja samaan aikaan sitä esiintyi myös Afrikassa, osassa Aasiaa ja Ranskan Polynesiassa. Yhdysvaltain tartuntatautivirasto kehotti tällöin raskaana olevia matkailijoita varovaisuuteen näillä alueilla. Suomessa Terveyden ja hyvinvoinnin laitos kehotti matkustajia suojautumaan hyttysiltä Latinalaisessa Amerikassa liikuttaessa.
Tapauksia todettiin myös Euroopassa, mutta ne olivat yleensä peräisin Etelä-Amerikasta. Suomessa todettiin ensimmäinen zikavirustapaus kesäkuussa 2015. Kyseessä oli lieväoireinen, Malediiveiltä lähtöisin oleva tautitapaus. Viruksen yleisin leviämistapa on tropiikissa elävän keltakuumehyttysen välityksellä, mutta myös ihmisestä toiseen tapahtuvia tartuntoja tunnetaan. Virus on aiemminkin aiheuttanut epidemioita Aasiassa ja Afrikassa.
Le virus Zika est l'agent infectieux à l'origine, chez l'homme, de l'infection à virus Zika. Il s'agit d'un virus à ARN monocaténaire de polarité positive, relevant donc du groupe IV de la classification Baltimore, et appartenant au genre Flavivirus. Il est notamment apparenté aux virus de la dengue, de la fièvre jaune, de l'encéphalite japonaise et du Nil occidental[3]. Il appartient au même sérogroupe que le virus Spondweni[4],[5].
Le nom du virus fait référence à la forêt de Zika, près d'Entebbe (Ouganda), où il a été isolé en 1947 sur un macaque rhésus avant d'être caractérisé en 1952 comme une nouvelle espèce virale[6]. Il existe en fait deux lignées de virus Zika, l'une originaire d'Afrique et l'autre d'Asie.
En février 2016, faisant suite à l'apparition de l'épidémie d'infections à virus Zika au Brésil, l'Organisation mondiale de la santé « a rendu l’avis que le groupe récent de cas de microcéphalie et d’autres troubles neurologiques signalés au Brésil, faisant suite à un regroupement similaire de cas en Polynésie française en 2014, constitue une urgence de santé publique de portée internationale (USPPI) »[7].
Il existe deux lignées de virus Zika, l'une originaire d'Afrique et l'autre d'Asie[8]. Des études phylogénétiques indiquent que le virus qui se propage sur le continent américain est identique à 89 % aux génotype africains mais est apparenté plus étroitement aux souches asiatiques qui ont circulé en Polynésie française au cours de l'épidémie de 2013-2014[9],[10]. La souche asiatique semble s'être différenciée aux alentours de 1928[11].
Les souches de virus Zika séquencées à Rio de Janeiro en 2016 (marquées d'un point noir ⬤ en haut de l'arbre) sont proches de celles identifiées en Polynésie française en 2013[12].
Ce virus enveloppé d'environ 50 nm de diamètre présente une capside icosaédrique recouverte d'une membrane et contenant l'ARN viral[13]. Il a un génome non segmenté long de 10 kilobases[14] qui code trois protéines structurelles et sept protéines non structurelles[15]. La séquence de l'ARN d'une souche de virus Zika issue de l'épidémie de 2013 en Polynésie française a ainsi montré un génome de 10 617 nucléotides avec un cadre de lecture ouvert de 10 272 nucléotides codant une polyprotéine clivée en les protéines suivantes[16] : protéine de capside C de 105 résidus d'acides aminés ; protéine de prémembrane prM de 187 résidus ; protéine d'enveloppe E de 505 résidus comprenant le motif de glycosylation de 154 résidus précédemment associé à la virulence ; et sept protéines non structurelles : NS1 de 352 résidus ; NS2A de 217 résidus ; NS2B de 139 résidus ; NS3 de 619 résidus, une hélicase[17] ayant une activité de protéase à sérine en complexe NS2B-NS3[18] ; NS4A de 127 résidus ; NS4B de 255 résidus ; NS5 de 904 résidus, une ARN polymérase ARN-dépendante[19].
L'une de ces protéines structurelles, la glycoprotéine d'enveloppe E, encapsule le virus et se lie à la membrane de l'endosome de la cellule hôte pour déclencher l'endocytose[20]. L'ARN viral forme une nucléocapside avec la protéine de capside C de 12 kDa. Cette nucléocapside est enveloppée dans une membrane dérivée de la membrane plasmique de la cellule hôte, modifiée avec deux glycoprotéines virales[21]. La réplication nécessite une ARN polymérase ARN-dépendante.
L'extrémité 5’ de l'ARN viral porte une coiffe tandis que l'extrémité 3’ est dépourvue de queue poly(A) mais forme une épingle à cheveux reconnue par l'exoribonucléase cellulaire XRN1 (en) qui la clive[13].
Représentation d'une capside de virus Zika[22] montrant les protéines de capside en jaune, orange et rouge-orangé pour mettre en évidence la symétrie icosaédrique. Les pointes couleur cyan sont des chaînes polyosidiques.
Coupe[22] d'un virion de virus Zika (à gauche) montrant les protéines d'enveloppe E représentées en rouge et les protéines de membrane M en magenta incluses dans la membrane lipidique en violet et interagissant avec les récepteurs membranaires à la surface des cellules en vert. Dans la capside, le génome d'ARN en jaune est lié aux protéines de capside C en orange.
Le virion a un diamètre ne dépassant pas 50 nm avec une capside à géométrie icosaédrique dont chaque face contient trois homodimères de la protéine d'enveloppe E[13], tandis que la protéine transmembranaire M se loge dans l'enveloppe virale et la protéine de capside C contient l'ARN viral.
Une étude a montré que six heures après l'infection de cellules par le virus Zika, les vacuoles et les mitochondries de ces cellules commencent à enfler. Ce gonflement devient suffisamment sévère pour déclencher la paraptose (en) des cellules. Cette forme de mort cellulaire programmée requiert l'expression de certains gènes.
Le virus Zika cible particulièrement les cellules de la peau[23] et les cellules souches neuronales[24], entraînant des malformations sévères chez le nouveau-né[25] et des atteintes neurologiques graves, comme le syndrome de Guillain-Barré[26].
La protéine IFITM3 (en) est une protéine transmembranaire des cellules capable de protéger ces dernières de l'infection virale en bloquant l'attachement du virus. Les cellules les plus sensibles à l'infection au virus Zika sont celles qui ont un faible taux de protéine IFITM3. Une fois les cellules infectées, le virus réorganise le réticulum endoplasmique en formant de grandes vacuoles, ce qui tue la cellule[27].
L'infection à virus Zika est une virose généralement asymptomatique avec quelques cas présentant des symptômes peu marqués évoquant la dengue[28],[29]. Parmi les symptômes de la maladie, on relève température, yeux rouges, douleurs articulaires, maux de tête, éruptions cutanées[28],[30],[31]. Ils se prolongent généralement moins d'une semaine et ne sont pas mortels[32], en revanche la transmission du virus de la femme enceinte à son fœtus est susceptible d'entraîner une microcéphalie et diverses autres malformations du cerveau chez le nouveau-né[33],[34], tandis qu'on peut observer un syndrome de Guillain-Barré chez l'adulte[32].
On peut contracter la maladie essentiellement par piqûre de moustiques du genre Aedes[30], mais elle peut également se transmettre sexuellement ainsi qu'éventuellement lors de transfusions sanguines[30],[35]. Les femmes enceintes peuvent transmettre le virus à leur bébé[33],[34]. Le virus peut encore être excrétée dans l'urine à taux élevés plus de 10 jours après le début de la maladie, après qu'on ne le trouve plus dans le sérum[36].
Le diagnostic est réalisé par prélèvement de sang, d'urine ou de salive pour y rechercher la présence d'ARN viral, ou pour rechercher des anticorps dans le sang chez les patients présentant les symptômes depuis plus d'une semaine[28],[30].
Le virus Zika est l'agent infectieux à l'origine, chez l'homme, de l'infection à virus Zika. Il s'agit d'un virus à ARN monocaténaire de polarité positive, relevant donc du groupe IV de la classification Baltimore, et appartenant au genre Flavivirus. Il est notamment apparenté aux virus de la dengue, de la fièvre jaune, de l'encéphalite japonaise et du Nil occidental. Il appartient au même sérogroupe que le virus Spondweni,.
Le nom du virus fait référence à la forêt de Zika, près d'Entebbe (Ouganda), où il a été isolé en 1947 sur un macaque rhésus avant d'être caractérisé en 1952 comme une nouvelle espèce virale. Il existe en fait deux lignées de virus Zika, l'une originaire d'Afrique et l'autre d'Asie.
En février 2016, faisant suite à l'apparition de l'épidémie d'infections à virus Zika au Brésil, l'Organisation mondiale de la santé « a rendu l’avis que le groupe récent de cas de microcéphalie et d’autres troubles neurologiques signalés au Brésil, faisant suite à un regroupement similaire de cas en Polynésie française en 2014, constitue une urgence de santé publique de portée internationale (USPPI) ».
O virus de Zika ou virus Zika (ZIKV, virus do bosque de Zika en Uganda) é un virus pertencente á familia Flaviviridae e ao xénero Flavivirus.
En humanos este virus causa inicialmente unha enfermidade leve chamada febre de Zika, Zika, ou doenza de/do Zika, transmitida por mosquitos, que se coñecía desde a década de 1950 como unha doenza propia dunha estreita área ecuatorial que se estendía desde África a Asia. Non obstante, en 2014, o virus espallouse máis cara ao leste a través do océano Pacífico e chegou á Polinesia Francesa, e despois á illa de Pascua e en 2015 alcanzou América Central, o Caribe e Suramérica, onde orixinou en 2015-2016 un brote que chegou ao nivel de pandemia.[1] O virus de Zika está relacionado cos virus causantes do dengue, febre amarela, encefalite xaponesa, e febre do Nilo occidental.[2] A doenza que causa é similar a unha forma suave do dengue,[2] que se trata principalmente gardando repouso,[3] e con calmantes e non pode ser previda con fármacos ou vacinas.[3] Hai unha moi posible ligazón entre a febre de Zika e a microcefalia en nenos neonatos que a adquiren por transmisión de nai a fillo,[4][5][6] e tamén con condicións neurolóxicas máis fortes en adultos infectados, incluíndo casos de síndrome de Guillain-Barré.[7]
Xunto con outros virus da súa familia, o virus de Zika é un virus con envoltura e icosaédrico cun xenoma de ARN monocatenario non segmentado e de sentido positivo. Está moi estreitamente relaciondao co virus Spondweni e é un dos dous virus situado no clado do virus Spondweni.[8][9]
O virus illouse por primeira vez en 1947 dun macaco rhesus que fora encerrado nunha gaiola e deixado no bosque de Zika en Uganda, preto do lago Vitoria, polos científicos do Instituto de investigación da febre amarela. Fíxose no mesmo lugar un segundo illamento do virus nun mosquito da especie Aedes africanus en 1948.[10][11] Cando o mencionado mono desenvolveu unha febre, os investigadores illaron do seu soro un axente transmisible que foi descrito definitivamente como o virus de Zika (Zika virus) en 1952. En 1968, foi illado por vez primeira de humanos en Nixeria.[12] De 1951 a 1981, houbo informes de probas de infeccións en humanos noutros países africanos, como a República Centroafricana, Exipto, Gabón, Serra Leoa, Tanzania, e Uganda, e tamén nalgúns países de Asia como India, Indonesia, Malaisia, Filipinas, Tailandia, e Vietnam.[12]
Hipotetízase que a patoxénese do virus empeza cunha infección das células dendríticas preto do sitio de inoculación, e seguidamente espállase aos ganglios linfáticos e ao torrente sanguíneo.[8] Os flavivirus xeralmente replícanse no citoplasma, pero os antíxenos do virus de Zika foron atopados no núcleo das células infectadas.[13]
Hai dúas liñaxes do virus de Zika, a liñaxe africana e a asiática.[14] Os estudos filoxenéticos indican que o virus espallado por América está moi probablemente relacionado coas cepas da Polinesia Francesa.[14] Publicáronse as secuencias xenómicas completas de virus Zika.[15] Recentes descubrimentos preliminares a partir de secuencias do virus atoparon un posible cambio nun codón da proteína non estrutural 1 do virus que pode incrementar a taxa de replicación viral en humanos.[16]
Debido á dimensión que alcanzou a epidemia de 2015-2016 as autoridades sanitarias dalgúns países recomendaron precaucións, especialmente a mulleres embarazadas, á hora de viaxar aos países máis afectados,[17][18][19][20][21] mentres que Colombia, República Dominicana, Ecuador, El Salvador, e Xamaica aconsellaron ás mulleres que pospuxeran o seu proxecto de quedaren preñadas ata que se saiba máis sobre os riscos para os fetos.[20][22]

O virus de Zika transmítese por medio de mosquitos que teñen actividade diúrna e foi illado de varias especies deles do xénero Aedes, como A. aegypti, e mosquitos arbóreos como A. africanus, A. apicoargenteus, A. furcifer, A. hensilli, A. luteocephalus, e A. vitattus. O período de incubación extrínseco nos mosquitos é de aproximadamente 10 días.[12] O virus de Zika pode transmitirse entre humanos por contacto sexual e pode tamén cruzar a placenta, e afectar aos fetos.
Os hóspedes vertebrados do virus son principalmente monos e humanos. Antes da epidemia de 2015-2016, que en realidade empezou en 2007, o virus de Zika "raramente causaba infeccións 'que se estendesen' recoñecidas en humanos, mesmo nas áreas enzoóticas".[7]
O risco social potencial do virus de Zika pode ser delimitado pola distribución das especies de mosquitos que o transmiten (o seu vector epidemiolóxico). A distribución global do portador máis citado do virus Zika, A. aegypti, está expandíndose debido ao comercio e viaxes globais.[23] A distribución de A. aegypti é agora a máis ampla da que se ten rexistro, xa que está presente en todos os continentes incluíndo a periferia de Europa e en Norteamérica.[24]
Fixéronse informes recentes sobre o espallamento do Zika en América Latina e o Caribe.[25] Os países e territorios que foron identificados pola Organización da Saúde Panamericana como zonas onde houbo unha "transmisión do virus de Zika local" son Barbados, Bolivia, Brasil, Colombia, República Dominicana, Ecuador, El Salvador, Güiana Francesa, Guadalupe, Guatemala, Güiana, Haití, Honduras, Martinica, México, Panamá, Paraguai, Puerto Rico, Saint Martin, Suriname e Venezuela.[26][27]
En 2009 acreditouse un caso de transmisión sexual do virus nun biólogo norteamericano que visitara Senegal e que de regreso transmitiu o virus á súa muller, a cal enfemou de Zika. Considérase que foi a primeira persoa que transmitiu por vía sexual un virus normalmente transmitido por insectos voadores.[28][29]
En 2015, detectouse o ARN do virus Zika no líquido amniótico de dous fetos, o que indicaba que cruzara a placenta e podía causar unha infección transmitida verticalmente de nai a fillo.[30] O 20 de xaneiro de 2016, científicos do estado de Paraná, Brasil, detectaron material xenético do virus de Zika na placenta dunha muller que sufrira un aborto debido á microcefalia do seu feto, o cal confirmaba que o virus pode atravesar a barreira placentaria.[31]
Aínda que existen vacinas efectivas contra varios flavivirus, non é así para o virus de Zika. Hai vacinas contra o virus da febra amarela, o da encefalie xaponesa e encefalite transitida por carrachas xa desde a década de 1930 e recentemente introduciuse a vacina contra o dengue.[32][33][34]
Porén, os traballos para obter unha vacina contra o virus de Zika aínda se iniciaron hai pouco, segundo Anthony Fauci, director do National Institute of Allergy and Infectious Diseases de EUA.[35] Os investigadores do Vaccine Research Center que traballan nesta vcina teñen unha ampla experiencia de traballo en vacinas para outros virus como o virus do Nilo occidental, o virus chikungunya e o do dengue.[35] Segundo algunhas previsións en 10 ou 12 anos podería dispoñerse dunha vacina efectiva contra o virus de Zika.[36]
Síntomas comúns das infeccións por este virus son dores de cabeza leves, erupción maculopapular, febre, malestar, conxuntivite e dor articular. O primeiro caso ben documentado de Zika foi descrito en 1964; empezou cunha dor de cabeza leve, e seguiu con erupción maculopapular, febre e dor de costas; despois, en dous días, a erupción empezou a diminuír, e en tres días, a febre cesou e só permaneceu a erupción. En xeral, a febre de Zika é unha doenza que adoita ser relativamente leve e de alcance limitado, da que só unha de cada cinco persoas afectadas chega a presentar síntomas, sen que haxa vítimas mortais, pero o seu verdadeiro potencial como axente viral descoñécese.[12]
En 2016, non hai vacina contra el nin fármacos preventivos. Os síntomas poden ser tratados con paracetamol (acetaminofén), mentres que a aspirina e outros antiinflamatorios non esteroideos só se deberían usar se foi descartado o dengue para así reducir o risco de hemorraxias.[37]
Nunha epidemia de zika na Polinesia Francesa, producíronse 73 casos de síndrome de Guillain–Barré e outras condicións neurolóxicas nunha poboación de 270.000 persoas, que poden ser resultado de complicacións por infección polo virus de Zika.[7]
En decembro de 2015, o Centro Europeo para a Prevención e Control de Doenzas sacou unha extensa actualización sobre a posible asociación do virus Zika coa microcefalia conxénita.[38] Os datos suxiren que os bebés neonatos paridos por nais que tiveran unha infección polo virus de Zika durante o primeiro trimestre de embarazo teñen un risco incrementado de padecer microcefalia.[39] En decembro de 2015 sospeitábase que unha infección transplacentaria do feto podía orixinar a microcefalia e danos cerebrais.[5][40] O ministro de Sanidade de Brasil confirmou despois a relación entre o virus Zika e a microcefalia.[4]
En 1947, científicos que investigaban a febre amarela situaron nunha gaiola un macaco rhesus no boque de Zika (zika significa 'descoidado' en idioma luganda), preto do Instituto de Investigación de Virus de África Occidental en Entebbe, Uganda. O mono desenvolveu unha febre, e os investigadores illaron do seu soro un axente transmisible, que en 1952 sería descrito como o virus de Zika.[11] Non se illou de humanos ata anos despois, en Nixeria. Desde entón ata 2007 os casos confirmados de infección por este virus foron raros e localizados en Asia e Sueste asiático.[41]
En 2007, deuse o primeiro brote fóra de África ou Asia na illa de Yap nos Estados Federados de Micronesia, que se caracterizou por producir erupcións, conxuntivite e artralxia, e inicialmente pensouse que se trataba de casos de dengue, de chikungunya, ou de doenza do río Ross.[42] Porén, as mostras do soro dos pacientes en fase aguda da doenza contiñan ARN do virus de Zika. Confirmáronse 49 casos, e contabilizáronse outros 59 casos non confirmados, e non houbo hospitalizacións nin falecementos.[43] Posteriormente houbo epidemias en Polinesia, illa de Pascua, illas Cook e Nova Caledonia.[41]
Desde abril de 2015, está tendo lugar un gran brote de virus Zika en América, que empezou en Brasil e que se espallou por moitos países de América do Sur e Central e o Caribe. En xaneiro de 2016, a CDC estadounidense emitiu unh alerta de nivel 2 para as viaxes por esas rexións onde se está a producir a transmisión do virus.[44] A CDC recomendou ás mulleres embarazadas consultar aos seus médicos antes de viaxar á zona.[45] Os gobernos ou axencias sanitarias de países como o Reino Unido,[19] Irlanda,[20] Nova Zelandia,[46] Canadá,[21] e a Unión Europea[21] fixeron advertencias similares pouco despois. En Colombia, o ministro de Sanidade recomendou evitar o embarazo durante oito meses, mentres que Ecuador, El Salvador e Xamaica fixeron tamén advertencias similares.[20][22]
En Brasil anunciáronse plans, para previr o espallamento do virus Zika durante os Xogos Olímpicos de Verán de 2016 de Río de Xaneiro.[21]
Segundo informou a CDC, as autoridades sanitarias brasileiras informaron de máis de 3.500 casos de micrfocefalia entre outubro de 2015 e xaneiro de 2016. Algúns dos nenos afectados presentaron un tipo grave de microcefalia e outros morreron. Aínda non se comprende ben o espectro completo de resultados que poderían estar asociados coa infección durante o embarazo e os factores que poderían incrementar o risco para o feto. Planéanse máis estudos para aprender máis sobre os riscos da infección polo virus Zika durante o embarazo.[47] Na rexión máis afectada de Brasil aproximadamente o 1 % dos neonatos son susceptibles de ter microcefalia.[48]
O virus de Zika ou virus Zika (ZIKV, virus do bosque de Zika en Uganda) é un virus pertencente á familia Flaviviridae e ao xénero Flavivirus.
En humanos este virus causa inicialmente unha enfermidade leve chamada febre de Zika, Zika, ou doenza de/do Zika, transmitida por mosquitos, que se coñecía desde a década de 1950 como unha doenza propia dunha estreita área ecuatorial que se estendía desde África a Asia. Non obstante, en 2014, o virus espallouse máis cara ao leste a través do océano Pacífico e chegou á Polinesia Francesa, e despois á illa de Pascua e en 2015 alcanzou América Central, o Caribe e Suramérica, onde orixinou en 2015-2016 un brote que chegou ao nivel de pandemia. O virus de Zika está relacionado cos virus causantes do dengue, febre amarela, encefalite xaponesa, e febre do Nilo occidental. A doenza que causa é similar a unha forma suave do dengue, que se trata principalmente gardando repouso, e con calmantes e non pode ser previda con fármacos ou vacinas. Hai unha moi posible ligazón entre a febre de Zika e a microcefalia en nenos neonatos que a adquiren por transmisión de nai a fillo, e tamén con condicións neurolóxicas máis fortes en adultos infectados, incluíndo casos de síndrome de Guillain-Barré.
Xunto con outros virus da súa familia, o virus de Zika é un virus con envoltura e icosaédrico cun xenoma de ARN monocatenario non segmentado e de sentido positivo. Está moi estreitamente relaciondao co virus Spondweni e é un dos dous virus situado no clado do virus Spondweni.
O virus illouse por primeira vez en 1947 dun macaco rhesus que fora encerrado nunha gaiola e deixado no bosque de Zika en Uganda, preto do lago Vitoria, polos científicos do Instituto de investigación da febre amarela. Fíxose no mesmo lugar un segundo illamento do virus nun mosquito da especie Aedes africanus en 1948. Cando o mencionado mono desenvolveu unha febre, os investigadores illaron do seu soro un axente transmisible que foi descrito definitivamente como o virus de Zika (Zika virus) en 1952. En 1968, foi illado por vez primeira de humanos en Nixeria. De 1951 a 1981, houbo informes de probas de infeccións en humanos noutros países africanos, como a República Centroafricana, Exipto, Gabón, Serra Leoa, Tanzania, e Uganda, e tamén nalgúns países de Asia como India, Indonesia, Malaisia, Filipinas, Tailandia, e Vietnam.
Hipotetízase que a patoxénese do virus empeza cunha infección das células dendríticas preto do sitio de inoculación, e seguidamente espállase aos ganglios linfáticos e ao torrente sanguíneo. Os flavivirus xeralmente replícanse no citoplasma, pero os antíxenos do virus de Zika foron atopados no núcleo das células infectadas.
Hai dúas liñaxes do virus de Zika, a liñaxe africana e a asiática. Os estudos filoxenéticos indican que o virus espallado por América está moi probablemente relacionado coas cepas da Polinesia Francesa. Publicáronse as secuencias xenómicas completas de virus Zika. Recentes descubrimentos preliminares a partir de secuencias do virus atoparon un posible cambio nun codón da proteína non estrutural 1 do virus que pode incrementar a taxa de replicación viral en humanos.
Debido á dimensión que alcanzou a epidemia de 2015-2016 as autoridades sanitarias dalgúns países recomendaron precaucións, especialmente a mulleres embarazadas, á hora de viaxar aos países máis afectados, mentres que Colombia, República Dominicana, Ecuador, El Salvador, e Xamaica aconsellaron ás mulleres que pospuxeran o seu proxecto de quedaren preñadas ata que se saiba máis sobre os riscos para os fetos.
Virus Zika (ZIKV) merupakan sejenis virus dari keluarga flaviviridae dan genus flavivirus yang disebarkan oleh nyamuk Aedes aegypti. Virus ini dapat menyebabkan sakit yang ringan kepada manusia yang dikenal sebagai demam Zika atau penyakit Zika. Penyakit Zika sendiri mulai diketahui terjadi di daerah khatulistiwa Afrika dan Asia sejak 1950-an. Kesakitan tersebut adalah satu bentuk penyakit ringan dari demam dengue, dimana sesorang yang terjangkit dirawat melalui istirahat dan tidak bisa dicegah melalui obat-obatan atau vaksin.[1][2] Penyakit Zika memiliki kaitan dengan demam kuning dan virus Nil Barat yang dibawa oleh flavivirus bawaan artropoda yang lain.
Pada 2014, virus ini menyebar ke timur melintasi Samudra Pasifik ke Polinesia Prancis, kemudian ke Pulau Paskah dan pada tahun 2015, ia menyebar ke Amerika Tengah, Karibia, dan kini ia menyebar ke Amerika Selatan sebagai satu wabah besar.[3] Pada Januari 2016, Pusat Kontrol dan Pencegahan Penyakit (CDC) Amerika Serikat mengeluarkan panduan perjalanan untuk negara-negara tejangkit wabah, termasuk panduan langkah pencegahan yang dipertingkatkan dan pertimbangan untuk menunda kehamilan bagi wanita.[4][5] Menurut laporan, transmisi virus Zika pada janin dapat menyebabkan mikrosefalus pada bayi yang baru lahir.[6] Badan-badan kesehatan dan pemerintah lain juga mengeluarkan peringatan yang serupa, sedangkan negara-negara seperti Kolombia, Ekuador, El Salvador, dan Jamaika, menasihati wanita untuk menunda kehamilan sehingga risiko tentang virus tersebut dapat lebih diketahui.[7][8][9][10][8][11]
Organisasi Kesehatan Dunia (WHO) menilai penyakit yang terkait dengan virus Zika di Amerika Latin pada akhir tahun 2015 hingga Januari 2016 telah menimbulkan keadaan darurat kesehatan bagi masyarakat. Oleh sebab itu, WHO mengumumkan Status Darurat Kesehatan Internasional[12].
Virus Zika (ZIKV) merupakan sejenis virus dari keluarga flaviviridae dan genus flavivirus yang disebarkan oleh nyamuk Aedes aegypti. Virus ini dapat menyebabkan sakit yang ringan kepada manusia yang dikenal sebagai demam Zika atau penyakit Zika. Penyakit Zika sendiri mulai diketahui terjadi di daerah khatulistiwa Afrika dan Asia sejak 1950-an. Kesakitan tersebut adalah satu bentuk penyakit ringan dari demam dengue, dimana sesorang yang terjangkit dirawat melalui istirahat dan tidak bisa dicegah melalui obat-obatan atau vaksin. Penyakit Zika memiliki kaitan dengan demam kuning dan virus Nil Barat yang dibawa oleh flavivirus bawaan artropoda yang lain.
Pada 2014, virus ini menyebar ke timur melintasi Samudra Pasifik ke Polinesia Prancis, kemudian ke Pulau Paskah dan pada tahun 2015, ia menyebar ke Amerika Tengah, Karibia, dan kini ia menyebar ke Amerika Selatan sebagai satu wabah besar. Pada Januari 2016, Pusat Kontrol dan Pencegahan Penyakit (CDC) Amerika Serikat mengeluarkan panduan perjalanan untuk negara-negara tejangkit wabah, termasuk panduan langkah pencegahan yang dipertingkatkan dan pertimbangan untuk menunda kehamilan bagi wanita. Menurut laporan, transmisi virus Zika pada janin dapat menyebabkan mikrosefalus pada bayi yang baru lahir. Badan-badan kesehatan dan pemerintah lain juga mengeluarkan peringatan yang serupa, sedangkan negara-negara seperti Kolombia, Ekuador, El Salvador, dan Jamaika, menasihati wanita untuk menunda kehamilan sehingga risiko tentang virus tersebut dapat lebih diketahui.
Organisasi Kesehatan Dunia (WHO) menilai penyakit yang terkait dengan virus Zika di Amerika Latin pada akhir tahun 2015 hingga Januari 2016 telah menimbulkan keadaan darurat kesehatan bagi masyarakat. Oleh sebab itu, WHO mengumumkan Status Darurat Kesehatan Internasional.
Il virus Zika (ZIKV) è un virus a RNA della famiglia Flaviviridae, isolato per la prima volta nel 1947 da un primate nella Foresta Zika, una riserva naturale vicino a Entebbe[1] in Uganda.[2] Negli esseri umani provoca una malattia nota come "febbre Zika". Il virus è strettamente correlato a quelli che provocano la dengue, la febbre gialla, l'encefalite del Nilo occidentale e l'encefalite giapponese, tutti trasmessi soprattutto da punture d'insetto e pertanto definiti arbovirus[3].
Negli anni 2010 si sono registrati occorrenze della malattia da virus Zika in tutti i continenti e dei casi isolati si sono registrati anche in Europa[4], su soggetti che erano reduci da viaggi in zone tropicali e senza che sia documentata alcuna forma di trasmissione del virus in Europa[5].
Il virus è trasmesso da numerose zanzare del genere Aedes, negli ambienti equatoriali soprattutto da Aedes aegypti. Studi sui vettori implicati nella trasmissione del virus hanno permesso di isolare il virus Zika anche in alcune popolazioni di Aedes albopictus (zanzara tigre) provenienti dal Gabon[6].
Poiché questa zanzara è divenuta assai comune anche nei climi temperati dell'emisfero boreale, come in Nord America, nella penisola italiana, e in altre zone del bacino mediterraneo, potrebbe in futuro rappresentare un serio rischio di espansione del virus anche in queste aree del pianeta[7]. Tuttavia non esistono casi documentati di trasmissione del virus in Europa da parte di questa zanzara[8].
Come gli altri virus in questa famiglia, il virus Zika è avvolto da un pericapside icosaedrico e il suo genoma è costituito da una singola elica di RNA a senso positivo, lunga 10.794 nucleotidi. Dal punto di vista filogenetico, esso è strettamente imparentato con il virus Spondweni, un virus che con lo Zika forma un proprio gruppo (clade) Spondweni all'interno al genere Flavivirus.
Condivide con gli altri membri del genere le stesse caratteristiche strutturali e lo stesso ciclo di replicazione, così come la stessa organizzazione genetica, tranne che per la regione 3' UTR[9]. Altri membri appartenenti allo stesso genere sono il virus Ilheus (ILHV), quello dell'encefalite di Rocio o virus Rocio (ROCV) e dell'encefalite di Saint-Louis[10].
Si segnalano casi di possibile co-infezione virale Dengue + Chikungunya + Zika[11].
La febbre Zika si contrae prevalentemente tramite punture di artropodi (zanzare), pur essendo possibile un contagio diretto attraverso emoderivati o per via sessuale, stante la presenza di virioni nel liquido seminale di uomini malati[12].
Principali serbatoi animali dell'infezione sono i primati, alcuni grandi mammiferi (ippopotami, impala, elefanti, capre, pecore, alcelafi, leoni, gnu, zebre) e i roditori[13]. Durante la prima settimana di infezione il virus Zika è presente in circolo e può essere isolato nel sangue del soggetto[14].
Molte specie di zanzare appartenenti ai generi Aedes, Anopheles, Mansonia ed Eretmapodites sono state identificate come vettori del virus[15]. Nei climi caldi il vettore principale è costituito da A. africanus e A. aegypti[16] e, in misura minore, da A. polynesiensis, A. unilineatus, A. vittatus e A. hensilli[17]. Durante l'epidemia di febbre Zika nell'Isola Yap nel 2007, l'Aedes hensilli venne identificata come principale vettore[18]. Negli altri climi più temperati, un potenziale vettore potrebbe diventare la zanzara tigre (Aedes albopictus), abbondantemente distribuita in tutto il mondo[19]. Tuttavia non sono stati documentati casi di trasmissione del virus nelle aree europee[5], sebbene questa zanzara sia ormai piuttosto comune in alcune zone come la penisola italiana o altre zone del bacino mediterraneo e dell'Europa centrale[20].
Le vie di trasmissione note sono[21]:
Inoltre è verosimile la possibilità di contagio materno-fetale, essendo stato trovato il virus all'interno della placenta e nel liquido amniotico di malate gravide, con conseguenti effetti teratogeni segnalati sull'embrione, soprattutto nel primo trimestre di gravidanza[25].
Viene segnalata la possibilità di una trasmissione del virus con la saliva in caso di bacio, però, secondo gli esperti infettivologi dell'ospedale Spallanzani[26], questa via è molto remota per la scarsa carica virale nella saliva. Al contrario la possibilità di una trasmissione con lo sperma è documentata, essendo stato accertato ufficialmente nel mese di febbraio 2016 il secondo caso di trasmissione del virus per via sessuale: in Texas in una donna contagiata dal partner tornato da un viaggio in Sud America[27][28].
Uno studio brasiliano pubblicato su The Lancet il 17 febbraio 2016 ha suggerito una possibile conferma della trasmissione materno-fetale con il liquido amniotico (trasmissione verticale). Il ceppo che interessa il Brasile nel 2016 è un ceppo geneticamente correlato a quello trovato nella Polinesia Francese nel 2013; inoltre i ricercatori scrivono che questo ceppo è responsabile dei casi di microcefalia trovati in Brasile in misura abnormemente alta rispetto a prima dell'epidemia da Zika virus, pur mancando ancora la prova definitiva del tropismo del virus sulle cellule nervose umane[29].
Il virus fu isolato nel 1947 da un esemplare di macaco rhesus presente nella Foresta Zika dell'Uganda, e successivamente nel 1968 fu isolato per la prima volta in esseri umani in Nigeria. Dal 1951 al 1981 altri campioni umani sono risultati positivi anche in Uganda, Tanzania, Egitto, Repubblica Centrafricana, Sierra Leone, Senegal e Gabon. In Asia si è riscontrata in India, Malaysia, Filippine, Thailandia, Vietnam e Indonesia, dove è stato trovato nel 2006[18].
La prima epidemia nota da virus Zika fuori dall'Africa è stata nel 2007 nell'isola di Yap, nella Micronesia[30]. Il virus Zika è stato trovato nel 2015 anche in Colombia, Suriname, El Salvador, Guatemala, Capo Verde, Figi, Vanuatu, Samoa, Nuova Caledonia, isole Salomone, Indonesia[31], Messico[1] e Brasile[32].
Gli studi che hanno analizzato l'intero RNA dell'agente infettivo hanno dimostrato un'alta omologia genomica tra il ceppo latino-americano e quello che ha circolato nel Pacifico tra il 2013 e il 2014[33].
Il virus Zika risulta avere un tropismo spiccato per il tessuto nervoso e per il sistema nervoso centrale: risulta, pertanto, collegato a problemi che riguardano il SNC, come deficit dell'apprendimento e microcefalia. In Polinesia ci sono stati molti casi di Zika ma pochi di microcefalia. Viene da chiedersi, naturalmente, quale sia la ragione: questa è da ricercarsi nel fatto che ivi è possibile ricorrere all'aborto terapeutico, quindi ogni volta che veniva trovato un quadro encefalico alterato, si ricorreva all'aborto.
Il virus Zika (ZIKV) è un virus a RNA della famiglia Flaviviridae, isolato per la prima volta nel 1947 da un primate nella Foresta Zika, una riserva naturale vicino a Entebbe in Uganda. Negli esseri umani provoca una malattia nota come "febbre Zika". Il virus è strettamente correlato a quelli che provocano la dengue, la febbre gialla, l'encefalite del Nilo occidentale e l'encefalite giapponese, tutti trasmessi soprattutto da punture d'insetto e pertanto definiti arbovirus.
Negli anni 2010 si sono registrati occorrenze della malattia da virus Zika in tutti i continenti e dei casi isolati si sono registrati anche in Europa, su soggetti che erano reduci da viaggi in zone tropicali e senza che sia documentata alcuna forma di trasmissione del virus in Europa.
Il virus è trasmesso da numerose zanzare del genere Aedes, negli ambienti equatoriali soprattutto da Aedes aegypti. Studi sui vettori implicati nella trasmissione del virus hanno permesso di isolare il virus Zika anche in alcune popolazioni di Aedes albopictus (zanzara tigre) provenienti dal Gabon.
Poiché questa zanzara è divenuta assai comune anche nei climi temperati dell'emisfero boreale, come in Nord America, nella penisola italiana, e in altre zone del bacino mediterraneo, potrebbe in futuro rappresentare un serio rischio di espansione del virus anche in queste aree del pianeta. Tuttavia non esistono casi documentati di trasmissione del virus in Europa da parte di questa zanzara.
Zika virus est virus generis Flaviviri familiae Flaviviridarum, quod per culicidas generis Aedis interdiu volantes, praecipue specierum Aedis aegypti et Aedis albopicti, transmittitur. Nomen ex silva Zika in Uganda venit, ubi virus primum detectum est anno 1947.[1]
Contagio, febris Zika appellanda,[2] saepe indicia nulla vel mitia exhibens, ex annis 1950, intra angustam zonam aequatorialem ab Africa ad Asiam migravisse nota est. Anno autem 2014, virus ad orientem trans Oceanum Pacificum ad Polynesiam Francicam, tum ad Insulam Paschalem et anno 2015 ad Mexicum, Americam Mediam, Mare Caribicum, et Americam Australem extentum est, ubi eruptio Zika viri pandemicos attigit gradus.[3]
Zika virus viris febris dengue, febri flavae, encephalitidis Iaponiensis, et Nili Occidentalis, viris morborum gravissimorum, cognatus est.[4] Morbus autem, quem efficit, formae miti febris dengue similis est,[4] et curatur enim quiete tantum,[5] a medicamentis autem vel vaccinis nondum prohiberi potest.[5] Probabilis est nexus a febri Zika ad microcephaliam in infantibus recentibus natis per transmissionem a matre ad infantem,[6][7][8] possibilis etiam maior nexus cum statibus neurologicis in adultis infectis, inter quos casus syndromae Guillain–Barré.
Febris Zika (in nonnullis regionibus etiam morbus febris Zika dictum) est eventus ex contagione. Saepe symptomata desunt vel parum, quasi forma lenis febris dengue. Symptomata una cum febri sunt arthralgiae, myalgiae, exanthema maculopapulosum[9]. Secundum CDC (centra gubernationis morbi et praeventionis) tractatio ad symptomata spectat, therapia specifica incognita sit, quies, bibere periculo dehydratationis, analgeticum acetaminophenum ibi commendantur[10].
Die 27 mensis Maii 2016 in epistula publica[11] ad Ordinem Mundi Sanitarium 150 periti pericula diffusionis monebantque postulabant Olympiam aestivam 2016 Urbis Fluminensis ad alterum temporis punctumve locum dilativa iri.

Zika virus est virus generis Flaviviri familiae Flaviviridarum, quod per culicidas generis Aedis interdiu volantes, praecipue specierum Aedis aegypti et Aedis albopicti, transmittitur. Nomen ex silva Zika in Uganda venit, ubi virus primum detectum est anno 1947.
Contagio, febris Zika appellanda, saepe indicia nulla vel mitia exhibens, ex annis 1950, intra angustam zonam aequatorialem ab Africa ad Asiam migravisse nota est. Anno autem 2014, virus ad orientem trans Oceanum Pacificum ad Polynesiam Francicam, tum ad Insulam Paschalem et anno 2015 ad Mexicum, Americam Mediam, Mare Caribicum, et Americam Australem extentum est, ubi eruptio Zika viri pandemicos attigit gradus.
Zika virus viris febris dengue, febri flavae, encephalitidis Iaponiensis, et Nili Occidentalis, viris morborum gravissimorum, cognatus est. Morbus autem, quem efficit, formae miti febris dengue similis est, et curatur enim quiete tantum, a medicamentis autem vel vaccinis nondum prohiberi potest. Probabilis est nexus a febri Zika ad microcephaliam in infantibus recentibus natis per transmissionem a matre ad infantem, possibilis etiam maior nexus cum statibus neurologicis in adultis infectis, inter quos casus syndromae Guillain–Barré.
Zika virusas (angl. Zika virus, ZIKV) – virusas, priklausantis Flavivirus genčiai, Flaviviridae šeimai; Zika virusinės infekcijos sukėlėjas. Pagrindiniai Zika viruso pernešėjai yra Aedes genties uodai.
Zika virusinei ligai būdingas karščiavimas ir bėrimas. Inkubacinis ligos periodas gali užtrukti nuo 3 iki 12 dienų. Apie 60–80 proc. infekcijos atvejų gali būti besimptomės. Infekcijos simptomai nežymūs, tęsiasi 4–7 dienas. Ligai būdingas makulinis ar papulinis bėrimas, karščiavimas, sąnarių, raumenų, galvos skausmai, nepūlingas konjunktyvitas. Bėrimas dažnai prasideda veido srityje ir išplinta po visą kūną.
Zika virusas pavojingas nėščiosioms, nes, manoma, sukelia apsigimimus – dėl jo sulėtėja vaisiaus galvos vystymasis. Jis gali būti perduodamas vaikui per placentą arba gimdymo metu. Yra nustatytų ir lytinio užsikrėtimo atvejų. Tikėtina, kad Zika virusas gali būti perduodamas per kraujo ir jo komponentų transfuzijas.
Vakcinos nuo Zika virusinės infekcijos nėra. Žmonės turėtų naudoti asmenines apsaugos priemones, skirtas apsisaugojimui nuo uodų įgėlimų.
Zika virusas pirmą kartą išskirtas 1947 m. iš beždžionės Ugandoje, tropiniame Zika miške. 1948 m. paaiškėjo, kad Zika virusą perneša to paties miško uodai Aedes africanus. Iki 2007 m. viruso cirkuliacija ir keletas protrūkių buvo registruoti tropinėje Afrikoje ir kai kuriose Pietryčių Azijos teritorijose, vėliau virusas pasireiškė Ramiojo vandenyno salose. 2015 m. šios ligos protrūkis pirmą kartą užregistruotas Pietų Amerikoje.
Zika virusas (angl. Zika virus, ZIKV) – virusas, priklausantis Flavivirus genčiai, Flaviviridae šeimai; Zika virusinės infekcijos sukėlėjas. Pagrindiniai Zika viruso pernešėjai yra Aedes genties uodai.
Zika virusinei ligai būdingas karščiavimas ir bėrimas. Inkubacinis ligos periodas gali užtrukti nuo 3 iki 12 dienų. Apie 60–80 proc. infekcijos atvejų gali būti besimptomės. Infekcijos simptomai nežymūs, tęsiasi 4–7 dienas. Ligai būdingas makulinis ar papulinis bėrimas, karščiavimas, sąnarių, raumenų, galvos skausmai, nepūlingas konjunktyvitas. Bėrimas dažnai prasideda veido srityje ir išplinta po visą kūną.
Zika virusas pavojingas nėščiosioms, nes, manoma, sukelia apsigimimus – dėl jo sulėtėja vaisiaus galvos vystymasis. Jis gali būti perduodamas vaikui per placentą arba gimdymo metu. Yra nustatytų ir lytinio užsikrėtimo atvejų. Tikėtina, kad Zika virusas gali būti perduodamas per kraujo ir jo komponentų transfuzijas.
Vakcinos nuo Zika virusinės infekcijos nėra. Žmonės turėtų naudoti asmenines apsaugos priemones, skirtas apsisaugojimui nuo uodų įgėlimų.
Zikas vīruss ir viens no Flaviviridae dzimtas vīrusiem, kas izplatās ar Aedes ģints odu starpniecību un tiek nodots arī seksuāli transmisīvā ceļā.[1] Cilvēkiem Zikas vīruss izraisa vieglu drudzi, ko neuzskata par dzīvībai bīstamu. To sauc par Zikas drudzi vai Zikas slimību. Pasaulē satraukumu radījusi atrastā saistība, ka grūtniecības laikā ar Zikas slimību inficētajām mātēm dzimst bērni ar mikrocefāliju.[2][3]
Slimība ir zināma jau no 1950. gadiem un bija sastopama šaurā ekvatoriālā joslā no Āfrikas līdz Āzijai. 2014. gadā vīruss izplatījās pāri Klusajam okeānam līdz Franču Polinēzijai, tad uz Lieldienu salām un 2015. gadā arī uz Centrālameriku, Karību salām, Dienvidameriku, kur Zikas slimība ir sasniegusi pandēmijas līmeni. Zikas vīruss ir līdzīgs denges, dzeltenā drudža, japāņu encefalīta, Rietumnīlas vīrusiem.[4] Visi šie vīrusi izplatās odu kodumu rezultātā. Reģistrēti arī vairāki gadījumi, kad Zikas vīruss izplatījies dzimumkontaktu ceļā.[5][6] Zikas slimības izpausmes ir līdzīgas mērenai Denges drudža formai, ko ārstē ar atpūtu. Pret to nav pieejamas vakcīnas vai zāles.[7]
2016. gadā ASV Slimību kontroles un profilakses centrs (U.S. Center for Disease Control and Prevention) izdevis ceļošanas vadlīnijas, kurās grūtnieces tiek brīdinātas ievērot piesardzību un, iespējams, arī atlikt ceļojumus uz Zikas slimības skartajām valstīm.[8] Citas valstis un veselības dienesti ir devuši līdzīgus brīdinājumus. Kolumbijā, Ekvadorā, Dominikānas Republikā un Jamaikā veselības dienesti ieteikuši neplānot grūtniecību, kamēr nav pilnībā skaidri riski.[9]
Biežākie Zikas vīrusa infekcijas simptomi ir mērenas galvassāpes, masalveida izsitumi, drudzis, konjunktivīts un locītavu sāpes, ko parasti ārstē ar paracetamolu. Nav reģistrēts neviens nāves gadījums vīrusa dēļ.
Zikas vīruss ir viens no Flaviviridae dzimtas vīrusiem, kas izplatās ar Aedes ģints odu starpniecību un tiek nodots arī seksuāli transmisīvā ceļā. Cilvēkiem Zikas vīruss izraisa vieglu drudzi, ko neuzskata par dzīvībai bīstamu. To sauc par Zikas drudzi vai Zikas slimību. Pasaulē satraukumu radījusi atrastā saistība, ka grūtniecības laikā ar Zikas slimību inficētajām mātēm dzimst bērni ar mikrocefāliju.
Slimība ir zināma jau no 1950. gadiem un bija sastopama šaurā ekvatoriālā joslā no Āfrikas līdz Āzijai. 2014. gadā vīruss izplatījās pāri Klusajam okeānam līdz Franču Polinēzijai, tad uz Lieldienu salām un 2015. gadā arī uz Centrālameriku, Karību salām, Dienvidameriku, kur Zikas slimība ir sasniegusi pandēmijas līmeni. Zikas vīruss ir līdzīgs denges, dzeltenā drudža, japāņu encefalīta, Rietumnīlas vīrusiem. Visi šie vīrusi izplatās odu kodumu rezultātā. Reģistrēti arī vairāki gadījumi, kad Zikas vīruss izplatījies dzimumkontaktu ceļā. Zikas slimības izpausmes ir līdzīgas mērenai Denges drudža formai, ko ārstē ar atpūtu. Pret to nav pieejamas vakcīnas vai zāles.
2016. gadā ASV Slimību kontroles un profilakses centrs (U.S. Center for Disease Control and Prevention) izdevis ceļošanas vadlīnijas, kurās grūtnieces tiek brīdinātas ievērot piesardzību un, iespējams, arī atlikt ceļojumus uz Zikas slimības skartajām valstīm. Citas valstis un veselības dienesti ir devuši līdzīgus brīdinājumus. Kolumbijā, Ekvadorā, Dominikānas Republikā un Jamaikā veselības dienesti ieteikuši neplānot grūtniecību, kamēr nav pilnībā skaidri riski.
Biežākie Zikas vīrusa infekcijas simptomi ir mērenas galvassāpes, masalveida izsitumi, drudzis, konjunktivīts un locītavu sāpes, ko parasti ārstē ar paracetamolu. Nav reģistrēts neviens nāves gadījums vīrusa dēļ.
Virus Zika virus /ˈziːkə, ˈzɪkə/[1][2][3][4] (ZIKV) adalah virus ahli keluarga Flaviviridae dan genus Flavivirus, yang disebarkan oleh oleh nyamuk Aedes aktif-siang, seperti A. aegypti dan A. albopictus. Virus ini boleh memberi kesakitan yang ringan kepada manusia dan ia dikenali sebagai demam Zika atau penyakit Zika, dimana penyakit tersebut mula diketahui berlaku di kawasan khatulistiwa Afrika dan Asia sejak 1950-an. Kesakitan tersebut adalah satu bentuk penyakit ringan daripada demam denggi,[5] dimana ia dirawat melalui rehat[6] dan tidak boleh dicegah melalui ubat-ubatan atau vaksin. Namanya berasal dari Hutan Zika di Uganda , di mana virus pertama kali diasingkan pada tahun 1947.[7] Virus Zika berkaitan dengan penyakit demam denggi, demam kuning, Ensefalitis Jepun, dan virus Nil Barat.[5]
Pada 2014, virus ini merebak ke timur merentasi Lautan Pasifik ke Polinesia Perancis, kemudian ke Pulau Easter dan pada tahun 2015, ia merebak ke Amerika Tengah, Caribbean dan kini ia merebak ke Amerika Selatan sebagai satu wabak besar.[8] Pada Januari 2016, Pusat Kawalan dan Pencegahan Penyakit (CDC) Amerika Syarikat mengeluarkan panduan perjalanan bagi negara-negara terjejas, termasuklah panduan langkah berjaga-jaga yang dipertingkatkan dan pertimbangan untuk menangguhkan perjalanan serta panduan untuk wanita hamil.[9][10] Agensi-agensi kesihatan dan pemerintah lain turut mengeluarkan amaran yang serupa,[11][12][13][14] manakala negara-negara seperti Colombia, Ecuador, El Salvador dan Jamaica, menasihati wanita untuk menangguhkan kehamilan sehingga risiko mengenai virus tersebut dapat lebih diketahui.[12][15].Pakar perubatan sedang bertungkus lumus dalam mencari vaksin bagi virus ini
Virus Zika virus /ˈziːkə, ˈzɪkə/ (ZIKV) adalah virus ahli keluarga Flaviviridae dan genus Flavivirus, yang disebarkan oleh oleh nyamuk Aedes aktif-siang, seperti A. aegypti dan A. albopictus. Virus ini boleh memberi kesakitan yang ringan kepada manusia dan ia dikenali sebagai demam Zika atau penyakit Zika, dimana penyakit tersebut mula diketahui berlaku di kawasan khatulistiwa Afrika dan Asia sejak 1950-an. Kesakitan tersebut adalah satu bentuk penyakit ringan daripada demam denggi, dimana ia dirawat melalui rehat dan tidak boleh dicegah melalui ubat-ubatan atau vaksin. Namanya berasal dari Hutan Zika di Uganda , di mana virus pertama kali diasingkan pada tahun 1947. Virus Zika berkaitan dengan penyakit demam denggi, demam kuning, Ensefalitis Jepun, dan virus Nil Barat.
Pada 2014, virus ini merebak ke timur merentasi Lautan Pasifik ke Polinesia Perancis, kemudian ke Pulau Easter dan pada tahun 2015, ia merebak ke Amerika Tengah, Caribbean dan kini ia merebak ke Amerika Selatan sebagai satu wabak besar. Pada Januari 2016, Pusat Kawalan dan Pencegahan Penyakit (CDC) Amerika Syarikat mengeluarkan panduan perjalanan bagi negara-negara terjejas, termasuklah panduan langkah berjaga-jaga yang dipertingkatkan dan pertimbangan untuk menangguhkan perjalanan serta panduan untuk wanita hamil. Agensi-agensi kesihatan dan pemerintah lain turut mengeluarkan amaran yang serupa, manakala negara-negara seperti Colombia, Ecuador, El Salvador dan Jamaica, menasihati wanita untuk menangguhkan kehamilan sehingga risiko mengenai virus tersebut dapat lebih diketahui..Pakar perubatan sedang bertungkus lumus dalam mencari vaksin bagi virus ini
Het zikavirus is een flavivirus dat de ziekte zikakoorts veroorzaakt. Het virus wordt voornamelijk overgebracht door vrouwelijke steekmuggen. De zikakoorts is over het algemeen een milde aandoening waar geen behandeling voor is. De ziekte gaat vaak vanzelf weer over.[1] Er zijn echter aanwijzingen dat besmetting met het virus ernstige gevolgen voor de menselijke gezondheid kan hebben, met name voor de foetus. Het kind zou als gevolg van het virus microcefalie kunnen ontwikkelen, een te kleine schedelomvang met grote gevolgen voor de verdere ontwikkeling.[2]
Het virus is bekend sinds 1947, toen het in het in Oeganda gelegen Zikawoud werd vastgesteld bij een resusaap. Het virus dankt zijn naam aan het betreffende woud.
Het zikavirus is in 1947 voor het eerst waargenomen in het Zikawoud (Entebbe, Oeganda), bij een onderzoek naar de transmissie van gele koorts bij resusmakaken.[3][4] Een besmetting met het zikavirus bij de mens werd in 1954 voor het eerst aangetoond, in Nigeria.[5] Daarna bleef het virus tot 2007 buiten beeld.
Eind 2013 werd het zikavirus bij ongeveer 10.000 patiënten gevonden in Frans-Polynesië.[1]
In de periode 2010 t/m 2014 werden in Brazilië minder dan 100 geboortes van baby's met microcefalie per jaar gemeld, maar in 2015 waren dit er meer dan 1200.[6], hetgeen een verband met het Zikavirus deed vermoeden. De virusuitbraak van mei 2015 in Brazilië verspreidde zich over andere landen in Zuid- en Midden-Amerika.
Op 20 januari 2016 werd het eerste geval op Curaçao bevestigd.[7] In Suriname komen eveneens besmettingen voor.[8]
Gezien de omvang van het gebied wordt in 2015 en 2016 van een pandemie gesproken.[9] In januari 2016 waren zoveel ziektegevallen in Zuid-Amerika vastgesteld dat overheden in verschillende landen vrouwen met een kinderwens afraadden om zwanger te worden.[10]
Op 3 september 2016 maakte de Wereldgezondheidsorganisatie bekend dat er tijdens de Olympische Zomerspelen (die waren gehouden in Rio de Janeiro) geen nieuwe gevallen van besmetting zijn geweest, iets waarvoor eerder was gevreesd.[11]
Meldingen van de ziekte waren er begin 2016 ook uit de Maldiven, Thailand, Kaapverdië, de Salomonseilanden, Fiji en Nieuw-Caledonië.[12]
Op 22 maart 2016 werd het eerste geval van het virus in Zuid-Korea gemeld.[13]
Begin september 2016 doken er 27 nieuwe besmettingsgevallen op in Singapore. Het totale aantal besmettingen in Singapore kwam hiermee op 242.[14]
Tussen oktober 2015 en januari 2016 werden in Duitsland vijf gevallen geconstateerd. Het waren zover bekend de eerste waarnemingen in Europa.[15] Op 4 februari 2016 werd het virus vastgesteld bij een zwangere vrouw in Noordoost-Spanje die daarvoor in Colombia was geweest.[16]
Op 6 mei 2016 werd in Spanje melding gemaakt van een uit een met het zikavirus besmette vrouw geboren baby, die reeds bij de geboorte afwijkingen (microcefalie) vertoonde. Het was het eerste concrete geval in Spanje waarbij een baby werd geboren met dergelijke afwijkingen die naar alle waarschijnlijkheid met het virus verband houden.[17]
Eind juli 2016 werden er voor het eerst gevallen van besmetting met het virus binnen de VS geconstateerd. Het ging om drie mannen en een vrouw uit Florida, die in de nabijheid van Miami besmet zouden zijn geraakt.[18] De Amerikaanse regering nam een ongebruikelijke maatregel: er werd een negatief reisadvies afgegeven dat alleen gold voor een deel van de stad Miami.[19]
Braziliaanse onderzoekers stelden dat een besmetting met het virus mogelijk het syndroom van Guillain-Barré kan veroorzaken.[20]
Eind juli 2016 beweerden Amerikaanse onderzoekers bij proeven op muizen antilichamen tegen het virus te hebben gevonden. Dezelfde antistoffen zouden ook helpen tegen knokkelkoorts.[21]
In augustus 2016 kwam het reeds bestaande niclosamide in beeld als middel tegen het zikavirus.[22]
In mei 2018 bracht de Belgische Hoge Gezondheidsraad (HGR) een advies uit voor reizigers naar gebieden waar het zikavirus voorkomt. In dat advies raadt de HGR reizigers aan steeds op de hoogte te blijven van evoluties in de situatie, in het bijzonder welke betrokken gebieden door de Wereldgezondheidsorganisatie zijn ondergebracht in categorie 1 en 2. Dit zijn de gebieden waar een actieve overdracht van het virus is of waar gevallen van overdracht onlangs zijn gemeld. Alle niet-noodzakelijke reizen naar gebieden van categorie 1 en 2 worden door de HGR afgeraden, in het bijzonder voor risicogroepen (zwangere vrouwen, vrouwen die zwanger willen worden en hun partners, peuters, bejaarden en immuungecompromitteerde mensen). Indien de reis absoluut noodzakelijk is, beveeldt de HGR aan alle door het Instituut voor Tropische Geneeskunde (ITG) aanbevolen preventiemaatregelen tegen muggen strikt op te volgen. Ook zouden mensen uit de risicogroepen voor vertrek een arts moeten raadplegen. Zwangere vrouwen, vrouwen die zwanger willen worden en hun partners dienen onbeschermde geslachtsgemeenschap tijdens hun verblijf te vermijden. Na terugkeer moeten mensen met symptomen van een infectie onmiddellijk een deskundige raadplegen. Zwangere vrouwen, vrouwen die zwanger willen worden en hun partners dienen ook als ze geen symptomen hebben geen onbeschermde geslachtsgemeenschap te hebben gedurende zes maanden of totdat ze een deskundige hebben geraadpleegd.[23]
Het zikavirus is een flavivirus dat de ziekte zikakoorts veroorzaakt. Het virus wordt voornamelijk overgebracht door vrouwelijke steekmuggen. De zikakoorts is over het algemeen een milde aandoening waar geen behandeling voor is. De ziekte gaat vaak vanzelf weer over. Er zijn echter aanwijzingen dat besmetting met het virus ernstige gevolgen voor de menselijke gezondheid kan hebben, met name voor de foetus. Het kind zou als gevolg van het virus microcefalie kunnen ontwikkelen, een te kleine schedelomvang met grote gevolgen voor de verdere ontwikkeling.
Het virus is bekend sinds 1947, toen het in het in Oeganda gelegen Zikawoud werd vastgesteld bij een resusaap. Het virus dankt zijn naam aan het betreffende woud.
Zika-virus (ZIKV) er et virus i familien flavivirus. Viruset overføres av aedes-mygg og videre mellom mennesker ved seksuell kontakt. Hos mennesker kan det føre til den vanligvis milde sykdommen zika-feber som siden 1950-tallet tidvis har forekommet innen et smalt belte langs ekvator fra Afrika til Asia. I november 2015 ble det oppdaget en mulig kobling mellom infeksjoner hos gravide og fosterskader. Den 1. februar klassifiserte Verdens helseorganisasjon (WHO) smittespredningen av zika-viruset som en internasjonal nødstilstand.
Viruset ble isolert første gang i april 1947 fra en rhesusape som forskere hadde plassert i et bur i Zika-skogen i Uganda.[1] Det første dokumenterte utbruddet blant mennesker fant sted i 2007 i Mikronesia.[2] I løpet av 2014 spredte viruset seg østover over Stillehavet til Fransk Polynesia og videre til Påskeøya for så å senere i løpet av 2015 fortsette til Sør-Amerika, Sentral-Amerika og Karibia. Utbruddet ble klassifisert som en pandemi.[3] I januar 2016 ble det publisert rapporter om eventuelle koblinger mellom zika-virusinfeksjon og alvorlige komplikasjoner som kan rammee foster. Viruset blir trodd å kunne forårsake mikrocefali hos nyfødte barn til mødre som var smittet under graviditeten, men sambandet og eventuell riskiko er (februar 2016) ikke helt klarlagt og utredning pågår.[4][5] Den 15. januar utferdiget USAs nasjonale folkehelsemyndighet Centers for Disease Control and Prevention (CDC) reiseråd gjeldende de berørte lande som innebærer at gravide kvinner bør overveie å utsette reisen.[6] Lignende råd er utferdiget av flere andre land.
Den 1. februar klassifiserte Verdens helseorganisasjon (WHO) smittespredningen av zika-viruset som en internasjonal nødstilstand. WHO fryktet at opp til fire millioner mennesker kunne ble smittet før årets slutt.[7] I den verst rammede regionen i Brasil er om lag en prosent av de nyfødte antatt født med mikrocefali.[8]
Virusets naturlige reservoar er ennå ikke fastslagt men man har påvist serologiske funn hos vestafrikanske aper og gnagere. Zika-viruset overføres av dagaktive mygg og er blitt isolert fra et antall arter i slekten Aedes, blant demAedes aegypti, Aedes africanus, Aedes apicoargenteus, Aedes furcifer, Aedes hensilli, Aedes luteocephalus og Aedes vittatus.[9]
Zika-virus kan overføres mellom mennesker ved seksuell kontakt.[10] Det kan også passere morkaken hos gravide kvinner og dermed påvirke et foster.
Ettersom viruset bare kan primørspres i de områder der det finnes myggarter som kan bære det, er forandringar av myggartenes utbredningsområder en viktig årsak til at regioner som tidligere var fri fra zika-smitte er blitt rammet. Den viktigste vektoren, A. aegypti, spres til nya områder ved handel og reiser.[11] A. aegypti finnes nå på alle kontinenter inklusive Nord-Amerika og også noen mindre deler av Europa.[12] En myggpopulasjon som er kapabel til å bære viruset er blitt påtruffet i Washington, DC og genetiske bevis antyder at den har overlevd i det minste fire vintre i området. Forskere antar at myggene har tilpasset seg for å kunne overleve i nordlig klima.[13]
I 2015 ble det registrert at zika hadde spredt seg i Karibia og Sør-Amerika. De land og territorier som ifølge Pan American Health Organisation (PAHO) er rammet av lokal spredning av zika-virus er Barbados, Bolivia, Brasil, Colombia, Den dominikanske republikk, Ecuador, El Salvador, Fransk Guyana, Guadeloupe, Guatemala, Guyana, Haiti, Honduras, Martinique, Mexico, Panama, Paraguay, Puerto Rico, Saint Martin, Surinam og Venezuela.[14][15]
I 2015 ble det detektert RNA fra zika-virus i fostervann hos to foster, noe som tyder på at det hadde passert morkaken og kunne gi en mor-til-barn-infeksjon.[16]
|dato= (hjelp) |dato= (hjelp) Zika-virus (ZIKV) er et virus i familien flavivirus. Viruset overføres av aedes-mygg og videre mellom mennesker ved seksuell kontakt. Hos mennesker kan det føre til den vanligvis milde sykdommen zika-feber som siden 1950-tallet tidvis har forekommet innen et smalt belte langs ekvator fra Afrika til Asia. I november 2015 ble det oppdaget en mulig kobling mellom infeksjoner hos gravide og fosterskader. Den 1. februar klassifiserte Verdens helseorganisasjon (WHO) smittespredningen av zika-viruset som en internasjonal nødstilstand.
Edge Hill
Bouboui
Uganda S
Banzi
Jugra
Potiskum, Saboya
wirus dengi
Kedougou
Spondweni
Zika Yap 2007
Zika Uganda 47
Zika Senegal 84a, 84b, 84c
Tembusu, Ntaya, Bagaza, Israel turkey ME
Ilheus, Rocio, St. Louis Enc
Bussuquara, Naranjal, Iguape, Aroa
Stratford, Kokobera
Cacipacore
Yacunde, wirus Zachodniego Nilu, Kountango
Alfuy, Japanese Enc, Usutu, Murray Valley Enc
Lanciotti i in. zwrócili uwagę na 12 par zasad w genie kodującym białko osłonki (ang. envelope protein) szczepu z 2007, które nie występowały u szczepu z Ugandy, jako że wiążą się one z motywem glikozylacji, a przez to z wirulencją. Motyw ten był tracony przez niektóre wirusy z rodzaju Flavivirus. Nie można wykluczyć, że szczep z Ugandy utraci go podczas pasażowania na mózgach mysich, podobnie jak to się stało w przypadku wirusa Zachodniego Nilu[1].
Haddow i współpracownicy przeprowadzili natomiast opisane w 2012 badania genetyczne, dzięki który porównali różne linie wirusa, co zobrazowano kladogramem (wirus Spondweni stanowi grupę zewnętrzną)[3]:
Uganda 1947
Nigeria 1968, Senegal 1984
Malezja 1966
Kambodża 2010, Mikronezja (Yap) 2007
W badaniu wyraźnie zaznaczył się podział na szczepy afrykańskie i azjatyckie. Różnią je między innymi pewne delecje zmieniające miejsca glikozylacji białka E. Jednakże zmiany te wynikać też mogą z pasażowania. Zgodnie z tymi badaniami szczep odpowiedzialny za epidemię na Yap powstał w Azji Południowo-Wschodniej. Natomiast szczep z Kambodży, nieznany przed 2010, wyodrębnił się niedawno od szczepu malezyjskiego, którego przodek rozprzestrzeniał się w Azji Południowo-Wschodniej w połowie pierwszej dekady XX wieku[3].
Kutsuna et al również zbadali pokrewieństwa pomiędzy różnymi szczepami wirusa Zika (wirus Spondweni także w tym badaniu pełni rolę grupy zewnętrznej). Ich wyniki zobrazowano następującym kladogramem[6]:
Uganda1947
Nigeria1968, Senegal1984
Malaisia1966
Japan-Tahiti2014
Cambodia2010, Micronesia 2007
ZIKV znany był początkowo z Afryki oraz Azji Południowo-Wschodniej[1]. Po raz pierwszy został wyizolowany w Ugandzie w 1947 z małpy z gatunku makak królewski podczas badań żółtej gorączki prowadzonych w lesie Zika[1] (w okolicy Entebbe[7]), na obszarze występowania komara Aedes africanus[1]. Zwierzę uczestniczące w programie badań gorączki żółtej Fundacji Rockefellera, nazwane Rhesus 766[2], cierpiało na gorączkę[1], która rozwinęła się 18 kwietnia 1947. Dwa dni później w laboratorium surowicą jego krwi inokulowano domózgowo myszy. W badaniach wzięły udział albinotyczne myszy szczepu Swiss[5]. Objawy pojawiały się zazwyczaj po 6 dniach[5], rozwinęły się u wszystkich gryzoni po 10 dniach[2]. Myszy prezentowały mniejszą aktywność, ich futro było bardziej szorstkie. Wszystkie zarażone gryzonie padały podczas 17 pierwszych pasażowań. Dopiero przy 18. pasażowaniu jeden z nich przeżył. Średni czas przeżycia zwierząt w następnych 4 pasażowaniach określono na 10,6 dnia, później spadł on do 5 dni. Po 60 pasażowaniach okres inkubacji spadł do 5 dni, a jeszcze później do 4, utrzymując się odtąd na stałym poziomie (przeprowadzono 157 pasażowań do czasu oddania publikacji). W miarę pasażowania pojawiały się też u myszy nowe objawy, jak słabość kończyn aż do paraliżu, śmiertelnego w skutkach (śmierć następowała po nim w 24–48 godzin). Jednakże niektóre myszy po 1–2 tygodniach choroby zdrowiały, także te z osłabieniem siły mięśniowej kończyn[5]. Podobne były wyniki analogicznych badań ze szczepem E/1 wirusa, choć okres inkubacji szybciej zmierzał ku 4 dniom. Ponadto zaobserwowano jeszcze zwiększającą się z wiekiem myszy podatność[5].
Z mózgów myszy udało się wyizolować wirusa[2], poza tymi, które wyzdrowiały. Sekcja zwłok wykazała także brak zajęcia przez niego innych narządów poza mózgiem. Badania Dicka wykazały również brak wykrywalnej wiremii[5]. Nie udało się natomiast zarazić ZIKV bawełniaka szczeciniastego[5] (chomikowate)[8], nie chorowały także laboratoryjne kawie domowe i króliki. Również u większości małp poza rezusem 766 (badano kotawce zielonosiwe, zwane także koczkodanami zielonosiwymi) nie dopatrzono się objawów choroby, po 2–3 tygodniach od zarażenia wykrywano u nich przeciwciała odpornościowe. Niekiedy obserwowano nieznaczne podwyższenie temperatury ciała[5].
Dick przebadał również osocze ludzkie. Nie znalazł żadnych przypadków przeciwciał neutralizujących działanie wirusa, podejrzewał jednak kontakt przebadanych ludzi z wirusem Zika bądź podobnym[5].
W 1948 udało się wyizolować wirusa z komarów Aedes africanus[2], natomiast w 1956 Boorman i Porterfield opisali metodę zainfekowania nim komara Aedes aegypti, z którego ZIKV udało się przenieść powtórnie na małpy[9].
Pierwsze doniesienia o zakażeniu tym wirusem człowieka pochodzą z 1952, kiedy to Smithburn znalazł przeciwciała neutralizujące go w surowicy krwi człowieka z Afryki Wschodniej[10]. W 1954 MacNamara doniósł o trzech przypadkach zachorowania przez człowieka podczas epidemii żółtaczki w Nigerii[11]. W 1964 Simpson opisał jako pierwszy przypadek choroby spowodowanej przez wirusa Zika u człowieka (u siebie samego)[2][12], a kolejny zdarzył się w 1973[13]. W końcu udało się wyizolować tego wirusa również od ludzi. Pisał o tym zespół Moore’a w 1975[14] oraz Fagbami dwa lata później. Oba badania przeprowadzono w Nigerii. Jak wynika z badań Fagbamiego przeprowadzonych w stanie Oyo w latach 1971–1975, znaczna część populacji Nigeryjczyków miała kontakt z wirusem. Test hamowania hemaglutynacji okazał się dodatni u 31% badanej próby. U 40% znaleziono w osoczu przeciwciała neutralizujące wirusa, jednak tylko u 9% z nich były one specyficzne jedynie dla ZIKV, reagowały zazwyczaj też z innymi flawiwirusami. Połowa osób odpornych na ZIKV posiadała przeciwciała monotypowe przeciwko samemu wirusowi bądź też razem z innymi flawiwirusami. Wynika z tego, że nie można utożsamiać odporności na wirusa z przeciwciałami reagującymi krzyżowo na flawiwirusy[10].
W wykonanych niedługo po odkryciu wirusa badaniach serologicznych specyficzne dlań przeciwciała wykryto u 6,1% przebadanej populacji w Ugandzie. Późniejsze badania wykrywały go u ludzi zamieszkujących Afrykę Wschodnią i Zachodnią[1]. Między 1951 a 1981 pojawiły się doniesienia z Ugandy, Tanzanii, Egiptu, Republiki Środkowoafrykańskiej, Sierra Leone i Gabonu[2]. Później do listy dołączył Senegal, na podstawie badań przeprowadzonych między 1988 a 1991, opublikowanych w 1993[15]. Badania serologiczne przeprowadzone w Azji wykryły przeciwciała u ludności Indii, Malezji, Indonezji, Pakistanu, Tajlandii, Wietnamu Północnego i Filipin[1]. Kolejne prace opisywały izolację wirusa z Aedes aegypti w Malezji, w okolicach miasta Bentong[16], komarów na Wybrzeżu Kości Słoniowej[2]. Wskazuje to na szeroki zasięg występowania ZIKV zajmującego tereny od Afryki do Azji Południowo-Wschodniej na północ od linii Wallace’a[1].
W 1981 Olson i współpracownicy opisali kilka przypadków zachorowań w Indonezji[17].
W 2006 zsekwencjonowano genom wirusa[7].
Do 2007 odnotowano mniej niż 10 przypadków zarażenia się tym wirusem u człowieka. W 1977 opisano 7 przypadków z indonezyjskiej Jawy[1]. W kwietniu 2007 wybuchła epidemia w Mikronezji, w stanie Yap[2]. Wirus na wyspę dostał się prawdopodobnie z zawleczonym tam przez człowieka komarem[3]. Pierwsze przypadki odnotowano 15 kwietnia. Donoszono o przypadkach wysypki, bólu i zapalenia stawów, zapalenia spojówek, poczucia gorączki[7]. Początkowo podejrzewano, że chodzi o wirusa powodującego dengę, choroba przebiegała bowiem podobnie do niej, a znalezione przeciwciała krzyżowo reagowały w teście na dengę[1]. Jednakże w rejonie tym dwukrotnie wcześniej doszło do epidemii tej choroby i lekarze dostrzegli pewne różnice. W czerwcu pobrane próbki wysłano do Centers for Disease Control and Prevention Arbovirus Diagnostic and Reference Laboratory w Fort Collins w amerykańskim stanie Kolorado[7]. Wykonane tam dokładniejsze badania z wykorzystaniem serologii, RT-PCR oraz sekwencjonowania DNA obaliły tę hipotezę, wskazując na wirusa Zika (chociaż jego materiał genetyczny w ok. 11% różnił się od szczepu MR766 wyizolowanego w Ugandzie w 1947, różnice te nie przekładają się na wysoką zmienność w sekwencji aminokwasów, która jest konserwatywna w 96%). Wydaje się, że wcześniejsza infekcja flawiwirusem nasila odpowiedź immunologiczną na ZIKV w klasie IgM[1]. Ostatnie przypadki zachorowań odnotowano 14 lipca. W sumie podczas tej epidemii odnotowano 185 zachorowań o podejrzewanej etiologii ZIKV, udało się ją potwierdzić w 49, co stanowi 26%. W dalszych 59 przypadkach, a więc 32%, ZIKV stanowił prawdopodobny czynnik chorobotwórczy. Daje to wskaźnik 14,6 na 1000 mieszkańców wyspy (zamieszkiwanej przez 7391 osób). Chorujący byli w wieku od 1 roku do 76 lat. Średnia wieku chorujących wyniosła 36 lat. Większość pacjentów (61%) stanowiły kobiety. Wirus częściej atakował osoby starsze niż młodsze. Zespół Duffy’ego zbadał również przeciwciała w kilkusetosobowej próbie mieszkańców wyspy. U prawie ¾ wykryto przeciwciała w klasie IgM (częściej u mężczyzn niż u kobiet), a 38% z tej grupy przyznało, że przeszło chorobę o objawach podobnych do wywoływanych przez ZIKV w czasie epidemii. Na podstawie tych badań oszacowano, że chorobę przeszło około 73% mieszkańców wyspy w wieku od 3 lat wzwyż, jednak tylko u 18% rozwinęły się objawy kliniczne[7]. Był to pierwszy przypadek, kiedy wirusa Zika znaleziono poza Azją bądź Afryką[2]. Nie wydaje się prawdopodobne, by wcześniej był on obecny na wyspie, raczej został nań świeżo zawleczony, być może przez jakiegoś naczelnego niebędącego człowiekiem (zamieszkują one pobliską wyspę Palau). Nic nie wiadomo jednak o przybyciu żadnego z nich na Yap, gdzie poza człowiekiem nie ma żadnych innych naczelnych. Pozostaje więc możliwość, że wirusa przeniósł komar bądź też sam człowiek, być może przybysz z Filipin, gdzie występuje ZIKV i skąd podróże na Yap nie należą do rzadkości[7]. W każdym razie może to oznaczać niebezpieczeństwo dalszego rozprzestrzeniania się go na inne wyspy Pacyfiku oraz Amerykę[2][7].
W 2008 Foy i współpracownicy donieśli o przypadku przeniesienia wirusa z jednego z dwóch wcześniej zaszczepionych przeciwko żółtej gorączce naukowców zarażonych w 2008 na północnym wschodzie Senegalu w okolicy Bandafassi na własną żonę po powrocie do domu, być może na drodze seksualnej[18].
Po epidemii z 2007 w rejonie Pacyfiku aż do 2013 nie było doniesień o nowych zachorowaniach. Pojawiły się one w październiku 2013 w Polinezji Francuskiej. W 2014 w tym kraju wybuchła epidemia, podczas której 11% populacji, czyli 28 tys. osób, szukało pomocy medycznej[19] (dane z lutego 2014[20]). Już wcześniej, gdy na początku roku odnotowano 5895 pacjentów, a całkowitą liczbę chorych szacowano na 19 tys., epidemię okrzyknięto największą spowodowaną przez arbowirusa innego niż wirus dengi w Polinezji Francuskiej[21]. Objawy obejmowały bóle stawów, zapalenia spojówek, wysypkę plamkowo-grudkową, niewysoką gorączkę. W listopadzie odnotowano przypadek zespołu Guillaina-Barrégo[19], opisany przez Oehlera i współpracowników[22]. Stwierdzono też po raz pierwszy przeniesienie wirusa z matki na płód[20]. Wirusa stwierdzono też u dwóch Japończyków wracających z Polinezji Francuskiej. Wyizolowany od jednego z tych pacjentów szczep wirusa przypominał znane z epidemii w Yap w 2007 (97,9% zgodności sekwencji nukleotydów) i ten z Kambodży z 2010 (99,1% zgodności sekwencji nukleotydów). Badania te świadczą o istnieniu grupy szczepów azjatyckich, odrębnych od ZIKV z Afryki[6]. Była to największa jak do tego czasu pory epidemia ZIKV[23]. Ponieważ wcześniej nie stwierdzono potrzeby hospitalizacji spowodowanej przez ZIKV, może to świadczyć o ewolucji wirusa w kierunku większej patogenności bądź o większej podatności podatności populacji Polinezji Francuskiej[22].
W sierpniu 2010 znaleziono wirusa w próbce krwi 3-latka z Kambodży, z prowincji Kampong Speu[24].
Kolejne zachorowania pod koniec 2013 pojawiały się w Nowej Kaledonii, na Wyspach Cooka, na Wyspie Wielkanocnej[19].
W 2015 doniesiono o epidemii w Brazylii[25], która rozpoczęła się na jeszcze pod koniec 2014 na północnym wschodzie kraju, gdzie stwierdzono chorobę przebiegającą z wysypką. Jednakże potwierdzenie etiologii nastąpiło dopiero w kwietniu 2015 wraz z wynikami RT-PCR ze stanów Bahia i Rio Grande do Norte. W styczniu 2016 wirus był już obecny w 22 z 26 jednostek administracyjnych tego kraju i we wszystkich jego 5 regionach[26]. To właśnie w Brazylii ZIKV po raz pierwszy skojarzono z ZIKV małogłowiem[25]. Pierwsze doniesienia napłynęły z północy kraju, ze stanu Pernambuco. Kolejne pochodziły z Paraíba i Rio Grande do Norte. W październiku 2015 brazylijskie ministerstwo zdrowia doniosło o wzroście częstości małogłowia. Do stycznia 2016 odnotowano już 3530 takich przypadków, podczas gdy przed wybuchem epidemii rocznie odnotowywano około 157[26].
W końcu wirus pojawił się w kolejnych państwach: w Ameryce (Barbados[27][28], Boliwia[28], Brazylia[28], Chile[29], Curaçao[30][28], Dominikana[31][28], Ekwador[27][28], Gujana[27][28], Gujana Francuska[32], Gwadelupa[28][33], Gwatemala[32], Haiti[28][32], Honduras[28][32], Jamajka[28], Kolumbia[28][32], Kostaryka[28], Martynika[28][32], Meksyk[28][32], Nikaragua[28], Panama[28][32], Paragwaj[34][32][28], Portoryko[28][32], Saint-Martin[28][33], Salwador[32], Stany Zjednoczone[35], Surinam[36][28][32], Wenezuela[28], Wyspy Dziewicze Stanów Zjednoczonych[28]), na południowym Pacyfiku (Samoa Amerykańskie[28], Samoa[28][37])[25], w Afryce (Republika Zielonego Przylądka[38]) i w Azji (Malediwy[38][28], Tajlandia[28]).
W 2016 pojawiły się zalecenia dla osób zajmujących się ochroną zdrowia dzieci i matek przebywających w czasie ciąży na terenach zajmowanych przez ZIKV[39].
Głównym żywicielem wirusa Zika jest człowiek rozumny[40].
ZIKV przenoszony jest przez komarowate. Znaleziono go u przedstawicieli gatunków Aedes africanus na terenie Afryki oraz Aedes aegypti z Malezji[1]. Nowsze badania pozwoliły znaleźć go także u Aedes apicoargenteus, Aedes luteocephalus, Aedes vitattus i Aedes furcifer[7]. Przenosić może go też Aedes albopictus[40]. Obecnie uznawany jest za najbardziej inwazyjny gatunek komara na świecie. Łatwo dostosowuje się on do różnorodnych warunków środowiskowych. Pochodzi w rzeczywistości z Azji Południowo-Wschodniej. Przez ostatnie 30 lat rozprzestrzenił się jednak w 28 krajach na wszystkich kontynentach oprócz Australii i Antarktydy[41], zaliczają się doń USA[40], a w Europie Albania, Bośnia i Hercegowina, Chorwacja, Czarnogóra, Francja, Grecja, Hiszpania, Słowenia, Szwajcaria, Włochy[41].
Epidemię w Polinezji Francuskiej mogły rozprzestrzeniać też Aedes polynesiensis[21].
Nie znaleziono go natomiast u Aedes hensili, dominującego gatunku komara na wyspie Yap, gdzie wybuchła epidemia w 2007[2]. Wykryto tam w sumie 12 gatunków komarów należących do 4 rodzajów, nie udało się jednak znaleźć u żadnego z nich wirusa, choć Aedes hensili wydawał się prawdopodobnym wektorem[7].
Po sztucznym zarażeniu Aedes aegypti początkowo, po 5–6 dniach, poziomy wirusa były niewielkie, następnie jednak rosły, od dnia 20 do 60 przekraczając małpią LD50 o pięć rzędów wielkości[9]. Czas inkubacji w organizmie owada trwa około 10 dni. Istnieją jednak poważne wątpliwości, czy komary mogą przenosić wirusa Zika na małpy w naturze. W badaniach Dicka komary nie wykazywały tendencji do kąsania trzymanych w klatkach małp[5][2].
W organizmie komara gnanego wiatrem wirus może przebyć nawet kilkaset kilometrów nad oceanem, choć w jego przenoszeniu rolę odgrywać też mogą pacjenci z wiremią[3].
Hayes nie zna żadnych rezerwuarów wirusa Zika poza naczelnymi, choć wymienia pojedyncze badanie stwierdzające go u gryzoni[2] – pracę autorstwa Darwisha et al opisującą badania przeprowadzone w Pakistanie[42]. Z drugiej strony przeciwciała reagujące z antygenami ZIKV znaleziono również u innych zwierząt, wśród których wymieniane są wół domowy, koza, owca, gnu, impala zwyczajna, bawolec krowi, hipopotamowate, zebry, słoniowate, lew afrykański, a także gryzonie[3].
Doniesienie o przeniesieniu wirusa przez naukowca na jego żonę w Kolorado sugeruje drogę seksualną (przez nasienie). W każdym razie wirus potrafi przenosić się bezpośrednio z człowieka na człowieka. Na tym obszarze występują pospolicie tylko komary z podrodzaju Aedimorphus (Aedes vexans), a ponadto Culex i Culiseta, podczas gdy wektory ZIKV zaliczają się do podrodzaju Stegomyia[18].
Ponadto wirus może przenosić się drogą perynatalną[19].
Nie ma informacji o przenoszeniu się ZIKV poprzez przetaczane preparaty krwiopochodne, chociaż mogą się w ten sposób przenosić inne flawiwirusy[23] (np. wirus Zachodniego Nilu[43]). W celu zminimalizowania potencjalnego ryzyka przeniesienia wirusa poprzez krew, wprowadzono dla dawców z Polinezji Francuskiej badania przesiewowe, w których 2,8% bezobjawowych dawców okazało się pozytywnych[19][23].
Informacje na temat patogenezy związanej z infekcją ZIKV są skąpe. Bazuje się tutaj na podobieństwach z innymi flawiwirusami. Hayes uważa, że wirus Zika namnaża się już w komórkach dendrytycznych w pobliżu miejsca, gdzie dostał się do organizmu człowieka. Następnie dostaje się do węzłów chłonnych. Jeszcze później powoduje wiremię (wykrywaną już w dniu pojawienia się choroby i przez następne 11 dni)[2]. Uczony odwołuje się tutaj do patomechanizmu choroby spowodowanej wirusem Zachodniego Nilu, również powodującej neuroinfekcję[44]. Zagadkowy jest również przedział w obrębie komórki zajmowany przez wirusa[2]. O ile bowiem flawiwirusy zajmują zazwyczaj cytoplazmę, to ZIKV znaleziony został przez Buckleya i Goulda w 1988 jedynie w jądrze[45].
Zespół Duffy’ego po zbadaniu epidemii na wyspie Yap stwierdził brak środowiskowych lub behawioralnych czynników ryzyka[7].
Profilaktyka chorób wirusowych przenoszonych przez komary obejmuje likwidację zbiorników z wodą, a także zabijanie larw komarów, zanim jeszcze rozpocznie się okres ich pojawu, jak też zabijanie osobników dorosłych. W przypadku wybuchu epidemii konieczne jest połączenie różnych metod[40].
Zaleca się, aby kobiety w ciąży nie podróżowały do rejonów, gdzie występują zakażenia wirusem Zika. Kobieta, po powrocie z takiego rejonu, jeżeli planuje zajście w ciążę, powinna wstrzymać się, aż upłynie okres ponad 8 tygodni.
U mężczyzn zakażonych wirusem Zika lub po powrocie z regionów zachorowań zaleca się przy stosunkach płciowych używanie prezerwatyw przez okres 6 miesięcy[46]
Szczególnie kobietom ciężarnym zaleca się unikanie ukąszeń przez komary poprzez odpowiedni ubiór (długie rękawy i spodnie), stosowanie repelentów oraz zabezpieczenie pomieszczeń przez ekrany bądź sieci powstrzymujące owady przed wtargnięciem[26].
Podczas epidemii w Polinezji Francuskiej wprowadzono badania krwi mające wykluczyć infekcję ZIKV u potencjalnych dawców. Próbki badano pod kątem obecności kwasów nukleinowych wirusa metodą RT-PCR. Przebadano wtedy 1505 dawców. U 42 z nich (2,8%) wynik był dodatni, co autorzy określili jako „niespodziewanie wysoką liczbę”. Po skontaktowaniu się z dodatnimi dawcami 11 z nich potwierdziło obecność objawów od 3 do 11 dni przed oddaniem krwi. Uzyskane wyniki wskazują na konieczność badania próbek krwi pod tym kątem, jak również na konieczność opracowania planów zagwarantowania dostępności bezpiecznej krwi w razie epidemii na terenach występowania Aedes[23].
W trzech czwartych[25] do czterech piątych zachorowań zakażenie przebiega bezobjawowo[39].
Jeśli już pojawią się objawy, są one zazwyczaj łagodne[25]. Okres wylęgania choroby wynosi przynajmniej 9 dni[18]. Objawy trwają zwykle od 2 do 7 dni[25]. Choroba cechuje się zwykle przebiegiem samoograniczającym[6], przypominającym grypę[22].
U człowieka ZIKV powoduje chorobę przebiegającą ze złym samopoczuciem, gorączką[1], wedle pierwszego opisu Simpsona z 1964 łagodną i krótko trwającą[12], wedle nowszych opisów wysoką[17], bólem i zawrotami głowy, bólem brzucha, brakiem apetytu oraz wysypką plamisto-grudkową. Zazwyczaj cechuje się ona łagodnym, samoograniczającym się przebiegiem[1]. Wedle opisu Simpsona najpierw pojawia się łagodny ból głowy. Następnego dnia pojawia się wysypka plamisto-grudkowa obejmująca twarz, szyję, tułów, kończyny górne – najpierw ramiona, potem dłonie i podeszwy stóp. Odnotowano pojawienie się złego samopoczucia, gorączki utrzymującej się do wieczora drugiego dnia choroby, bólu pleców. Wysypka również zaczęła zanikać drugiego wieczora, co zabrało jej jeszcze 2 dni – była więc najdłużej utrzymującym się objawem[2][12]. Natomiast wedle opisu Filipe i współpracowników (pacjent, przedtem zaszczepiony przeciwko gorączce żółtej, również był naukowcem i zaraził się podczas pracy laboratoryjnej) w przebiegu choroby szybko pojawia się gorączka do 38 °C z towarzyszącymi potami, bólem w okolicy zaoczodołowej, bólami szyi i stawów. Drugiego dnia temperatura spadła do 37,5 °C, by podnieść się w nocy do 38,3 °C. Objawy utrzymywały się do trzeciego dnia, po czym zaczęły ustępować. Powrót do zdrowia trwał tydzień. Co istotne, nie zaobserwowano wysypki[13]. Z kolei u naukowca zarażonego przez ukąszenie komara w Senegalu w 2008 początkowe objawy obejmowały obrzęk w okolicy kostek, wysypkę plamisto-grudkową na tułowiu, ból głowy i znaczne uczucie zmęczenia. Gorączka nie wystąpiła. Drugiego dnia dołączyły oszołomienie i dreszcze, a także bóle nadgarstków i stawów skokowych. Ponadto doszło do zapalenia prostaty objawiającego się dyzurią i bólem krocza. Trzeciego dnia złagodzeniu uległy wysypka i uczucie zmęczenia. Czwartego dnia zaobserwowano pojawienie się dwóch aftowatych owrzodzeń na wargach. Piątego dnia wystąpiła hematospermia, utrzymująca się odtąd przez 4 dni. Objawy utrzymywały się 6–9 dni po powrocie. U innego zarażonego choroba przebiegała podobnie, z tym że objawy stawowe dotyczyły także kolan. Piątego dnia od wystąpienia objawów u opisywanego pacjenta choroba ujawniła się u jego żony, prawdopodobnie wirus przeniósł się bezpośrednio, drogą seksualną. Wystąpiły u niej dreszcze, złe samopoczucie, ból głowy i mięśni, światłowstręt. Objawy te trwały 3 dni. Również nie doszło do gorączki. 5 dnia od zachorowania u kobiety pojawiła się wysypka na tułowiu, która następnego dnia rozprzestrzeniła się na szyję i biodra. Zaobserwowano również aftowate owrzodzenia warg. 6 dnia pojawiły się zmiany stawowe (nadgarstek, kciuk) i zapalenie spojówek. U jednego z chorych bóle nadgarstka utrzymywały się przez miesiąc, u pozostałych nawracały po ostrej fazie choroby[18].
Inaczej przedstawiały się zachorowania podczas epidemii w 2007. Odnotowano wysypkę, zapalenie spojówek, ból stawów[1], ból mięśni, obrzęk, wymioty[2][7]. Wiremię określono jako niską, choć nie przeprowadzono dokładniejszych pomiarów. Przy założeniu 200–500 cząsteczek DNA na wirion wiremię oszacowano na od 2 do 3,5 tysiąca wirionów na ml[1]. Doniesienie z Kambodży mówi też o bólu gardła i kaszlu[24].
Wobec tego typowy przebieg choroby opisuje się jako chorobę grypopodobną z niewysoką gorączką (zazwyczaj 37,8–38,5 °C), z bólami stawów, zwłaszcza niewielkich stawów dłoni i stóp, niekiedy z obrzękiem stawów, z bólami mięśni i głowy, zwłaszcza zaoczodołowymi, z zapaleniem spojówek oraz wysypką z grudkami i plamkami[22], z uczuciem zmęczenia[24], rzadziej ze świądem i objawami z układu pokarmowego, do których zaliczają się ból brzucha, zaparcia, biegunka, afty[22].
Kutsuna i inni (2014) prócz leukopenii zwrócili uwagę na trombocytopenię, którą stwierdzili w tej chorobie po raz pierwszy[6].
Dwa pierwsze udokumentowane przypadki wertykalnego przeniesienia wirusa Zika odnotowano podczas epidemii w Polinezji Francuskiej w grudniu 2013 i lutym 2014. Pierwsza z matek nawet nie gorączkowała, zaobserwowano jedynie swędzącą wysypkę, która pojawiła się na 2 dni przed porodem. W drugim przypadku matka w 5. dekadzie życia z cukrzycą ciążową urodziła noworodka z hipotrofią. Dopiero trzeciego dnia połogu rozwinęła łagodną gorączkę, swędzącą wysypkę i bóle mięśniowe. Wysypka pojawiła się również u dziecka, dołączyła do niej trombocytopenia. Pierwsze dziecko pozostało bezobjawowe. W obu przypadkach przebieg choroby był pomyślny. Rozważano transfer przezłożyskowy, podczas porodu, z mlekiem matki (gdzie również wykryto wirusa w stężeniu 2,9 × 104 i 205 × 104 cząsteczek RNA na ml, jednak w opisywanych przypadkach badania serologiczne nie wskazują na tę drogę)[20].
Pojawiły się też doniesienia wiążące infekcję ZIKV u ciężarnej z wrodzonym małogłowiem[25]. Podczas epidemii w Brazylii odnotowano zwiększenie liczby stwierdzanych przypadków małogłowia. Może do niego dochodzić zwłaszcza jeśli infekcja ZIKV wystąpiła na początku ciąży, w pierwszym trymestrze. W badaniach autorstwa Kleber de Oliveira et al. obejmujących 574 przypadki małogłowia 58,5% dzieci z mikrocefalią było dziewczynkami. Średni obwód głowy wyniósł 28 cm. Ponadto w 15 stanach objętych epidemią małogłowie występowało 2,80 na 10000 porodów, podczas gdy w stanach, gdzie nie potwierdzono kontaktu matek z wirusem, wartość ta wynosiła 0,60 na 10000. Najwyższy wynik pochodził ze stanu Pernambuco: 14,62. Odnotowywano tam do 4 noworodków z małogłowiem tygodniowo. Opisany w ten sposób związek ma jedynie charakter czasowy. Wykonano wobec tego badania mające za zadanie uprawdopodobnić hipotezę o wywoływaniu mikrocefalii przez wirus Zika. Od ciężarnych z Paraíba, u płodów których ultrasonograficznie wykazano mikrocefalię i zwapnienia w obrębie mózgowia, pobrano próbki płynu owodniowego. Następnie za pomocą RT-PCR udało się w nich zidentyfikować RNA wirusa. Później udało się także znaleźć wirusa w tkankach noworodków z małogłowiem, który zmarł niedługo po przyjściu na świat. Powiązania pomiędzy ZIKV a mikrocefalią wymagają jednakże dalszych badań, chociaż mówi się obecnie o zasadności unikania ukąszeń komarów przez ciężarne kobiety na terenie występowania wirusa[26].
Inne doniesienia łączą ZIKV z zespołem Guillaina-Barrégo[19]. Pierwszy taki przypadek (i w ogóle pierwszy przypadek, kiedy to leczenie zakażenia ZIKV wymagało hospitalizacji) opisał zespół Oehlera u kobiety na początku piątej dekady życia, która zachorowała w październiku 2013 w Polinezji Francuskiej. Pierwszym objawem neurologicznym były parestezje wszystkich kończyn. Po upływie doby pojawiło się osłabienie mięśni, a po trzech – tetrapareza bardziej nasilona na kończynach dolnych. Towarzyszyły jej rozlane bóle mięśniowe i asymetryczne porażenie twarzy, jak też brak głębokich odruchów ścięgnistych. Ponadto obecne były tachykardia, hipotensja ortostatyczna. EMG potwierdziło rozlaną demielinizację[22].
W badaniach Dicka z 1952 wirusa udało się wykryć jedynie w mózgu zakażonych myszy, pomimo zbadania licznych innych narządów wewnętrznych. Zaobserwowano degenerację neuronów. W ich obrębie znaleziono ciałka Cowdry’ego typu A[5].
Zmiany zapalne błon czy ependymy były minimalne[5].
Diagnostyka ZIKV opiera się na rozpoznaniu RNA wirusa za pomocą PCR lub poprzez stwierdzenie obecności swoistych przeciwciał skierowanych przeciw wirusowi za pomocą testu ELISA. Natomiast przeciwciała neutralizujące można wykryć dopiero od 5 dnia choroby. Badanie z wykorzystaniem PCR jest skuteczne, gdy bada się materiał pobrany przed 10. dniem choroby[2].
Jeśli ciężarna przebywała na terenie bytności wirusa ZIKV, zaleca się przeprowadzenie nie tylko badań matki, ale też płodu (USG)[39]. Badania w kierunku wirusa należy przeprowadzić także u dzieci[39]:
Chorobę wywoływaną przez wirusa Zika łatwo pomylić z dengą, chikungunyą oraz innymi chorobami wirusowymi przebiegającymi z wysypką i gorączką[25]. Jednakże zarówno denga, jak i chikungunya znane są lekarzom terenów endemicznych, a testy potwierdzające ich diagnozy wykonują liczne laboratoria. Natomiast gorączka Zika pozostaje chorobą mało znaną i tylko nieliczne ośrodki prowadzą diagnostykę w jej kierunku[3].
Nie opracowano skutecznego specyficznego leczenia przeciwwirusowego ZIKV ani żadnej skutecznej szczepionki przeciw wirusowi[47]. Leczenie choroby jest wyłącznie objawowe i obejmuje leczenie przeciwgorączkowe, przeciwbólowe, podawanie płynów i odpoczynek. Leczenie zakażenia wrodzonego również jest objawowe i opiera się na leczeniu stwierdzonych zaburzeń neurorozwojowych[39][48]. Brak specyficznego leczenia, jednak w łagodzeniu objawów pomocny może być paracetamol (acetaminofen)[47]. Pobyt w szpitalu rzadko bywa konieczny[49].
Zespół Guillaina-Barrégo w przebiegu zakażenia ZIKV leczy się immunoglobulinami dożylnie[22].
O Vírus da zica [1][2][3][4][5][6] ou vírus da zika[7][8][9][10] ou, ainda, vírus de Zika[11] (em inglês, Zika virus; abreviatura: ZIKV[12]) é um vírus do gênero Flavivirus. Em humanos, transmitido através da picada do mosquito Aedes aegypti, causa a doença também conhecida como zika[1][2][3][4][13][14] — que embora raramente acarrete complicações para seu portador, pode causar microcefalia congênita (quando adquirido por gestante, podendo prejudicar o feto em alguns casos).[9][15][16] O nome Zika tem sua origem na floresta de Zika, perto de Entebbe, capital da República de Uganda, onde o vírus foi isolado pela primeira vez em 1947. É relacionado aos vírus da dengue, da febre amarela e do Nilo Ocidental, os quais igualmente fazem parte da família Flaviviridae.[17]
A América Latina enfrentou um surto de vírus da zica em 2015. Suspeita-se que a entrada do vírus no Brasil tenha se dado durante a Copa do Mundo de 2014, quando o país recebeu turistas de várias partes do mundo, inclusive de áreas tropicais atingidas de forma mais intensa pelo vírus, como a África — onde surgiu — e a Polinésia Francesa na Oceania. No primeiro semestre de 2015, já havia casos confirmados em estados de todas as regiões do país. Com sintomas mais brandos que os da dengue e os da febre chikungunya (doenças também transmitidas pelo mosquito Aedes aegypti), a zica chegou a ser inicialmente ignorada pelas autoridades de saúde; porém há evidências de que a infecção pelo vírus da zica está associada a casos mais graves, como microcefalia congênita e síndrome de Guillain-Barré.[9][15][16][18]
Durante os surtos de microcefalia em 2015, pesquisas científicas sobre a relação entre o zika e a microcefalia ainda estavam em andamento, porém, já se sabe que o zika vírus está diretamente relacionado com casos de microcefalia.[19]
Junto com outros vírus da família, o vírus da zica é envelopado e icosaedral com um genoma de RNA não segmentado, de cadeia simples e senso positivo. É mais próximo ao vírus Spondweni e é um dos dois vírus do clado do Spondweni.[20]
O vírus foi isolado pela primeira vez em 1947 de um macaco reso (Macaca mulatta), capturado na floresta de Zika, em Entebbe, Uganda por cientistas do Uganda Virus Research Institute.[21] e foi isolado pela primeira vez em humanos em 1968, na Nigéria. De 1951 a 1981, evidências de infecção humana foram reportadas em outras nações africanas como Uganda, Tanzânia, Egito, República Centro-Africana, Serra Leoa e Gabão, assim como em partes da Ásia incluindo Índia, Paquistão, Malásia, Filipinas, Tailândia, Vietnã e Indonésia. [22] É transmitida por mosquitos e foi isolado de um número de espécies do gênero Aedes - Aedes aegypti, Aedes africanus, Aedes apicoargenteus, Aedes furcifer, Aedes luteocephalus e Aedes vitattus. Estudos mostram que o período de incubação extrínseca em mosquitos é de cerca de 10 dias.[22] Os hospedeiros vertebrados do vírus incluem macacos e humanos.[carece de fontes?]
Acredita-se que patogênese do vírus consista inicialmente em infectar células dendríticas próximas ao lugar de inoculação, e então espalham-se pelos nódulos linfáticos e na corrente sanguínea.[20] Em termos de replicação, os flavivírus tendem geralmente a se replicarem no citoplasma, mas os antígenos do vírus Zika foram encontrados em núcleos de células infectadas.[carece de fontes?]
Aproximadamente 80% das pessoas infectadas não desenvolvem manifestações clínicas. Nos casos em que há manifestação de sintomas, eles costumam incluir dores de cabeça leves, febre baixa, mal estar, dores leves nas articulações, conjuntivite, coceira e exantema maculopapular (erupção cutânea que não se eleva acima da superfície da pele), que, no geral, desaparecem espontaneamente após 3 a 7 dias.[8]
O primeiro caso bem documentado do vírus da zica foi em 1964, começando com uma leve dor de cabeça que progrediu para um exantema maculopapular, febre e dor nas costas. Com dois dias, a erupção começou a desaparecer, e com 3 dias, a febre desapareceu com apenas a erupção permanecendo.[23]
Não existe tratamento específico ou vacina para a infecção pelo vírus da zica. O tratamento recomendado para os casos sintomáticos é baseado no uso de paracetamol ou dipirona para o controle da febre e manejo da dor. No caso de erupções pruriginosas, os anti-histamínicos podem ser considerados. Não se recomenda o uso de ácido acetilsalicílico (AAS) e outros anti-inflamatórios, em função do risco aumentado de complicações hemorrágicas descritas nas infecções por outros flavivírus como o vírus da dengue.[8]
Dados recentes sugerem que recém-nascidos de mães que contraíram o vírus da zica durante a gestação estão sob risco de terem microcefalia. Casos da malformação congênita cresceram exponencialmente no Brasil em 2015, ano em que também cresceu o número de infectados pelo vírus da zica.[24][25]
Em Novembro de 2015, o vírus da zica foi isolado em um recém-nascido com microcefalia no estado do Ceará, Brasil. Desde Dezembro de 2015, existia a suspeita (já comprovada) de que a infecção pelo zica ultrapassa a placenta e ocasiona microcefalia e danos cerebrais.[26]
Em Janeiro de 2016, um bebê em Oahu, Estados Unidos nasceu com microcefalia, e foi o primeiro caso de dano cerebral causado pelo vírus da zica nos Estados Unidos. O bebê e a mãe testaram positivo para uma cepa do vírus. A mãe provavelmente adquiriu a doença em uma viagem ao Brasil em Maio de 2015 durante os primeiros estágios da gravidez. Apesar da gravidez ter progredido normalmente, a microcefalia do bebê só foi descoberta no nascimento.[27]
Em 20 de Janeiro de 2016, cientistas do estado do Paraná, Brasil, descobriram que o vírus é capaz de penetrar a placenta durante a gravidez. Restos do material genético do vírus da zica foi encontrado numa amostra de tecido da placenta de uma mulher que abortou devido à microcefalia.[28]
As principais causas da microcefalia são rubéola, toxoplasmose, sífilis e infecções causadas pelo citomegalovírus. Existem ainda poucos casos comprovados cientificamente da relação entre o zika e a microcefalia. Por enquanto, há muitos casos inferidos (sintomas similares aos do zika, mas sem comprovação por teste de material genético - PCR).[29]
Embora a dengue e a chikungunya sejam também febres causadas por um arbovírus, como a zika, nunca se estabeleceu (de acordo com a OMS) nenhuma relação entre a infecção por essas doenças e o nascimento de bebês com microcefalia congênita. O Brasil foi o primeiro país do mundo a registrar crescimento de casos de microcefalia, cerca de 150 casos em 2014 para mais de 3 800 em 2015. Dos 3 800 casos, apenas 134 foram associadas ao vírus zika.[29] A Polinésia Francesa também investigou e notou aumento dos casos de microcefalia após a notificação brasileira.[30]
Pesquisados brasileiros demonstraram que o zika pode infectar células troncos neurais humanas e tem efeitos deletérios em neuroesferas e organóides cerebrais.[31]
Em maio de 2016, utilizando-se modelos experimentais em camundongos, foi provado que o vírus da zika pode causar danos a placenta e ao feto [32]
Em fevereiro de 2018, uma pesquisa realizada com gêmeos demonstrou que há fatores de susceptibilidade genética para ocorrências de microcefalia. A mesma pesquisa demonstrou que caso a mãe seja infectada com o zika vírus, teve como estimativa da chance do bebê nascer com microcefalia sendo de 6 a 12%[33]
O primeiro surto da doença fora da África e Sudeste Asiático foi em abril de 2007, na ilha de Yap nos Estados Federados da Micronésia na Oceania. O vírus se caracterizou pelas erupções cutâneas, conjuntivite, e artralgia, e inicialmente se pensou que era dengue. Os vírus chicungunha e do rio Ross também foram tomados como suspeitos.[34] Porém, amostras de soro dos pacientes na fase aguda da doença continham RNA do vírus Zika. A processo infeccioso da febre Zika foi relativamente leve: houve 49 casos confirmados, 59 não confirmados, nenhuma morte ou microcefalia congênita.[35]
O primeiro surto do vírus Zika nas Américas foi confirmado em abril de 2015, no Brasil. Na cidade de Salvador, capital do estado da Bahia, as autoridades de saúde confirmaram que uma doença até então desconhecida que afeta cerca de 500 pacientes com sintomas semelhantes aos da gripe, seguido de exantema e artralgia é realmente um surto em curso da febre Zika, como provado pela técnica de RT-PCR por pesquisadores da Universidade Federal da Bahia. As autoridades locais ligaram o surto recente ao aumento do fluxo de visitantes estrangeiros motivados pela Copa do Mundo FIFA de 2014, juntamente com a grande população de insetos vetores Aedes aegypti e Aedes albopictus que habitam a região tropical. O surto segue um padrão semelhante ao também recente surto do vírus chicungunha na mesma região, outra doença até então desconhecida à população local.[36]
O vírus Zika pode ser considerado um patógeno emergente, visto que se espalhou dos Estados Federados da Micronésia pela primeira vez em 2007, para Polinésia Francesa em 2013 e Nova Caledônia em 2014. Até o momento, 1.434 casos de microcefalia em decorrência da doença já confirmados e mais 3.257 em avaliação.
O vírus foi isolado pela primeira vez em 1947 por cientistas que, pesquisando a febre amarela, capturaram um macaco reso na floresta de Zika (zika significando, na língua Luganda, "invadido", no sentido de "vegetação que cresceu demais e tomou conta do lugar"[37]), próximo ao Instituto de Pesquisa Virológica do leste africano, em Entebbe, capital da República de Uganda. A febre se desenvolveu no macaco e os pesquisadores isolaram de seu soro um agente transmissível que foi descrito como Vírus Zika pela primeira vez em 1952. Junto com a descrição do vírus, os cientistas financiados pela Fundação Rockefeller (Dr. Jordi Casals) forneceram o vírus para uma organização que mantém culturas de organismos para laboratórios.[38] O vírus não foi patenteado pela Fundação.[38] Foi subsequentemente isolado num humano na Nigéria em 1954. Da sua descoberta até 2007, casos confirmados de infecção com o vírus Zika na África e Sudeste da Ásia eram raros. Em 2007 porém, uma forte epidemia ocorreu na ilha Yap, Micronésia. Mais recentemente, epidemias ocorreram na Polinésia, ilha da Páscoa, Ilhas Cook e Nova Caledônia.[39]
Em 2009, se verificou que o vírus Zika pode ser sexualmente transmitido entre humanos. Professor Brian Foy, biólogo universitário da Colorado State University no Laboratório de Doenças Infecciosas e Transmitidas por Artropódes, visitou o Senegal para estudar mosquitos e foi picado em algumas ocasiões na sua pequisa. Alguns dias depois de voltar aos EUA ele ficou doente com febre Zika, mas não sem antes ter relações sexuais com sua esposa. Sua esposa subsequentemente mostrou sinais de infecção com febre Zika,além de extrema sensibilidade à luz. Foy é a primeira pessoa conhecida a ter passado um vírus vindo de insetos a outro ser humano via contato sexual.[40]
As formas conhecidas atualmente para a prevenção contra a Zika são as mesmas da Dengue, a principal delas é evitar a proliferação do mosquito Aedes aegypti, eliminando potenciais criadouros com água parada. Além disso, é recomendado o uso de inseticidas e repelentes de mosquitos. [41]
A Organização Mundial da Saúde sugeriu em 2016 que deveria ser priorizado o desenvolvimento de vacinas inativadas, que são seguras para mulheres grávidas.[42]
Em março de 2016, 18 empresas e instituições estavam desenvolvendo vacinas contra o Zika, mas afirmam que o desenvolvimento é demorado, e a vacina pode levar cerca de 10 anos até se tornar amplamente disponível.[42][43]
Em junho de 2016, o primeiro teste clínico em humanos para uma vacina para o Zika foi aprovado pelo FDA.[44] E em 2017, foram iniciados testes clínicos com vacinas de DNA,[45] como vacinas inativadas e de subunidade.[46]
Um mecanismo proposto para combate à proliferação de vetores de doenças como a Dengue e a Zica consiste no desenvolvimento e liberação de mosquitos geneticamente modificados. Em uma das modificações propostas e em fase de testes, os mosquitos, ao se reproduzirem, produzem apenas larvas inviáveis. Outro mecanismo sendo desenvolvido envolve o método chamado de genética dirigida, e envolve criar uma variante genética dos mosquitos nos quais os vírus ou parasitas são incapazes de sobreviver.[47]
Após ter sido confirmada a relação entre o vírus e os casos de microcefalia, foram desenvolvidas pesquisas na Universidade Estadual de Campinas que mostraram que esse vírus pode combater o glioblastoma e que pode inibir o crescimento de tumores associados ao câncer de próstata.[48]
|coautores= (ajuda) |Editora= (ajuda) O Vírus da zica ou vírus da zika ou, ainda, vírus de Zika (em inglês, Zika virus; abreviatura: ZIKV) é um vírus do gênero Flavivirus. Em humanos, transmitido através da picada do mosquito Aedes aegypti, causa a doença também conhecida como zika — que embora raramente acarrete complicações para seu portador, pode causar microcefalia congênita (quando adquirido por gestante, podendo prejudicar o feto em alguns casos). O nome Zika tem sua origem na floresta de Zika, perto de Entebbe, capital da República de Uganda, onde o vírus foi isolado pela primeira vez em 1947. É relacionado aos vírus da dengue, da febre amarela e do Nilo Ocidental, os quais igualmente fazem parte da família Flaviviridae.
A América Latina enfrentou um surto de vírus da zica em 2015. Suspeita-se que a entrada do vírus no Brasil tenha se dado durante a Copa do Mundo de 2014, quando o país recebeu turistas de várias partes do mundo, inclusive de áreas tropicais atingidas de forma mais intensa pelo vírus, como a África — onde surgiu — e a Polinésia Francesa na Oceania. No primeiro semestre de 2015, já havia casos confirmados em estados de todas as regiões do país. Com sintomas mais brandos que os da dengue e os da febre chikungunya (doenças também transmitidas pelo mosquito Aedes aegypti), a zica chegou a ser inicialmente ignorada pelas autoridades de saúde; porém há evidências de que a infecção pelo vírus da zica está associada a casos mais graves, como microcefalia congênita e síndrome de Guillain-Barré.
Durante os surtos de microcefalia em 2015, pesquisas científicas sobre a relação entre o zika e a microcefalia ainda estavam em andamento, porém, já se sabe que o zika vírus está diretamente relacionado com casos de microcefalia.
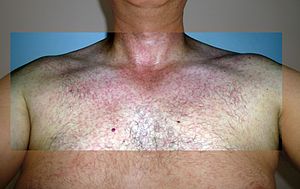
Virusul Zika este un virus ARN monocatenar cu sens pozitiv din genul Flavivirus (familia Flaviviridae) identificat prima dată în 1947 în pădurea tropicală Zika din Uganda (de unde și numele lui). El provoacă la om o boală infecțioasă virală, numită febra Zika, transmisă prin înțepătura unui țânțar din genul Aedes infectat cu acest virus.[1][2][3]
Timp de mai multe decenii virusul Zika a fost semnalat doar sporadic în Africa și Asia. Epidemiile de febră Zika au fost raportate pentru prima dată în regiunea pacifică în 2007 (insula Yap) și 2013 (Polinezia Franceză), apoi în 2015, în Africa (Capul Verde) și America de Sud (Brazilia și Columbia). De aici, virusul Zika s-a răspândit rapid în mai multe țări din America de Sud și America Centrală, ajungând să fie semnalat în 13 țări la începutul anului 2016.[1][2][3] Până la 29 iulie 2016, 42 de țări și teritorii din America au confirmat transmiterea locală prin țânțari a virusului Zika.[4] Organizația Mondială a Sănătății (OMS) a anunțat pe 28 ianuarie 2016 că 3-4 milioane de persoane ar putea fi infectate în acest an cu virusul Zika în America.[5]
În Europa nu s-a confirmat transmiterea virusului Zika prin țânțari, însă au fost semnalate mai multe cazuri de import de infecție cu acest virus în mai multe țări, inclusiv în România. Primul caz de infectare cu virusul Zika a fost confirmat în România pe 12 iulie 2016, fiind vorba de o femeie de 27 de ani, din București, care a călătorit în Martinica.[6] Al doilea caz de virus Zika din România a fost identificat pe 19 iulie 2016 la un băiat în vârstă de 10 ani, care locuiește împreună cu familia sa în Guyana Franceză de aproape doi ani și care a venit în România, în vizită la rude.[7][8] În data de 27 iulie 2016 Ministerul Sănătății a confirmat un al treilea caz de import de virus Zika în România. Este vorba despre un bărbat în vârstă de 36 ani, din Cluj-Napoca care a călătorit în Republica Dominicană.[9]
Există două cicluri de transmitere a virusului Zika. Primul, ciclul silvatic (sau selvatic), implică un rezervor animal, primatele neumane, și țânțarii vectori, Aedes africanus, Aedes luteocephalus, omul fiind în cazul acesta numai o gazdă "accidentală", el fiind înțepat întâmplător în timpul deplasărilor prin pădurile tropicale și savanelor limitrofe, de un țânțar contaminat cu virusul Zika; acest ciclu de transmitere este responsabil de majoritatea cazurilor sporadice. Al doilea ciclu este de tip urban; virusul se transmite de la om la om prin intermediul unor țânțari vectori ca Aedes aegypti (țânțarul febrei galbene) și Aedes albopictus (țânțarul tigru asiatic); acești 2 țânțari din genul Aedes, spre deosebire de cei din genul Culex, înțeapă în timpul zilei și sunt antropofili, trăind pe lângă așezărilor umane, mai ales în orașe. Cele mai multe epidemii actuale din America Latină se propagă prin intermediul țânțarului Aedes aegypti. Prezența în sânge (viremia) a virusului Zika este relativ scurtă (3-5 zile), însă virionii au fost detectați în mai multe alte fluide biologice, inclusiv în urină (la 10 zile postinfecție), salivă (3-5 zile) și spermă (la 15 zile după infecție). Cu toate că principala cale de transmitere a infecției cu virusul Zika la om este vectorială, prin intermediul înțepăturilor de țânțari, au fost raportate cazuri de transmitere nevectorială: perinatală (de la mamă la făt pe cale transplacentară sau în timpul delivrenței), prin transfuzii de sânge sau pe cale sexuală.
Perioada de incubație este de 3-12 zile după înțepătura unui țânțar infectat. Majoritatea infecțiilor provocate de virusul Zika sunt asimptomatice (60-80%). În cazurile simptomatice, simptomele bolii sunt de obicei ușoare și dispar în 2-7 zile, fără decese.[10] Principalele simptome sunt erupția cutanată (un exantem macular sau papular care apare inițial pe față și apoi se extinde pe tot corpul), febra moderată, artralgiile, mialgiile, cefaleea, conjunctivita nepurulentă cu hiperemie conjunctivală. Au fost descrise 2 complicații neurologice alarmante, probabil determinate de virusul Zika: sindromul Guillain-Barré (o paralizie ascendentă simetrică care atinge cele patru membre și uneori nervii cranieni) și microcefalia (capul anormal de mic) nou-născuților.[1][2][3]
Ca și în cazul majorității infecțiilor provocate de alți arbovirusuri, diagnosticul biologic de laborator al infecției cu virusul Zika recurge la tehnici virologice directe (prin RT-PCR), atunci când pacientul este consultat în primele zile după instalarea semnelor clinice (în general, până în 5-7 zi), și după aceste 5-7 zile la tehnici serologice (ELISA) care permit cel mai adesea reconfirmarea ulterioară a diagnosticului.
Până în prezent, nu există nici un tratament antiviral specific sau vaccin disponibil împotriva infecției cu virusul Zika. Tratamentul este numai simptomatic: analgezice-antipiretice (paracetamol pentru febră și durere), antihistaminice (pentru erupții cutanate pruriginoase). Tratamentul cu acid acetilsalicilic (aspirina) și medicamente antiinflamatoare nesteroidiene (cum ar fi ibuprofenul și naproxenul) trebuie evitat până la excluderea diagnosticului de denga, pentru a reduce riscul de hemoragie cunoscut pentru denga. Lupta antivectorială rămâne cel mai eficient mijloc de combatere a acestui virus. Controlul vectorial include utilizarea insecticidelor care distrug țânțarii adulți, distrugerea larvelor și asanarea zonelor de înmulțire a țânțarilor folosind larvicide chimice sau biologice (bacteria Bacillus thuringiensis, ciuperca Beauveria bassiana, peștele Gambusia affinis holbrooki), eliberări masive de țânțari vectori Aedes aegypti de sex masculin modificați transgenic în scopul procreării unei progenituri neviabile, dezinsecția sistematică a locuințelor și adăposturilor animale; dezinsecția cu insecticide a avioanelor, vapoarelor ce sosesc din teritorii endemice. Măsurile individuale includ: utilizarea de plase în jurul patului și a geamurile locuințelor; folosirea de substanțe repelente și îmbrăcăminte adecvată (pantaloni lungi și bluze, cămăși cu mâneca lungă) când se pătrunde în teritorii cu risc crescut. Femeile însărcinate sau care doresc sa rămână însărcinate în perioada următoare trebuie să evite călătoriile în țări cu transmitere locala a virusului Zika.[1][2][3]
Doar puțin peste 100 de articole de specialitate au fost publicate din 1952 până în 2015 despre virusul Zika, din care jumătate în 2015, majoritatea lor fiind analize epidemiologice. Prin urmare se știe foarte puțin despre tropismul, ciclul sau patogeneza virusului Zika.
Virusul care cauzează boala a fost prima oară identificat în anul 1947.[11] Primele epidemii în rândul oamenilor au fost raportate în anul 2007, în Statele Federate ale Microneziei.[12] Până în ianuarie 2016, boala apăruse în douăzeci de regiuni ale continentului American.[12] A mai fost semnalată și în Africa, Asia și regiunea Pacificului.[13] Ca urmare a epidemiei izbucnite în Brazilia în anul 2015,în luna februarie 2016, Organizația Mondială a Sănătății a declarat boala drept o urgență de sănătate publică de interes internațional.[14]
Deși nu există un tratament specific, paracetamolul (acetaminofenul)ar putea ajuta la ameliorarea simptomelor.[12] Spitalizarea nu este necesară în cele mai multe cazuri.[10]
Prevenția presupune reducerea numărului de înțepături de țânțari în zonele afectate de boală.[12] Măsurile de prevenție includ utilizarea unor produse împotriva insectelor, folosirea de îmbrăcăminte care să acopere o porțiune cât mai mare a corpului, plase împotriva țânțarilor și eliminarea zonelor cu apă stătătoare, deoarece acestea sunt locurile în care țânțarii se reproduc.[13] Din cauza epidemiei, în anul 2015, oficialii din domeniul sănătății din Brazilia au recomandat cuplurilor să evite sarcinile, iar femeile însărcinate au fost sfătuite să nu călătorească în zonele afectate de epidemie.[15][12]
Nu există niciun vaccin eficient.[12]
Virusul Zika este un virus ARN monocatenar cu sens pozitiv din genul Flavivirus (familia Flaviviridae) identificat prima dată în 1947 în pădurea tropicală Zika din Uganda (de unde și numele lui). El provoacă la om o boală infecțioasă virală, numită febra Zika, transmisă prin înțepătura unui țânțar din genul Aedes infectat cu acest virus.
Timp de mai multe decenii virusul Zika a fost semnalat doar sporadic în Africa și Asia. Epidemiile de febră Zika au fost raportate pentru prima dată în regiunea pacifică în 2007 (insula Yap) și 2013 (Polinezia Franceză), apoi în 2015, în Africa (Capul Verde) și America de Sud (Brazilia și Columbia). De aici, virusul Zika s-a răspândit rapid în mai multe țări din America de Sud și America Centrală, ajungând să fie semnalat în 13 țări la începutul anului 2016. Până la 29 iulie 2016, 42 de țări și teritorii din America au confirmat transmiterea locală prin țânțari a virusului Zika. Organizația Mondială a Sănătății (OMS) a anunțat pe 28 ianuarie 2016 că 3-4 milioane de persoane ar putea fi infectate în acest an cu virusul Zika în America.
În Europa nu s-a confirmat transmiterea virusului Zika prin țânțari, însă au fost semnalate mai multe cazuri de import de infecție cu acest virus în mai multe țări, inclusiv în România. Primul caz de infectare cu virusul Zika a fost confirmat în România pe 12 iulie 2016, fiind vorba de o femeie de 27 de ani, din București, care a călătorit în Martinica. Al doilea caz de virus Zika din România a fost identificat pe 19 iulie 2016 la un băiat în vârstă de 10 ani, care locuiește împreună cu familia sa în Guyana Franceză de aproape doi ani și care a venit în România, în vizită la rude. În data de 27 iulie 2016 Ministerul Sănătății a confirmat un al treilea caz de import de virus Zika în România. Este vorba despre un bărbat în vârstă de 36 ani, din Cluj-Napoca care a călătorit în Republica Dominicană.
Există două cicluri de transmitere a virusului Zika. Primul, ciclul silvatic (sau selvatic), implică un rezervor animal, primatele neumane, și țânțarii vectori, Aedes africanus, Aedes luteocephalus, omul fiind în cazul acesta numai o gazdă "accidentală", el fiind înțepat întâmplător în timpul deplasărilor prin pădurile tropicale și savanelor limitrofe, de un țânțar contaminat cu virusul Zika; acest ciclu de transmitere este responsabil de majoritatea cazurilor sporadice. Al doilea ciclu este de tip urban; virusul se transmite de la om la om prin intermediul unor țânțari vectori ca Aedes aegypti (țânțarul febrei galbene) și Aedes albopictus (țânțarul tigru asiatic); acești 2 țânțari din genul Aedes, spre deosebire de cei din genul Culex, înțeapă în timpul zilei și sunt antropofili, trăind pe lângă așezărilor umane, mai ales în orașe. Cele mai multe epidemii actuale din America Latină se propagă prin intermediul țânțarului Aedes aegypti. Prezența în sânge (viremia) a virusului Zika este relativ scurtă (3-5 zile), însă virionii au fost detectați în mai multe alte fluide biologice, inclusiv în urină (la 10 zile postinfecție), salivă (3-5 zile) și spermă (la 15 zile după infecție). Cu toate că principala cale de transmitere a infecției cu virusul Zika la om este vectorială, prin intermediul înțepăturilor de țânțari, au fost raportate cazuri de transmitere nevectorială: perinatală (de la mamă la făt pe cale transplacentară sau în timpul delivrenței), prin transfuzii de sânge sau pe cale sexuală.
Perioada de incubație este de 3-12 zile după înțepătura unui țânțar infectat. Majoritatea infecțiilor provocate de virusul Zika sunt asimptomatice (60-80%). În cazurile simptomatice, simptomele bolii sunt de obicei ușoare și dispar în 2-7 zile, fără decese. Principalele simptome sunt erupția cutanată (un exantem macular sau papular care apare inițial pe față și apoi se extinde pe tot corpul), febra moderată, artralgiile, mialgiile, cefaleea, conjunctivita nepurulentă cu hiperemie conjunctivală. Au fost descrise 2 complicații neurologice alarmante, probabil determinate de virusul Zika: sindromul Guillain-Barré (o paralizie ascendentă simetrică care atinge cele patru membre și uneori nervii cranieni) și microcefalia (capul anormal de mic) nou-născuților.
Ca și în cazul majorității infecțiilor provocate de alți arbovirusuri, diagnosticul biologic de laborator al infecției cu virusul Zika recurge la tehnici virologice directe (prin RT-PCR), atunci când pacientul este consultat în primele zile după instalarea semnelor clinice (în general, până în 5-7 zi), și după aceste 5-7 zile la tehnici serologice (ELISA) care permit cel mai adesea reconfirmarea ulterioară a diagnosticului.
Până în prezent, nu există nici un tratament antiviral specific sau vaccin disponibil împotriva infecției cu virusul Zika. Tratamentul este numai simptomatic: analgezice-antipiretice (paracetamol pentru febră și durere), antihistaminice (pentru erupții cutanate pruriginoase). Tratamentul cu acid acetilsalicilic (aspirina) și medicamente antiinflamatoare nesteroidiene (cum ar fi ibuprofenul și naproxenul) trebuie evitat până la excluderea diagnosticului de denga, pentru a reduce riscul de hemoragie cunoscut pentru denga. Lupta antivectorială rămâne cel mai eficient mijloc de combatere a acestui virus. Controlul vectorial include utilizarea insecticidelor care distrug țânțarii adulți, distrugerea larvelor și asanarea zonelor de înmulțire a țânțarilor folosind larvicide chimice sau biologice (bacteria Bacillus thuringiensis, ciuperca Beauveria bassiana, peștele Gambusia affinis holbrooki), eliberări masive de țânțari vectori Aedes aegypti de sex masculin modificați transgenic în scopul procreării unei progenituri neviabile, dezinsecția sistematică a locuințelor și adăposturilor animale; dezinsecția cu insecticide a avioanelor, vapoarelor ce sosesc din teritorii endemice. Măsurile individuale includ: utilizarea de plase în jurul patului și a geamurile locuințelor; folosirea de substanțe repelente și îmbrăcăminte adecvată (pantaloni lungi și bluze, cămăși cu mâneca lungă) când se pătrunde în teritorii cu risc crescut. Femeile însărcinate sau care doresc sa rămână însărcinate în perioada următoare trebuie să evite călătoriile în țări cu transmitere locala a virusului Zika.
Doar puțin peste 100 de articole de specialitate au fost publicate din 1952 până în 2015 despre virusul Zika, din care jumătate în 2015, majoritatea lor fiind analize epidemiologice. Prin urmare se știe foarte puțin despre tropismul, ciclul sau patogeneza virusului Zika.
Vírus Zika alebo (nesprávne) Zikov vírus[1] patrí do čeľade Flaviviridae a je prenášaný komármi rodu Aedes.[2] Inkubácia vírusu v tele nakazeného trvá maximálne 14 dní, klinické príznaky infekcie bývajú mierne. U 80 % nakazených osôb sa neprejavia žiadne symptómy. Zvyšných 20 % nakazených môže prekonať horúčku Zika, ktorá má podobný priebeh ako chrípka. Okrem vysokých teplôt sa prejavuje vyrážkami šíriacimi sa z tváre na ostatné časti tela, bolesťami hlavy a kĺbov.[3] Riziko môže predstavovať najmä pre tehotné ženy, nakoľko bola zaznamenaná možná súvislosť so zvýšeným výskytom ťažkej vývojovej poruchy, mikrocefálie, u novorodencov.[2]
Vírus bol prvýkrát identifikovaný v roku 1947 u opíc v Ugande, v roku 1952 aj u človeka.[2] V súčasnosti bol zachytený vo viac ako dvadsiatich krajinách, medzi ktoré patria najmä juho a stredoamerické štáty: napr. Brazília, Kolumbia, Ekvádor, Paraguaj, Panama, Mexiko.[4]
V Brazílii bol najväčší výskyt zaznamenaný na severovýchode krajiny. Prípady nákazy sa však objavili i na juhovýchodnom pobreží, kde se nachádza bývalé hlavné mesto krajiny – Rio de Janeiro, v ktorom sa v auguste 2016 konali letné olympijské hry.
Vírusu Zika je prisudzovaný zvýšený výskyt mikrocefálie, ktorá sa prejavuje zakrpatením, či predčasným ukončením rastu mozgu. V roku 2014 sa v Brazílii s touto vadou narodilo 150 detí, o rok neskôr ich bolo už 2 700.[5] V niektorých častiach Brazílie bol v tejto súvislosti vyhlásený výnimočný stav. Párom plánujúcim narodenie potomka, lekári odporučili odklad rodičovstva.[6][4]
Proti ochoreniu neexistuje liek, brazílska vláda sa však usiluje o urýchlenie vývoja vakcíny. Jedinou prevenciou preto zostávajú tradičné formy ochrany pred uštipnutím komára. Armáda a zdravotníci likvidujú stojaté vody, v ktorých sa komáre množia.[7]
Vírus Zika alebo (nesprávne) Zikov vírus patrí do čeľade Flaviviridae a je prenášaný komármi rodu Aedes. Inkubácia vírusu v tele nakazeného trvá maximálne 14 dní, klinické príznaky infekcie bývajú mierne. U 80 % nakazených osôb sa neprejavia žiadne symptómy. Zvyšných 20 % nakazených môže prekonať horúčku Zika, ktorá má podobný priebeh ako chrípka. Okrem vysokých teplôt sa prejavuje vyrážkami šíriacimi sa z tváre na ostatné časti tela, bolesťami hlavy a kĺbov. Riziko môže predstavovať najmä pre tehotné ženy, nakoľko bola zaznamenaná možná súvislosť so zvýšeným výskytom ťažkej vývojovej poruchy, mikrocefálie, u novorodencov.
Virus zika je virus iz rodu flavivirusov, ki se prenaša preko vboda komarjev iz rodu Aedes. Slednji prenašajo tudi druge nalezljive bolezni, kot sta denga in čikungunja.[1] Pri ljudeh povzroča blago okužbo, imenovano tudi vročica zika, ki je bila od 50-ih let prejšnjega stoletja značilna le za ozek ekvatorialni pas od Afrike do Azije. Leta 2014 se je bolezen razširila proti vzhodu, na območje Tihega ocena do Francoske Polinezije in dalje do Velikonočnega otoka, leta 2015 pa v Južno in Srednjo Ameriko ter Karibsko otočje, kjer povzroča še vedno trajajoč izbruh, ki so ga že uvrstili med pandemije.[2] Bolezen poteka kot blaga oblika vročice denge,[3] pri kateri se priporoča počitek,[4] zanjo pa ne obstajajo specifična zdravila ali cepiva.[4]
Vročica zika je sorodna z rumeno mrzlico in vročico zahodnega Nila, ki ju pa povzročata druga vrsta flavivirusov, vendar se prenašata prav tako s komarji.[3] Okužbo nosečnic povezujejo z možnostjo povzročitve mikrocefalije pri novorojenčkih.[5][6] Posledično je januarja 2016 ameriški Center za nadzor bolezni (CDC) izdal opozorila za potovanje v prizadete države s smernicami za preventivne ukrepe in priporočilom za opustitev potovanja ter posebna priporočila za nosečnice.[7][8][9] Vlade več držav s tega območja so svetovale ženskam, naj odložijo nosečnost, če jo načrtujejo.[10]
Kot drugi virusi iz družine flavivirusov je tudi virus zika ikozaedričen virus z ovojnico, ki ima nesegmentiran genom v obliki enoverižne, pozitivno usmerjene RNK.[11][12]
Virus so prvič osamili leta 1947 iz opice rezus iz gozda Zika v Ugandi, iz človeka pa so ga prvič osamili leta 1968 v Nigeriji.[13] Do leta 1981 so o okužbi ljudi poročali iz več afriških držav, med drugim iz Ugande, Tanzanije, Egipta, Srednjeafriške republike, Sierre Leone in Gabona, ter iz nekaterih azijskih držav, na primer Indije, Malezije, Filipinov, Tajske, Vietnama in Indonezije.[13]
Patogenetski procesi v telesu naj bi se začeli z okužbo dendritičnih celic v bližini mesta vstopa virusa v telo; okužba naj bi se nato prenesla do bližnjih bezgavk ter v krvni obtok.[11] Flavivirusi se na plošno množijo v celični citoplazmi, vendar so pri virusu zika odkrili antigene v celičnem jedru okužene celice.[14]
Virus zika prenašajo komarji, ki so dejavni preko dneva; virus so osamili iz različnih vrst komarja iz rodu Aedes (A. aegypti, A. africanus, A. apicoargenteus, A. furcifer, A. hensilli, A. luteocephalus, A. vitattus). Študije so pokazale, da inkubacijska doba okužbe v komarju traja okoli 10 dni.[13] Komarji nato okužijo sesalčje gostitelje, najpogosteje opice in ljudi. Pred letom 2007, ko se je začela trenutna pandemija, je veljalo, da so izbruhi bolezni med ljudmi, tudi na zelo enzootičnih območjih, redki.[15]
Leta 2009 so zabeležili prvi spolni prenos okužbe z virusom zika. Ameriški biolog, ki je obiskal Senegal z namenom preučevanja komarjev, je po povratku v ZDA zbolel za vročico zika. Pred izbruhom simptomov je imel nezaščiten spolni odnos z ženo, ki je nato prav tako zbolela.[16][17]
Leta 2015 so RNK virusa zika zaznali v plodovnici dveh plodov, kar je pokazalo na možnost prehoda virusa z okužene matere preko posteljice na nerojenega otroka.[18] 20. januarja 2016 so znanstveniki v Braziliji zaznali dednino virusa zika v posteljici ženske, pri kateri so opravili splav zaradi mikrocefalije pri plodu, kar je potrdilo domnevo, da virus prehaja posteljico.[19]
Okužba pogosto poteka povsem brez simptomov, določen delež (okoli 20 %) okuženih pa razvije simptome in znake okužbe z virusom zika. Potek bolezni je pri večini lahek, težave z zdravjem običajno izzvenijo v nekaj dneh ali največ po enem tednu. O smrtih zaradi okužbe z virusom zika ni poročil.[1] 00 Bolezenski znaki se pojavijo 3 do 7 dni po vbodu okuženega komarja.[1] Pogosti simptomi okužbe so blag glavobol, makulopapulozni izpuščaj, vročina, utrujenost, vnetje očesne veznice in bolečine v sklepih.[13]
Zdravila ali cepiva, ki bi preprečila okužbo, niso na voljo. Simptomi se lahko lajšajo s paracetamolom, aspirin in druga nesteroidna protivnetna zdravila pa se lahko uporabijo le, če je izključeno, da ne gre za dengo, in sicer zaradi tveganja za krvavitev.[20]
Med izbruhom v Francoski Polineziji so zabeležili 73 primerov Guillain–Barréjevega sindroma in drugih nevroloških motenj, ki bi lahko bili zaplet vročice zika.[15]
Podatki kažejo, da je pri novorojenčkih, katerih matere so se okužile z virusom zika v prvem trimesečju nosečnosti, povečano tveganje za mikrocefalijo. Domneva, da lahko okužba preko posteljice pri plodu povzroči mikrocefalijo ali možganske poškodbe, je obstajala že od decembra 2015.[21][5] Povezavo med okužbo z virusom zika in razvojem mikrocefalije pa so prvi dokazali slovenski znanstveniki. Izide raziskave je februarja 2016 objavila ugledna znanstvena revija New England Journal of Medicine.[22][23]
Virus zika je virus iz rodu flavivirusov, ki se prenaša preko vboda komarjev iz rodu Aedes. Slednji prenašajo tudi druge nalezljive bolezni, kot sta denga in čikungunja. Pri ljudeh povzroča blago okužbo, imenovano tudi vročica zika, ki je bila od 50-ih let prejšnjega stoletja značilna le za ozek ekvatorialni pas od Afrike do Azije. Leta 2014 se je bolezen razširila proti vzhodu, na območje Tihega ocena do Francoske Polinezije in dalje do Velikonočnega otoka, leta 2015 pa v Južno in Srednjo Ameriko ter Karibsko otočje, kjer povzroča še vedno trajajoč izbruh, ki so ga že uvrstili med pandemije. Bolezen poteka kot blaga oblika vročice denge, pri kateri se priporoča počitek, zanjo pa ne obstajajo specifična zdravila ali cepiva.
Vročica zika je sorodna z rumeno mrzlico in vročico zahodnega Nila, ki ju pa povzročata druga vrsta flavivirusov, vendar se prenašata prav tako s komarji. Okužbo nosečnic povezujejo z možnostjo povzročitve mikrocefalije pri novorojenčkih. Posledično je januarja 2016 ameriški Center za nadzor bolezni (CDC) izdal opozorila za potovanje v prizadete države s smernicami za preventivne ukrepe in priporočilom za opustitev potovanja ter posebna priporočila za nosečnice. Vlade več držav s tega območja so svetovale ženskam, naj odložijo nosečnost, če jo načrtujejo.
Zikavirus (ZIKV) är ett virus i familjen Flavivirus. Viruset överförs av Aedes-myggor samt sexuellt och kan hos människor orsaka en vanligen mild sjukdom som kallas zikafeber och som sedan 1950-talet tidvis har förekommit inom ett smalt bälte längs ekvatorn från Afrika till Asien. I november 2015 föreslogs en koppling mellan infektioner hos gravida och fosterskador. Den 1 februari 2016 klassade världshälsoorganisationen (WHO) smittspridningen av zikaviruset som ett internationellt nödläge.
Viruset isolerades första gången i april 1947 från en rhesusapa som forskare hade placerat i en bur i Zikaskogen i Uganda.[1] Det första dokumenterade utbrottet bland människor skedde år 2007 i Mikronesien.[2] Under 2014 spred sig viruset österut över Stilla havet till Franska Polynesien och vidare till Påskön, för att senare under 2015 fortsätta till Sydamerika, Centralamerika och Karibien. Utbrottet klassades som en pandemi.[3] I januari 2016 publicerades rapporter om eventuella kopplingar mellan zikavirusinfektion och allvarliga komplikationer som kan drabba foster. Viruset tros kunna orsaka mikrocefali hos nyfödda barn till mödrar som smittats under graviditeten, men sambandet och eventuell risk är inte helt klarlagd och utredning pågick fortfarande i mitten av januari.[4][5] Den 15 januari utfärdade USA:s nationella folkhälsomyndighet Centers for Disease Control and Prevention (CDC) reserekommendationer gällande de berörda länderna som innebär att gravida kvinnor bör överväga att skjuta upp resan.[6] Liknande reserekommendationer har utfärdats av myndigheter i många andra länder.
Den 1 februari klassade världshälsoorganisationen (WHO) smittspridningen av zikaviruset som ett internationellt nödläge. WHO befarar att upp till fyra miljoner människor kan ha smittats vid årets slut.[7] I den värst drabbade regionen i Brasilien har ungefär 1 procent av de nyfödda barnen mikrocefali.[8]
Virusets naturliga reservoar är ännu ej fastställd, men man har påvisat serologiska fynd hos västafrikanska apor och gnagare. Zikaviruset överförs av dagaktiva myggor och har isolerats från ett antal arter i släktet Aedes, bland dessa finns Aedes aegypti, Aedes africanus, Aedes apicoargenteus, Aedes furcifer, Aedes hensilli, Aedes luteocephalus och Aedes vittatus.[9] Zikavirus kan överföras mellan människor genom sexuell kontakt.[10] Det kan också passera moderkakan hos gravida kvinnor och därmed påverka ett foster.
Eftersom viruset endast kan spridas i de områden där det finns myggarter som kan bära det, är förändringar av myggarternas utbredningsområden en viktig orsak till att regioner som tidigare var fria från zikasmitta har drabbats. Den viktigaste vektorn, A. aegypti, sprids till nya områden genom handel och resor.[11] A. aegypti finns nu på alla kontinenter inklusive Nordamerika och även några mindre delar av Europa.[12] En myggpopulation som är kapabel att bära viruset har påträffats i Washington, DC och genetiska bevis antyder att den överlevt åtminstone fyra vintrar i området. Forskare drar slutsatsen att myggorna anpassat sig för att kunna överleva i nordligt klimat.[13]
Under 2015 uppmärksammades att zika spridit sig i Karibien och Sydamerika. De länder och territorier som enligt Pan American Health Organisation (PAHO) har drabbats av "lokal spridning av zikavirus" är Barbados, Bolivia, Brasilien, Colombia, Dominikanska republiken, Ecuador, El Salvador, Franska Guyana, Guadeloupe, Guatemala, Guyana, Haiti, Honduras, Martinique, Mexiko, Panama, Paraguay, Puerto Rico, Saint Martin, Surinam och Venezuela.[14][15]
År 2015 detekterades zikavirusets RNA i fostervatten hos två foster med microencefali enligt ultraljudsmätning, vilket tyder på att det hade passerat moderkakan och kunde orsaka en mor-till-barn-infektion.[16]
Vanliga symptom på zikavirusinfektion inkluderar mild huvudvärk, utslag, feber, sjukdomskänsla, ögoninflammation och ledvärk. Det första väldokumenterade sjukdomsfallet beskrevs 1964. Det började med lätt huvudvärk och därefter utslag, feber och ryggsmärtor. Inom två dagar började utslagen blekna. Inom tre dagar var febern borta och bara utslagen fanns kvar. Hittills har zikafeber varit en relativt mild sjukdom. Endast en av fem personer utvecklar symptom, medan de övriga är asymtomatiska.[9]
Sjukdomen kan för närvarande inte behandlas eller förebyggas med läkemedel eller vaccin. Symtomen kan behandlas med vila, vätska, och paracetamol, medan acetylsalicylsyra och andra icke-steroida antiinflammatoriska läkemedel endast ska användas när dengue har uteslutits för att minska risken för blödning.[17]
Under zikavirusutbrottet i Brasilien 2015 upptäcktes ett troligt samband mellan zikavirusinfektion och mikrocefali hos nyfödda barn. År 2015 upptäcktes 2 782 fall av mikrocefali jämfört med 147 under 2014 och 167 under 2013.[18]
I november 2015 isolerades zikavirus från en nyfödd baby med mikrocefali och andra missbildningar i den nordöstra delstaten Ceará i Brasilien. Medicintidskriften The Lancet rapporterade i januari 2016 att det brasilianska hälsoministeriet hade bekräftat 134 fall av mikrocefali som "tros vara associerade med zikavirusinfektion" och att det finns ytterligare 2 165 fall i 549 län i 20 delstater som är under utredning.[19]
I januari 2016 föddes en baby i Oahu, Hawaii, med mikrocefali vilket var det första fallet i USA där hjärnskador sätts i samband med viruset. Barnet och modern testades positivt för en tidigare zikavirusinfektion. Modern, som förmodligen smittats under en resa i Brasilien i maj 2015 under de tidiga stadierna av graviditeten, hade rapporterat milda symptom. Hon återhämtade sig innan hemresan till Hawaii. Hennes graviditet hade fortskridit normalt, och barnets tillstånd blev inte känt förrän vid födseln.[20]
En hög förekomst av den autoimmuna sjukdomen Guillain-Barrés syndrom (GBS) konstaterades i Franska Polynesien och har också påträffats i Brasilien.[21] Det finns dock inga laboratoriebekräftelser på zikavirusinfektion hos patienter med GBS.[22]
Ögonsjukdomar hos nyfödda har också varit knutna till zikavirusinfektion.[23] I en studie i Pernambuco i Brasilien hade cirka 40 procent av barn med zikarelaterad mikrocefali även ärrbildning i näthinnan med fläckar eller pigmentförändring.[22]
Flera länder, däribland Colombia, Ecuador, El Salvador och Jamaica, rådde kvinnor att undvika graviditet tills mer blir känt om riskerna.[24][25] Planer tillkännagavs av myndigheterna i Rio de Janeiro i Brasilien att försöka förhindra spridning av viruset under olympiaden i Rio sommaren 2016.
WHO:s rekommendationer för zikavirusskydd omfattar huvudsakligen användande av myggmedel; kläder (helst ljusa) som täcker en så stor del av kroppen som möjligt; barriärer som stängda dörrar och fönster, och användning av myggnät. Det är också viktigt att förhindra att myggor förökar sig i vattensamlingar nära hemmet genom att ta bort till exempel hinkar, blomkrukor eller däck, där myggor kan samlas och föröka sig.
I Brasilien har myndigheterna godkänt utsläpp av genetiskt modifierade myggor av arten Aedes aegypti. Ett brittiskt bioteknikföretag har tidigare publicerat ett testresultat för så kallade "självbegränsande" myggor för att bekämpa denguefeber, chikungunya och zikavirus. De drog slutsatsen att myggpopulationerna har minskat med över 90 % i testområdet.[26][27][28] De genetiskt modifierade hanmyggorna parar sig med honor i naturen och sprider en "självbegränsande gen" som får den resulterande avkomman att dö innan vuxen ålder och därmed minskar myggornas antal. [26][29]
Pesticider används också för att bekämpa mygglarver, bland annat pyriproxifen.[30]
Den svenska Folkhälsomyndigheten har informerat landets mödravårdscentraler, men reserekommendationerna för gravida i Sverige har inte uppdaterats (gällde 19 januari 2016).[5][31] UD avrådde inte heller från resor till de drabbade länderna (gällde 1 februari 2016).[32]
Zikavirusinfektion sprids för närvarande snabbt framförallt i Syd- och Centralamerika men också i Mexiko och Karibien och i olika ögrupper i Stilla havet och Atlanten. (14 oktober 2016)[33]
En forskare vid Statens Veterinärmedicinska Anstalt (SVA) säger att man "inte helt kan utesluta" att myggarten Aedes geniculatus, den silvertecknade trädhålsmyggan, skulle kunna sprida zikavirus. Myggan finns i Sverige och har i laboratorietester visat sig kunna sprida närbesläktade virus som chikungunya och gula febern, men ännu inte testats för zikavirus.[34] SVA samordnar ett projekt för att tillsammans med andra myndigheter få mer kunskap om insektsburen smitta i Sverige.[35]
Zikavirus (ZIKV) är ett virus i familjen Flavivirus. Viruset överförs av Aedes-myggor samt sexuellt och kan hos människor orsaka en vanligen mild sjukdom som kallas zikafeber och som sedan 1950-talet tidvis har förekommit inom ett smalt bälte längs ekvatorn från Afrika till Asien. I november 2015 föreslogs en koppling mellan infektioner hos gravida och fosterskador. Den 1 februari 2016 klassade världshälsoorganisationen (WHO) smittspridningen av zikaviruset som ett internationellt nödläge.
Zika virüsü (ZIKV), Flaviviridae virüs familyasının ve Flavivirus cinsinin bir üyesi. İnsanlara sivrisineklerden ve cinsel yoldan geçer ve Zika ateşi veya Zika hastalığı olarak bilinen hastalığa neden olur. Daha önce maymunlarda görülen virüs, ilk kez Nijerya'da bir insanda tespit edildi. Gebe kadınlara bulaştığında bebeklerde anomaliler görülmesine yol açar. Zika ile doğan bebeklerin kafaları normalden 31.5-32 santimetre daha küçük olur ve beyin fonksiyonlarında bozukluklar olur.
Zika virüsü Afrika, Amerika, Asya ve Pasifik’te yayılmış ve 2015'te Orta ve Güney Amerika'da yaşanan salgın, pandemik hâle gelmiştir.[1] Dünya Sağlık Örgütü, 2016'da 33 ülkeye yayıldığı saptanan[2] virüse karşı acil durum ilan etti. Bu virüse karşı bir aşı geliştirilebilmesi için en az 10 yıla ihtiyaç duyulduğu açıklandı.[3][4] Ayrıca doktorlar tarafından zika virüsünün cinsel yolla da bulaştığı duyuruldu.[5] Yetkililer tarafından, virüsle mücadelenin tek yolunun, sivrisineklerin ürediği durgun suları ilaçlamak ve kurutmaktan geçtiği vurgusu yapıldı.
Zika virüsü ilk olarak Hint şebeği maymunlarının yaşadığı Uganda'nın Zika Ormanları'nda görülmüştür. Maymunlardan sonra bu hastalık sivrisineklerde görülmüştür. Bu yüzden virüse "Zika" adı verilmiştir. Dünya Sağlık Örgütü'nün açıklamasına göre hastalık Şili hariç tüm Güney Amerika ülkelerine yayılmıştır. Latin Amerika ve Karayipler'de birçok ülkede de etkili olan virüs, örneğin Kolombiya'da 13 bin 500 kişide görülmüştür. Stockholm'daki Avrupa Hastalık Önleme ve Kontrol Merkezi'nden bir bilim insanı, Almanya ve İngiltere'de de Zika virüsü vakalarına rastlandığını söylemiştir. Türkiye Sağlık Bakanlığı da, 25 Ocak 2016'da yaptığı basın açıklamasında, Dünya Sağlık Örgütü verilerine göre Güneydoğu Asya, Pasifik Adaları, Orta ve Güney Amerika’da hastalığın yayıldığını bildirmiştir. Bu bağlamda Bakanlık, özellikle gebe kadınlara bu bölgelere seyahat etmemesi çağrısında bulunmuştur.[6]
ABD Hastalık Kontrol ve Korunma Merkezleri (CDC), Zika virüsüne ilişkin açıklamasında virüsün bulaştığı kişilerde semptomların yaklaşık bir hafta içinde ortaya çıktığını ve kanda birkaç gün duran virüsün bazı kişilerde daha da uzun kaldığını ifade etti.
Başlıca belirtileri:
Zika virüsü (ZIKV), Flaviviridae virüs familyasının ve Flavivirus cinsinin bir üyesi. İnsanlara sivrisineklerden ve cinsel yoldan geçer ve Zika ateşi veya Zika hastalığı olarak bilinen hastalığa neden olur. Daha önce maymunlarda görülen virüs, ilk kez Nijerya'da bir insanda tespit edildi. Gebe kadınlara bulaştığında bebeklerde anomaliler görülmesine yol açar. Zika ile doğan bebeklerin kafaları normalden 31.5-32 santimetre daha küçük olur ve beyin fonksiyonlarında bozukluklar olur.
Zika virüsü Afrika, Amerika, Asya ve Pasifik’te yayılmış ve 2015'te Orta ve Güney Amerika'da yaşanan salgın, pandemik hâle gelmiştir. Dünya Sağlık Örgütü, 2016'da 33 ülkeye yayıldığı saptanan virüse karşı acil durum ilan etti. Bu virüse karşı bir aşı geliştirilebilmesi için en az 10 yıla ihtiyaç duyulduğu açıklandı. Ayrıca doktorlar tarafından zika virüsünün cinsel yolla da bulaştığı duyuruldu. Yetkililer tarafından, virüsle mücadelenin tek yolunun, sivrisineklerin ürediği durgun suları ilaçlamak ve kurutmaktan geçtiği vurgusu yapıldı.
Zika virüsü ilk olarak Hint şebeği maymunlarının yaşadığı Uganda'nın Zika Ormanları'nda görülmüştür. Maymunlardan sonra bu hastalık sivrisineklerde görülmüştür. Bu yüzden virüse "Zika" adı verilmiştir. Dünya Sağlık Örgütü'nün açıklamasına göre hastalık Şili hariç tüm Güney Amerika ülkelerine yayılmıştır. Latin Amerika ve Karayipler'de birçok ülkede de etkili olan virüs, örneğin Kolombiya'da 13 bin 500 kişide görülmüştür. Stockholm'daki Avrupa Hastalık Önleme ve Kontrol Merkezi'nden bir bilim insanı, Almanya ve İngiltere'de de Zika virüsü vakalarına rastlandığını söylemiştir. Türkiye Sağlık Bakanlığı da, 25 Ocak 2016'da yaptığı basın açıklamasında, Dünya Sağlık Örgütü verilerine göre Güneydoğu Asya, Pasifik Adaları, Orta ve Güney Amerika’da hastalığın yayıldığını bildirmiştir. Bu bağlamda Bakanlık, özellikle gebe kadınlara bu bölgelere seyahat etmemesi çağrısında bulunmuştur.
Детальніші відомості з цієї теми Ви можете знайти в статті Пандемія хвороби, яку спричинює вірус Зіка.
У 2007 році вірус Зіка раптово поширився на схід через Тихий океан до Океанії — Французької Полінезії та острову Пасхи. Упродовж декількох років вірус вирував у Тихоокеанському регіоні. 2015 року досяг Південної та Центральної Америки, карибських країн і на сьогодні ставлять питання про можливість пандемії хвороби, яку спричинює вірус Зіка[2], хоча фахівці ВООЗ про це ще остаточно не вирішили. Захворювання нагадує легку форму гарячки денге[3], перебігає без необхідності серйозного лікування, і, на сьогодні, не може бути попереджено ані противірусними препаратами, ані специфічною вакциною[4]. Хвороба, яку спричинює вірус Зіка, споріднена з жовтою гарячкою та гарячкою Західного Нілу, тому що їх спричинюють флавівіруси, що передаються комарами[3].
Під час епідемії у Французькій Полінезії було виявлено 73 випадки синдрому Гієна — Барре та інших неврологічних ускладнень серед 270 000 осіб, що може бути пов'язане з вірусом Зіка[2]. Згідно сповіщення ВООЗ, у Сальвадорі спостерігають незвичне збільшення кількості захворілих на синдром Гієна — Барре. Середньорічне число захворілих на цей синдром у цій країні складає 169. Але від 1 грудня 2015 року по 6 січня 2016 року зареєстровано вже 46 випадків цього ураження нервової системи, зокрема 2 смерті. Проводять комплекс різноманітних досліджень, в тому числі направлених на виявлення можливого зв'язку між синдромом Гієна — Барре й вірусом Зіка у цій країні[5].
Європейський центр із запобігання і контролю захворювань у грудні 2015 року випустив публікацію на тему можливого зв'язку вірусу Зіка з вродженою мікроцефалією і синдромом Гієна — Барре[6]. Зв'язок цієї хвороби з мікроцефалією у новонароджених, які народилися від інфікованих матерів, на даний час вважають найімовірнішим[7], про це свідчать результати розтину окремих померлих дітей з явищами мікроцефалії[8][9], проте фахівці з боротьби з поширенням інфекційних хвороб застерігають поки що від безапеляційних висновків про абсолютний зв'язок та наголошують на необхідності проводити подальші всеосяжні ґрунтовні комплексні дослідження. Друге засідання Комітету Міжнародних медико-санітарних правил 8 березня 2016 року обговорило питання можливого зв'язку між хворобою, яку спричинює вірус Зіка, та неврологічним розладом — синдромом Гієна — Барре і вродженою аномалією — мікроцефалією. Було відмічено, що все більш імовірним ввижається між ними прямий зв'язок, але остаточний висновок робити ще зарано, тому Комітет і ВООЗ закликають до всеосяжного продовження наукових досліджень та їхній інтенсифікації задля швидшого вирішення цього питання.[10]
15 січня 2016 року відділ Центрів з контролю і профілактики захворювань (CDC) оприлюднив рекомендації для мандрівників по країнам, де зафіксовано випадки хвороби, яку спричинює вірус Зіка, включаючи рекомендації щодо прийняття особливих заходів безпеки і перенесення поїздки, якщо в ній немає термінової необхідності[11].
Детальніші відомості з цієї теми Ви можете знайти в статті Хвороба, яку спричинює вірус Зіка.
На сайті Дитячого фонду (ЮНІСЕФ) Організації Об'єднаних Націй (ООН) 2 лютого 2016 року опубліковано інформацію, згідно якої можливість розвитку мікроцефалії у плода вагітної жінки, яку було інфіковано вірусом Зіка, поки не підтверджено, але і не спростовано. "Не дивлячись на те, що до сіх пір немає переконливих доказів причинно-наслідкового зв'язку між мікроцефалією та вірусом Зіка, досить занепокоєння, щоб гарантувати негайну дію, " — сказав доктор Хізер Паповіц, старший радник ЮНІСЕФ з питань охорони здоров'я надзвичайних ситуацій. «Ми повинні діяти швидко, аби забезпечити доступ до інформації жінкам і вагітним, необхідної, щоб захистити себе і своїх дітей, і ми повинні взаємодіяти з громадами з питань того, як зупинити комарів, передачу цього вірусу.» Там же наведено статистику виявлення випадків мікроцефалії у новонароджених в Бразилії: за даними фонду за період з 22 жовтня 2015 року по 26 січня 2016 виявлено 4 180 випадків, у той час протягом 2014 року — лише 147 випадків[12].
Вперше вірус було виділено 1947 року у макак-резусів в лісі Зіка, Уганда[13]. У 1952 році вірус вперше було виділено від людини теж в Уганді[14][15]. З того часу по 1981 рік були отримані численні свідоцтва того, що вірус має сталу циркуляцію серед людей в Африці і може спричиняти захворювання, докази чого було отримано і в інших африканських країнах, таких як Танзанія, Єгипет, ЦАР, Сьєрра-Леоне, Габон, а також в деяких областях Азії, включаючи Індію, Малайзію, Філіппіни, Таїланд, В'єтнам та Індонезію[13].
Подібно іншим флавівірусам, вірус Зіка має оболонку. Нуклеокапсид приблизно 25-30 нм в діаметрі з несегментованим, одноланковим, позитивно-спрямованим РНК-геномом. Він оточений мембраною з двошарової ліпідної оболонки, яка містить білки оболонки. Віріон приблизно сягає 40 нм в діаметрі з поверхневими виступами, які становлять приблизно 5-10 нм. Поверхневі білки розташовані в ікосаедричноподібній симетрії. Має дві некодуючі області, відомі як 5 'NCR і 3' NCR. Відкрита рамка зчитування вірусу Зіка має структуру 5'-С-PRM-Е-НС1-NS2A-NS2B-NS3-NS4A-NS4B-N S5-3'. Кодує поліпротеїни, які згодом розщеплюються в капсид (С), мембранний попередник (PRM), білок (Е) і неструктурні білки (NS)[16]. Білок Е складає більшість поверхні віріона і бере участь у зв'язуванні з клітинами хазяїна і злитті їх мембран[17]. Білки НС1, NS3, NS5 є високомолекулярними білками, а білки NS2A, NS2B, NS4A і NS4B менші за молекулярністю, гідрофобні білки. Розташований в 3 'NCR фрагмент з 428-ми нуклеотидів можливо грає роль в трансляції, пакуванні РНК, циклізації, стабілізації геному і розпізнаванні. 5' NCR проводить трансляцію за допомогою метилованого нуклеотиду або геном-пов'язаного білка.[18]
Разом з вірусом Спондвені утворює кладу Спондвені (англ. Spondweni) в роді Flavivirus[19][17].
Адгезійні фактори (наприклад, адгезін рецептора тирозинкінази) сприяють інфекції.[18]
Філогенетичний аналіз показує, що вірус Зіка можна бути класифікувати на різні африканські та азійські родоводи; які вийшли зі Східної Африки в кінці 1800-х або на початку 1900-х років. Азійські родоводи виникли під час міграції вірусу з Африки в Південно-Східну Азію, де його вперше виявили в Малайзії. Звідти вірус Зіка поширився на острови Тихого океану, а потім до Нової Каледонії, острови Кука, острів Пасхи, а також до Північної і Південної Америки. Вивчення молекулярної еволюції вірусу Зіка на основі вірусних штамів, зібраних з 4-х країн в Західній Африці протягом 1947—2007 років, визначило кілька ділянок всередині генома вірусу, які перебували під сильним негативним тиском відбору. Ці дані свідчать про часті згубні зміни функціонально важливих генів і можливість їх рекомбінації, яка зустрічається дуже рідко серед інших флавівірусів. Наслідки цього спостереження вимагають подальшої оцінки щодо особливостей поширення вірусу в світі, існування можливого зоонозного резервуару, епідеміологічного потенціалу.[18]
Отримані свідчення, що проникнення вірус після укусу відбувається через фібробластів людської шкіри, кератиноцитів і незрілих дендритних клітин[18]. Вважають також, що вірус спочатку інфікує дендритні клітини поблизу від місця потрапляння, потім поширюється у лімфатичні вузли і, врешті решт, поступає у кровотік[19]. Флавівіруси зазвичай відтворюються у цитоплазмі, але антигени вірусу Зіка були знайдені в ядрах інфікованих клітин[20]. Така особливість реплікації вірусу Зіка, яка є відмінною від інших флавівірусів, потребує подальшого вивчення для розуміння особливостей поширення вірусу в світі та його патогенезу.[18]
Вірус Зіка передають активні протягом денного періоду комарі роду Aedes — Aedes aegypti і, рідше, так звані деревні комарі Aedes africanus, Aedes apicoargenteus, Aedes furcifer, Aedes hensilli, Aedes luteocephalus та Aedes vitattus. Тривалість набуття патогенності в організмі комарів становить приблизно 10 днів[13]. Хребетні джерела вірусу — мавпи і люди, хоча питання про усі можливі джерела та резервуари інфекції достеменно не вивчено. До початку поширення, що почалося 2007 року, вірус Зіка «рідко спричиняв помітні „надлишкові“ захворювання у людини, навіть у високоендемічних районах»[2].
У 2009 році Браян Фой, біолог з лабораторії з вивчення антропонозних інфекційних хвороб Державного університету Колорадо заразив вірусом Зіка свою дружину статевим шляхом. Він відвідував Сенегал і вивчав комарів, деякі з них його кусали. Через кілька днів після повернення в США він відчув, що захворів, було визначено, що це хвороба, яку спричинює вірус Зіка, але це сталося вже після незахищеного статевого контакту з дружиною. Згодом у неї з'явилися ознаки хвороби з нетривалою гарячкою, надмірною чутливістю до світла. Фой — перша відома людина, яка передала поширюваний комахами вірус іншій людині через статевий контакт[21][22], довівши, таким чином, можливість не тільки натуральної трансмісивної передачі, але й контактної статевої передачі.
У 2015 році РНК вірусу Зіка було виявлено в навколоплідних водах двох людських ембріонів, це показало, що вірус проникає через плаценту і може спричинити інфекцію у плода[23]. 20 січня 2016 року вчені у штаті Парана (Бразилія) виявили генетичний матеріал вірусу Зіка у плаценті жінки, якій зробили аборт з приводу передбачуваної мікроцефалії її плода. Ця знахідка підтвердила той факт, що вірус може проникати через плаценту[24].
Ознаки хвороби включають легкий головний біль, плямистий висип, нетривалу гарячку без виразної інтоксикації, нездужання, кон'юнктивіт і біль в суглобах. Тільки в однієї людини з п'яти проявлялися ознаки захворювання, відсутня летальність, проте справжній патогенний потенціал вірусу досі не відомий[13].
На січень 2016 року не існує вакцини або противірусних засобів для запобігання захворювання. Гарячку можна полегшити, використовуючи парацетамол, тоді як аспірин та інші нестероїдні протизапальні препарати можна застосовувати тільки після виключення гарячки денге через можливий ризик виникнення кровотеч[25].
Дослідники з університету Пурду були першими, кому в 2016 році вдалося сфотографувати структуру вірусу Зика. Використовуючи кріоелектронну мікроскопію, вони отримали зображення вірусу з роздільною здатністю в 3.8 ангстрема. 1 ангстрем -10 ^ -10 метра, ця одиниця традиційно використовується для вираження розмірів вірусів, молекул та інших мікроскопічних об'єктів. А в 2018 році, поліпшивши використовувані cryo-EM-технології, дослідники зробили знімок з роздільною здатністю в 3.1 ангстрема, що дозволило більш точно визначити атомарну структуру вірусу і виявити свого роду «кишені» на його поверхні, які можна використовувати при розробці і виробництві вакцини[26].
|displayauthors= (довідка) Virus Zika (ZIKV) là một virus RNA (arbovirus) thuộc chi Flavivirus, họ Flaviviridae, lây truyền chủ yếu qua vết cắn của muỗi Aedes bị nhiễm. Tên của virus lấy tên từ khu rừng Zika, gần hồ Victoria ở Uganda, nơi đầu tiên phân lập vào năm 1947. Virus Zika có liên quan đến bệnh sốt xuất huyết, sốt vàng da, viêm não Nhật Bản, và West Nile virus. Virus Zika đã có mặt ở khu vực nhiệt đới của châu Á và châu Phi từ năm 1950. Đây là virus mới nổi, chịu trách nhiệm cho một số dịch bệnh: năm 2007 trên đảo Yap, liên bang Micronesia, sau đó lan về phía đông qua Thái Bình Dương đến Polynesia thuộc Pháp, tiếp đến đảo Phục Sinh; đến 2015 qua Trung Mỹ, vùng Caribbean, và Nam Mỹ, nơi sốt Zika đã đạt đến cấp đại dịch.[1] Các trường hợp đầu tiên được phát hiện ở Brazil; quốc gia này đang bị ảnh hưởng nặng nhất với hơn 1.500.000 trường hợp (0,72% dân số Brazil).
Virus Zika xác định qua phát hiện bộ gen bằng PCR. Đến nay bệnh do Zika gây nên chưa có thuốc điều trị đặc hiệu và chưa có vắc xin phòng bệnh vì vậy diệt vec tơ truyền bệnh với sự tham gia tích cực của cộng đồng là biện pháp hiệu quả nhất trong phòng chống bệnh.[2]
Đợt nhiễm virua zika được gọi là sốt Zika, thường không có hoặc chỉ có triệu chứng nhẹ, tương tự như dạng rất nhẹ của bệnh sốt xuất huyết. Zika có thể lây từ bà mẹ qua thai nhi. Điều này có thể dẫn đến tật đầu nhỏ ở trẻ sơ sinh và các biến chứng não nghiêm trọng khác. Người lớn có thể nhiễm Zika, hiếm khi dẫn đến hội chứng Guillain Barre - hội chứng tổn thương thần kinh có thể gây liệt.[3][4][5]
Vào tháng 1 năm 2016, Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa kỳ (CDC) đã ban hành hướng dẫn du lịch các nước bị ảnh hưởng, bao gồm cả việc sử dụng các biện pháp phòng ngừa tăng cường, và hướng dẫn cho phụ nữ mang thai bao gồm xem xét hoãn các chuyến đi du lịch. Chính phủ một số nước và các cơ quan sức khỏe trên thế giới cũng đưa ra cảnh báo du lịch tương tự, trong khi Colombia, Cộng hòa Dominica, Ecuador, El Salvador, và Jamaica khuyên phụ nữ trì hoãn việc mang thai cho đến khi hơn được biết rõ về những nguy cơ.
Vào ngày 1 tháng 2 năm 2016, Tổ chức Y tế Thế giới (WHO) ban bố tình trạng Khẩn cấp Y tế Công cộng Quốc tế về virus Zika, sau khi tham khảo ý kiến từ các chuyên gia hàng đầu về dịch tễ học, y tế công cộng và bệnh truyền nhiễm từ khắp thế giới tại một cuộc họp của Ủy ban khẩn cấp y tế quốc tế thuộc WHO. Virus Zika đã lây hơn 70 quốc gia và vùng lãnh thổ, trong đó có 57 quốc gia và vùng lãnh thổ tiếp tục có sự lây truyền của virus Zika do muỗi truyền, khiến nguy cơ xảy ra dịch là rất lớn. Tổ chức này cảnh báo dịch Zika có thể diễn biến tồi tệ hơn trước khi được kiểm soát và khuyến cáo người dân thực hiện các biện pháp chống muỗi và tránh bị muỗi đốt.[6]
Virus Zika thuộc Flaviviridae và chi Flavivirus, và do đó có liên quan đến bệnh sốt xuất huyết, sốt vàng da, viêm não Nhật Bản và West Nile virus.
Giống như flaviviruses khác, cấu trúc gen Zika gồm RNA sợi đơn dài 10.794bp với hai vùng không mã hóa là 5 'NCR và 3' NCR (non-coding regions). Với khung đọc mở: 5'-C-prM-E-NS1-NS2A-NS2B-NS3-NS4A-NS4B-NS5-3', mã hóa cho một polyprotein và sau đó cắt thành capsid (C), màng tiền thân (prM), vỏ (E), và các protein không cấu trúc (NS). Các protein E tạo nên bề mặt hạt vi rút để tham gia vào quá trình sao chép bằng cách gắn lên trên thụ thể của các tế bào cảm thụ NS1, NS3, và NS5 là những protein kích thước lớn và có tính bảo tồn cao trong khi protein NS2A, NS2B, NS4A và NS4B là những protein nhỏ hơn và kỵ nước. Vùng 3 'NCR có 428 nucleotide có thể đóng vai trò dịch mã, đóng gói RNA, tạo vòng, ổn định hệ gen, và định danh. 3 'NCR tạo thành một cấu trúc vòng lặp và 5' NCR cho phép dịch mã thông qua một mũ nucleotide methyl hóa hoặc một protein gắn kết gen.[7].
Có hai dòng Zika: dòng châu Phi, và dòng châu Á.[8] Nghiên cứu loài cho thấy virus lây lan ở châu Mỹ có liên quan chặt chẽ nhất đến dòng châu Á, trong đó có đợt bùng nỗ dịch tại Pháp.[8][9] Trình tự bộ gen hoàn chỉnh của Zika đã được xuất bản.[10] Ở Tây bán cầu Zika được tìm thấy là 89% giống với kiểu gen Phi, nhưng liên quan di truyền chặt chẽ nhất là ở Polynesia, Pháp năm 2013-2014.[11]
Virus lây truyền cho người qua vec tơ trung gian là muỗi cái Aedes aegypti, dân gian gọi là muỗi vằn. Muỗi này rất thích đốt người, hút máu ban ngày cao điểm vào sáng sớm và chiều tối. Ngoài ra cũng có một số dòng muỗi cùng chi với Aedes aegypti Aedes như A. africanus , A. apicoargenteus, A. furcifer, A. hensilli, A. luteocephalus và A. vitattus cũng có thể lan truyền virus. Sau khi hút máu người hay động vật có chứa virus Zika, thời gian cần thiết để cho virus phát triển trong muỗi là khoảng 10 ngày, sau đó muỗi có khả năng truyền virus cho người hoặc động vật khác khi hút máu và có thể truyền bệnh suốt đời. Một cá thể muỗi nhiễm virus Zika có thể truyền virus cho các thế hệ muỗi con cháu.[12] Ổ chứa tự nhiên của virus Zika là các loài linh trưởng và một số loài gặm nhấm.[13]
Sự phân bố muỗiAedes aegypti được đánh giá là rộng lớn nhất từng được ghi nhận, hầu như loài muỗi này đã có mặt ở hầu các châu lục, bao gồm Bắc Mỹ và các ngoại vi của châu Âu.[14]
Các hoạt động hương mại và du lịch làm tăng sự lây lan virus này.[15]
Ngoài lây truyền qua muỗi đốt là con đường chủ yếu, còn nhiều đường lây truyền khác có thể làm truyền virus Zika như lây truyền từ mẹ sang thai nhi, lây truyền qua quan hệ tình dục. ARN của virus Zika cũng đã được phát hiện trong máu, nước tiểu, tinh dịch, dịch não tủy, nước ối và sữa của các bệnh nhân nhiễm virus Zika.
Zika có thể được truyền từ một người đàn ông cho các đối tác tình dục của họ.[16] Tính đến tháng 4 năm 2016 phương thức lây truyền này đã ghi nhận ở sáu quốc gia - Argentina, Chile, Pháp, Ý, New Zealand và Hoa Kỳ - trong đợt dịch năm 2015.
Năm 2009, Brian Foy, một nhà sinh học tại Đại học bang Colorado đã truyền vi rút Zika sang vợ của ông qua đường tình dục. Ông trước đó đã đến thăm Senegal để nghiên cứu về muỗi, và đã bị muỗi cắn vài lần. Một vài ngày sau khi trở về Mỹ, ông cảm thấy bị bệnh, được xác định rằng đó là một căn bệnh gây ra bởi virus Zika, sau khi có quan hệ tình dục không an toàn với người vợ của mình. Sau đó, bà ta đã phát triển các triệu chứng của bệnh Zika như nhạy cảm quá mức với ánh sáng. Foy là người đầu tiên mà được biết tới đã truyền vi rút Zika từ muỗi qua đường tình dục sang một người khác.[17][18]
Một người đàn ông tại Texas (Mỹ) được phát hiện nhiễm virus Zika do quan hệ với bệnh nhân vừa trở về từ vùng dịch ở Venezuela. Thông tin được Trung tâm Kiểm soát và Phòng tránh Dịch bệnh Mỹ (CDC) xác nhận ngày 2/2. Đây là trường hợp lây nhiễm qua đường tình dục đầu tiên được xác định tại Mỹ.[19]
Tổ chức Y tế thế giới (WHO) ngày 3/2 đã bày tỏ sự quan ngại về báo cáo xác nhận ca virus Zika lây truyền qua đường tình dục tại Mỹ và kêu gọi tiến hành điều tra thêm đối với loại virus gây teo não ở trẻ này.[20]
Các nhà khoa học đưa ra cảnh báo rằng Zika có thể tồn tại trong tinh trùng của người đàn ông, tuy nhiên người ta vẫn chưa biết nó sẽ sống được bao lâu và khi nào nó sẽ bị lây nhiễm khi quan hệ tình dục. Trong khi chờ đợi, CDC khuyên những người đàn ông trở về từ các vùng có Zika hãy tạm ngưng quan hệ tình dục hoặc sử dụng bao cao su trong một thời gian (chưa xác định).
Virus Zika có thể lây từ mẹ sang thai nhi trong quá trình mang thai hoặc khi sinh.[21]
Nhiễm virus Zika gần hạn khả năng có thể được truyền đi trong cả thai kỳ và lúc sinh con, mặc dù đến nay cho điều vẫn chưa được chứng minh một cách khoa học. Phụ nữ mang thai nói chung, bao gồm cả những người có triệu chứng nhiễm virus Zika, có nghi ngờ nên đến các cơ sở y tế để giám sát chặt chẽ thai kỳ.
Virus Zika đã được phát hiện trong sữa mẹ nhưng hiện nay chưa có bằng chứng cho thấy virus lây truyền sang con qua sữa mẹ. WHO khuyến cáo bú mẹ hoàn toàn trong 6 tháng đầu đời.
Hầu hết phụ nữ trong khu vực bị ảnh hưởng Zika sẽ sinh ra những trẻ bình thường. Siêu âm đầu không đáng tin cậy dự đoán dị tật thai nhi. WHO khuyến cáo nên siêu âm lặp lại vào cuối tam cá nguyệt thứ ba thứ hai hoặc đầu (tốt nhất là giữa tuần 28 và 30) để xác định đầu nhỏ của thai nhi và/ hoặc các bất thường khác của não khi lúc này dễ phát hiện.
Bà mẹ có thể yêu cầu phá thai an toàn phù hợp với kỹ thuật, chính sách hướng dẫn cho hệ thống y tế và khía cạnh pháp lý.
Ngày 4/2, Brazil đã xác nhận 2 trường hợp nhiễm virus Zika qua đường máu.[22]
Ngày 5/2, các nhà khoa học tại một viện y tế công cộng của Brazil thông báo đã tìm thấy virus Zika trong nước bọt và nước tiểu của hai bệnh nhân được xác định là nhiễm loại virus nguy hiểm này. Đây là lần đầu tiên,virus gây teo não Zika được phát hiện trong chất dịch. Gia tăng mối lo ngại loại virus này có thể lây truyền qua nhiều con đường khác nhau. Tuy nhiên, theo các nhà khoa học, vẫn cần phải nghiên cứu thêm để xác định liệu virus Zika có truyền được qua các chất dịch hay không.[23]
Thời kỳ ủ bệnh (thời gian từ khi tiếp xúc với các triệu chứng) của bệnh virus Zika vẫn chưa rõ, nhưng có khả năng là vài ngày. Chẩn đoán phân biệt sốt zika bao gồm Sốt xuất huyết Dengue, Chikungunya, Parvovirus, Rubella, Enterovirus, Adenovirus, Alphaviruses, Sởi; nhiễm vi khuẩn và ký sinh trùng như Leptospirosis, Rickettsia, nhiễm liên cầu tan huyết nhóm A, Sốt rét. Với các dấu hiệu bệnh lý như khởi phát sốt nhẹ (37,8-38,5 °C), phản ứng viêm, phản ứng dị ứng có ban dát sẩn trên da, viêm kết mạc, viêm khớp (đặc biệt là các khớp nhỏ ở bàn tay và bàn chân) hay gout. Những triệu chứng này thường nhẹ và kéo dài từ 2 đến 7 ngày.
Sốt zika bắt đầu với một cơn đau đầu nhẹ và tiến triển thành phát ban dạng sẩn với sốt và đau lưng. Sau hai ngày, phát ban bắt đầu giảm. Đến ngày thứ ba, cơn sốt giảm xuống chỉ còn phát ban. Sốt Zika là một bệnh tương đối nhẹ, chỉ một trong 5 người có các triệu chứng điển hình không gây tử vong, nhưng tác nhân thực sự để gây bệnh của virus này thì chưa rõ.
Việc chẩn đoán cần dựa vào biểu hiện lâm sàng cũng như yếu tố dịch tễ gợi ý. Virus này có thể được phát hiện bởi test phản ứng nhanh Elisa, qua sự hiện diện của kháng thể immunoglobulin M(IgM) chống lại virus Zika trong huyết thanh. IgM có thể phát hiện từ 3 ngày sau triệu chứng khởi phát đầu tiên, tuy nhiên có thể sai sót khi xuất hiện phản ứng chéo với các virus khác trong nhóm flavivirus như Dengue. Các xét nghiệm chẩn đoán nhanh chóng tìm kháng thể chống lại virus dengue có thể xảy ra trường hợp dương tính giả trong một cơn sốt Zika, đặc biệt là nếu bệnh nhân đã bị nhiễm flavivirus trước đây có thể dẫn đến việc chẩn đoán sai. Trường hợp đầu tiên là ở Quần đảo Yap, ba bệnh nhân sốt Zika được thực hiện một chẩn đoán nhanh bệnh sốt xuất huyết tích cực. Các xét nghiệm trung hòa huyết thanh bằng cách giảm mảng bám có tính đặc hiệu cao hơn so với phương pháp ELISA, nhưng không loại trừ nguy cơ phản ứng chéo.
Việc chẩn đoán xác định dựa trên các phát hiện của virus bằng RT-PCR hoặc phân lập virus trong tế bào nuôi cấy. Các tìm kiếm có thể được thực hiện bằng PCR trên các mẫu máu thu được trong giai đoạn virus trong máu nhiễm trong vòng tối đa 10 ngày sau khi khởi phát triệu chứng, nhưng một nghiên cứu gần đây(tháng 1 năm 2016), dựa trên 1.067 mẫu được thực hiện với 855 bệnh nhân trong 6 tháng cho thấy RNA Zika được phát hiện tốt hơn bằng PCR trong nước bọt và trong máu (không phụ thuộc vào giai đoạn của bệnh), trong nghiên cứu này cho thấy nước bọt tăng tỷ lệ phát hiện tổng thể phát hiện virus Zika và rằng phương pháp này có lợi ích bổ sung cho lấy mẫu máu đang còn gặp khó khăn. Mẫu nước bọt cũng thường xuyên được sử dụng để chẩn đoán sốt Zika ở vụ dịch tại Polynesia Pháp.
Ngày 2/2, các nhà khoa học tại Đức cho biết đã phát triển thành công một phương pháp xét nghiệm nhanh virus Zika.Theo đó, phương pháp xét nghiệm nhanh ADN để phát hiện xem bệnh nhân có bị nhiễm virus Zika hay không đã được phát triển thành công. Sau khi lấy máu xét nghiệm, phương pháp này sẽ cho kết quả chính xác chỉ trong 2 - 3 giờ. [24]
Tổ chức Y tế Thế giới (WHO) công bố virus Zika là nguyên nhân của hai hội chứng rối loạn thần kinh. Đó là gây teo não ở trẻ sơ sinh và hội chứng làm tê liệt hệ thần kinh ở người lớn (thường gọi là Hội chứng tự miễn dịch Guillain-Barré).
Virus Zika gây ảnh hưởng đến trẻ sơ sinh, làm đầu trẻ không được phát triển bình thường, gọi là tật đầu nhỏ.
Tật đầu nhỏ được định nghĩa là sự thoái hóa hay dị dạng não ở trẻ sơ sinh với kích thước đầu nhỏ hơn bình thường và đôi khi dẫn đến tử vong.
Tổ chức Y tế Thế giới (WHO) cho biết có 20 quốc gia và vùng lãnh thổ trong khu vực châu Mỹ Latin bị ảnh hưởng bởi virus Zika, trong đó có Barbados, Bolivia, Guadeloupe, Guatemala, Puerto Rico và Panama, dự đoán khoảng ba đến bốn triệu người sẽ bị nhiễm virus Zika ở khu vực châu Mỹ nói chung trong năm 2016.[25]
Các dữ liệu cho thấy ở bào thai của người phụ nữ bị nhiễm virus trong ba tháng đầu của thai kỳ có nguy cơ cao tật đầu nhỏ[26].Chính vì điều này mà chính phủ nhiều nước như El Salvador, Colombia và Ecuador khuyên phụ nữ không nên mang thai và sinh con trong giai đoạn virus Zika đang hoành hành, thay vào đó chỉ nghĩ đến việc sinh con sau năm 2018[27].
Brazil là quốc gia bị ảnh hưởng nặng nề nhất bởi virus Zika, có gần 4.000 ca bị bệnh đầu nhỏ, với 49 ca tử vong. Chính quyền nước này khuyên phụ nữ không sinh con khi dịch Zika chưa được ngăn chặn.[28]
Ngày 15/2 một nhóm bác sĩ Argentina cho rằng nguyên nhân gây chứng teo não không phải virút Zika mà do hóa chất diệt ấu trùng muỗi có trong nguồn nước sinh hoạt tại Brazil. Loại hóa chất này có tên Pyriproxyfen này đã được sử dụng trong chương trình diệt muỗi quy mô lớn do chính phủ Brazil triển khai. [29] Tuy nhiên, sau đó vài ngày, các quan chức y tế Brazil và WHO bác bỏ nhận định trên, rằng không có bằng chứng thuốc diệt muỗi chứa Pyriproxygen gây ra đợt bùng phát dị tật đầu nhỏ và vẫn nghiêng về giả thuyết thủ phạm là virus Zika. [30]
Theo các chuyên gia của WHO, hội chứng Guillain-Barré là một bệnh lý hiếm gặp khi hệ thống miễn dịch của cơ thể tấn công một phần hệ thần kinh ngoại biên. Những triệu chứng đầu tiên của chứng rối loạn này bao gồm nhiều cấp độ của những cảm giác suy yếu hoặc tê buốt ở chân tay và phần trên cơ thể. Những triệu chứng này gia tăng cho đến khi các cơ không còn sử dụng được nữa và người bệnh gần như liệt hoàn toàn. Mặc dù có bệnh nhân hồi phục được song phần lớn vẫn tiếp tục cảm nhận mức độ suy yếu. Hiện tại trong giới y học đang áp dụng phương pháp tăng glôbulin miễn dịch liều cao để điều trị.
Ngoài các hội chứng trên, một số nhà nghiên cứu cũng đã báo cáo trường hợp các bệnh nhân nhiễm virus Zika có triệu chứng phát triển viêm não và viêm tủy. Khi các tế bào thần kinh bị tổn thương, có thể dẫn đến rối loạn thần kinh.
Hiện chưa có vắc-xin bảo vệ đặc hiệu. Điều trị chủ yếu là điều trị triệu chứng.
Người bệnh nên nghỉ ngơi, bù dịch bằng cách uống nhiều nước để chống mất nước. Dùng các thuốc hạ sốt,giảm đau như paracetamol, acetaminophen. Không dùng aspirin và các thuốc chống viêm không steroid khác (NSAID) như ibuprofen và naproxen cho đến khi loại trừ được sốt xuất huyết Dengue. Nếu đang dùng các loại thuốc cho những bệnh khác, nên hỏi ý kiến bác sĩ trước khi cho dùng thêm thuốc bổ sung. Nếu đang bị nhiễm virus Zika, cần ngăn ngừa muỗi đốt trong tuần đầu tiên của bệnh. Trong tuần đầu tiên virus Zika có thể được tìm thấy trong máu và truyền từ người bị nhiễm bệnh qua muỗi làm lây lan virus cho người khác.[31]
Theo dõi các biểu hiện yếu, liệt cơ sau khi bị bệnh để phát hiện, xử trí sớm hội chứng Gulain Barre nếu có. Theo dõi phụ nữ có thai và trẻ sơ sinh bị nhiễm virus Zika. Phụ nữ có thai nghi ngờ hoặc xác định bị nhiễm virus Zika cần được theo dõi siêu âm thai mỗi 3-4 tuần một lần để phát hiện sớm tình trạng đầu nhỏ hoặc vôi hóa não ở thai nhi. Phụ nữ có thai trên 15 tuần bị nhiễm virus Zika có thể chỉ định chọc ối làm xét nghiệm RT-PCR hoặc lấy máu dây rốn trong vòng 2 ngày sau cuộc đẻ để xét nghiệm huyết thanh nếu người mẹ đang trong thời gian bị bệnh, hoặc lấy máu dây rốn xét nghiệm huyết thanh có thể hồi cứu tình trạng nhiễm virus Zika bẩm sinh của thai nhi. Trẻ bị dị tật đầu nhỏ hoặc có tiền sử mẹ nhiễm virus Zika khi mang thai cần được theo dõi sự phát triển về tinh thần- vận động, đánh giá thị lực và điều trị các rối loạn như co giật, động kinh. [32]
Hiện chưa có thuốc để chống lại virus Zika. Việc điều trị chủ yếu dựa trên điều trị các triệu chứng. Thuốc paracetamol có thể được sử dụng để làm giảm cơn đau và sốt. Nên tránh việc sử dụng ibuprofen, aspirin, vì có khả năng gây ra hội chứng xuất huyết, phổ biến ở flaviviroses.[33] Nếu phát ban có triệu chứng ngứa có thể dùng diphenhydramine[34]
Các test chẩn đoán nhanh chỉ để phát hiện ra có sự hiện diện virus này hay không[35]. Trong trường hợp không có vắc xin, việc phòng chống lây nhiễm chủ yếu thông qua kiểm soát các vector truyền bệnh.[36].
Muỗi và nơi sinh sản của chúng là một yếu tố nguy cơ quan trọng đối với nhiễm virus Zika. Phòng ngừa và kiểm soát dựa trên việc giảm muỗi. Tại vùng có dịch cần triển khai các biện pháp diệt muỗi, lăng quăng, bọ gậy như: vệ sinh môi trường, loại bỏ các vật dụng đọng nước như các mảnh vỡ chai lọ, lốp xe, vỏ lon, vũng nước đọng... Đậy kín các chum, vại, bể chứa nước. Thả cá để diệt loăng quăng, diệt muỗi bằng bẫy, vợt. Mọi cá nhân trong vùng dịch nên áp dụng các biện pháp hạn chế muỗi đốt như: Mặc quần áo kín, sáng màu, dùng các thuốc xua đuổi côn trùng, nằm màn. Những nguyên tắc này cũng áp dụng đối với những người đã bị nhiễm bệnh nhằm tránh nguy cơ lây nhiễm cho người khác. Chất chống côn trùng nên chứa DEET (N, N-diethyl-3-methylbenzamide), IR3535 (3- [N-acetyl-N-butyl] axit -aminopropionic ethyl ester) hoặc icaridin (1-piperidinecarboxylic acid, 2- (2-hydroxyethyl) -1-methylpropylester). Hướng dẫn trên nhãn sản phẩm phải được thực hiện nghiêm túc. Đặc biệt chú ý và giúp đỡ nên được trao cho những người có thể không có khả năng tự bảo vệ mình đầy đủ, chẳng hạn như trẻ em, người ốm hoặc người già. Trong thời gian bùng phát, cơ quan y tế có thể tư vấn để phun thuốc. Thuốc được đề nghị bởi Đề án đánh giá thuốc diệt muỗi WHO cũng có thể được sử dụng như larvicides để điều trị chứa nước tương đối lớn. Khuyến cáo người dân không nên đi du lịch đến các vùng đang có dịch bệnh để tránh lây lan bệnh[33] · [34]. Tại Pháp, ngày 28 tháng 1 năm 2016, Marisol Touraine, Bộ trưởng Bộ Y tế Pháp Marisol Touraine nhấn mạnh phụ nữ mang thai nên hoãn các kế hoạch chuyến đi đến Caribbean và French Guiana[35].
Tất cả những người đã bị nhiễm virus Zika và bạn tình của họ nên thực hành tình dục an toàn, bằng cách sử dụng bao cao su đúng cách và nhất quán. Các đối tác tình dục phụ nữ mang thai sống trong hoặc trở về từ những nơi truyền dẫn nội hạt của virus Zika xảy ra nên thực hành tình dục an toàn, mang bao cao su, hoặc kiêng trong suốt thai kỳ. Người dân sống trong khu vực có lây truyền của virus Zika xảy ra nên thực hành tình dục an toàn hay tránh hoạt động tình dục. Ngoài ra, những người trở về từ các khu vực dịch xảy ra nên áp dụng thực hành tình dục an toàn hơn hoặc xem xét kiêng ít nhất 4 tuần sau khi họ trở về để làm giảm nguy cơ lây truyền trở đi.
Sử dụng bao cao su khi quan hệ tình dục với người bị nhiễm virus Zika. Mặc dù đã phát hiện ARN của virus Zika trong sữa nhưng chưa có bằng chứng lây truyền virus Zika qua bú mẹ nên chưa có khuyến cáo kiêng cho con bú trong khi mẹ nghi ngờ hoặc xác định bị nhiễm virus Zika.
Hiện nay, có nhiều loại vắc-xin hiệu quả để chống lại các Flavivirus. Ví dụ, vắc xin sốt vàng và viêm não Nhật Bản đã được giới thiệu vào năm 1930, trong khi vắc-xin sốt xuất huyết chỉ mới gần đây.[37][38]. Việc hướng tới sự phát triển một loại vắc xin chủng ngừa vi rút Zika đã được bắt đầu.[39] Và thời gian cần thiết để phát triển một loại vắc xin có hiệu quả, kiểm định để đưa vào sản xuất là quá trình lâu dài và phức tạp.[40] Người ta ước tính có thể mất ít nhất 10-12 năm để có một loại vắc xin hiệu quả đưa vào sử dụng chống lại virus Zika.[41]
Ngày 2/2 Hãng dược phẩm Sanofi (Pháp) thông báo đã bắt đầu dự án phát triển một loại vaccine phòng virus Zika.[42]
Bharat Biotech, một công ty dược phẩm Ấn Độ tuyên bố họ đã phát triển một loại vắc xin cho virus Zika. Hiện tại, thời điểm hai loại vaccine này có mặt trên thị trường vẫn chưa được xác định rõ.[43]
Tuy vậy, trong thời gian chờ đợi vắc xin, các nhà khoa học đề xuất ý tưởng dùng muỗi đột biến gen để ngăn ngừa virus Zika lây lan. Các thí nghiệm của Oxitec được tiến hành tại nhiều địa điểm khác nhau của châu Mỹ La tinh và châu Á. Kết quả cho thấy muỗi đột biến gen làm quần thể muỗi tự nhiên giảm số lượng đến 90%. Mở ra một giải pháp mới cho việc giảm sự lây lan bệnh xuất xuất huyết và virus Zika trong khi các phương pháp chữa trị đang được nghiên cứu. [44]
Virus được phát hiện ra vào năm 1947 từ khỉ Macaca mulatta trong rừng Zika của Uganda và vào năm 1968 đã được phát hiện trên con người ở Nigeria.[12] Từ năm 1951 đến tận năm 1981, bằng chứng nhiễm trên con người đã được báo cáo từ các nước châu Phi khác như là Cộng hòa Trung Phi, Ai Cập, Gabon, Sierra Leone, Tanzania, và Uganda, cũng như tại một số nước châu Á bao gồm Ấn Độ, Indonesia, Malaysia, Philippines, Thái Lan, và Việt Nam.[12]
Trong năm 2015, đã được phát hiện RNA của virus Zika trong ối của hai bào thai, chỉ ra rằng đã vượt qua nhau và có thể gây ra lây truyền dọc của các bệnh từ mẹ sang con.[45] Ngày 20 tháng 1 năm 2016, các nhà khoa học từ tiểu bang Parana ở Brazil đã phát hiện ra vật liệu di truyền của virus Zika trong nhau thai của một người phụ nữ bị sảy thai nhi vì tật đầu nhỏ, họ khẳng định rằng virus này có khả năng truyền qua nhau thai .[46]

Sau Brazil virus Zika lần lượt tấn công các quốc gia ở khu vực Nam Mỹ, các nước lân cận khu vực này và nhanh chóng lan sang Châu Á [102]. Các quốc gia láng giềng của Việt Nam như Lào[103], Campuchia, Thái Lan [104], Trung Quốc[105], Hàn Quốc, Singapore,... lần lượt lên tiếng xác nhận về những trường hợp đầu tiên nhiễm virus Zika.
Đến ngày 5/4/2016, Bộ Y tế Việt Nam chính thức xác nhận 2 ca dương tính với virus Zika tại Khánh Hòa và Thành phố Hồ Chí Minh.[106] Ngay sau khi công bố thông tin trên, Bộ Y tế đã nâng mức cảnh báo với virus Zika trên toàn quốc.
Ngày 29/8/2016, Y tế Singapore chính thức xác nhận có 1 trường hợp bị nhiễm Zika, và đặc biệt bệnh nhân này không đến bất kì quốc gia nhiễm Zika nào trong thời gian gần đây. Đến ngày 31/8/2016, số ca nhiễm đã tăng lên 82 ca.
Ngày 2/2/2016, WHO ban bố Tình trạng Khẩn cấp Y tế Công cộng Quốc tế về virus Zika, được đặt trong cùng hạng mục với Ebola. Giám đốc Tổ chức Y tế Thế giới (WHO) gọi Zika gây bệnh đầu nhỏ là "sự kiện bất thường", đòi hỏi phản ứng phối hợp nhanh chóng của toàn nhân loại.[107]
Văn phòng Tây Thái bình dương của WHO ở Manila (Philippines) dự báo virus Zika sẽ xuất hiện tại Đông Nam Á vì khu vực này có nhiều muỗi vằn Aedes.
Bộ Y tế các nước Đông Nam Á khuyến cáo tất cả khách du lịch, đặc biệt là những người đến từ Nam Mỹ và Trung Mỹ khi có triệu chứng sốt và mẩn đỏ phải báo cáo đến cơ sở y tế gần nhất.
Tại Việt Nam, Bộ Y tế Việt Nam cùng với các cơ quan chức năng đang triển khai các hoạt động kiểm dịch y tế tại các cửa khẩu quốc tế; giám sát chặt chẽ các hành khách nhập cảnh, đặc biệt những người đi về từ những vùng đang có dịch để phát hiện sớm các trường hợp nghi ngờ mắc bệnh, cách ly, xử lý kịp thời; tăng cường công tác phòng chống dịch bệnh do virus Zika đáp ứng các hoạt động khi dịch bệnh đang xâm nhập.[108]
Hơn 150 chuyên gia y tế trong một bức thư ngỏ đề nghị di dời thời gian hoặc không gian của Thế vận hội tại Rio vì dịch Zika. Trong một bài viết được công bố ngày 27/5 viết cho Tổ chức Y tế Thế giới (WHO) ở Geneva, các chuyên gia cảnh báo về nguy cơ sức khỏe toàn cầu. Nửa triệu người đi xem các trận đấu thế vận hội có thể bị nhiễm ở Rio de Janeiro và mang bệnh này về quốc gia của họ. 151 người ký là chuyên gia của các đại học và các trung tâm y tế ở 29 nước, bài viết được soạn thảo bởi Amir Attaran của đại học Ottawa, Arthur Caplan và Lee Igel của đại học New York và Christopher Gaffney của đạ học Zürich.[109] Nhưng, Ủy ban Olympic Quốc tế bác bỏ bức thư này vì cho rằng, thời gian tổ chức Thế vận hội Mùa hè 2016 ở Brasil là mùa đông nên tỉ lệ bị nhiễm Zika tại đây khá thấp, thậm chí là 0%.
|prénom2= (trợ giúp); Đã bỏ qua tham số không rõ |nom1= (trợ giúp); Đã bỏ qua tham số không rõ |nom2= (trợ giúp); Đã bỏ qua tham số không rõ |prénom1= (trợ giúp) |idioma= (trợ giúp); Đã bỏ qua tham số không rõ |volumen= (trợ giúp) |date=, |accessdate= (trợ giúp) |date=, |accessdate= (trợ giúp) |date= (trợ giúp) |accessdate= (trợ giúp) |date=, |accessdate= (trợ giúp) |date= (trợ giúp) |date=, |accessdate= (trợ giúp) |accessdate= (trợ giúp) |tựa đề= trống hay bị thiếu (trợ giúp) |date=, |accessdate= (trợ giúp) |date=, |accessdate= (trợ giúp) Virus Zika (ZIKV) là một virus RNA (arbovirus) thuộc chi Flavivirus, họ Flaviviridae, lây truyền chủ yếu qua vết cắn của muỗi Aedes bị nhiễm. Tên của virus lấy tên từ khu rừng Zika, gần hồ Victoria ở Uganda, nơi đầu tiên phân lập vào năm 1947. Virus Zika có liên quan đến bệnh sốt xuất huyết, sốt vàng da, viêm não Nhật Bản, và West Nile virus. Virus Zika đã có mặt ở khu vực nhiệt đới của châu Á và châu Phi từ năm 1950. Đây là virus mới nổi, chịu trách nhiệm cho một số dịch bệnh: năm 2007 trên đảo Yap, liên bang Micronesia, sau đó lan về phía đông qua Thái Bình Dương đến Polynesia thuộc Pháp, tiếp đến đảo Phục Sinh; đến 2015 qua Trung Mỹ, vùng Caribbean, và Nam Mỹ, nơi sốt Zika đã đạt đến cấp đại dịch. Các trường hợp đầu tiên được phát hiện ở Brazil; quốc gia này đang bị ảnh hưởng nặng nhất với hơn 1.500.000 trường hợp (0,72% dân số Brazil).
Virus Zika xác định qua phát hiện bộ gen bằng PCR. Đến nay bệnh do Zika gây nên chưa có thuốc điều trị đặc hiệu và chưa có vắc xin phòng bệnh vì vậy diệt vec tơ truyền bệnh với sự tham gia tích cực của cộng đồng là biện pháp hiệu quả nhất trong phòng chống bệnh.
Đợt nhiễm virua zika được gọi là sốt Zika, thường không có hoặc chỉ có triệu chứng nhẹ, tương tự như dạng rất nhẹ của bệnh sốt xuất huyết. Zika có thể lây từ bà mẹ qua thai nhi. Điều này có thể dẫn đến tật đầu nhỏ ở trẻ sơ sinh và các biến chứng não nghiêm trọng khác. Người lớn có thể nhiễm Zika, hiếm khi dẫn đến hội chứng Guillain Barre - hội chứng tổn thương thần kinh có thể gây liệt.
Vào tháng 1 năm 2016, Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa kỳ (CDC) đã ban hành hướng dẫn du lịch các nước bị ảnh hưởng, bao gồm cả việc sử dụng các biện pháp phòng ngừa tăng cường, và hướng dẫn cho phụ nữ mang thai bao gồm xem xét hoãn các chuyến đi du lịch. Chính phủ một số nước và các cơ quan sức khỏe trên thế giới cũng đưa ra cảnh báo du lịch tương tự, trong khi Colombia, Cộng hòa Dominica, Ecuador, El Salvador, và Jamaica khuyên phụ nữ trì hoãn việc mang thai cho đến khi hơn được biết rõ về những nguy cơ.
Vào ngày 1 tháng 2 năm 2016, Tổ chức Y tế Thế giới (WHO) ban bố tình trạng Khẩn cấp Y tế Công cộng Quốc tế về virus Zika, sau khi tham khảo ý kiến từ các chuyên gia hàng đầu về dịch tễ học, y tế công cộng và bệnh truyền nhiễm từ khắp thế giới tại một cuộc họp của Ủy ban khẩn cấp y tế quốc tế thuộc WHO. Virus Zika đã lây hơn 70 quốc gia và vùng lãnh thổ, trong đó có 57 quốc gia và vùng lãnh thổ tiếp tục có sự lây truyền của virus Zika do muỗi truyền, khiến nguy cơ xảy ra dịch là rất lớn. Tổ chức này cảnh báo dịch Zika có thể diễn biến tồi tệ hơn trước khi được kiểm soát và khuyến cáo người dân thực hiện các biện pháp chống muỗi và tránh bị muỗi đốt.
На основании филогенетического анализа обширного набора штаммов вируса была высказана гипотеза, что вирус Зика впервые появился в Уганде в 20-е годы XX века, после чего дважды независимо распространился в Западную Африку — около 1935 года в Нигерию и Сенегал через ЦАР, а также около 1940 года в Кот-д’Ивуар и затем в Сенегал; азиатские штаммы вируса, вероятно, в конце 1940-х были занесены в Малайзию, а в 1960-е — в Микронезию[16].
Предполагается, что вирус первоначально инфицирует дендритные клетки около места внедрения, затем распространяется в лимфатические узлы и кровоток[12]. Репликация флавивирусов обычно происходит в цитоплазме, однако белок оболочки вируса Зика был обнаружен в ядрах инфицированных клеток с помощью моноклональных антител к вирусу Западного Нила[17].
Основной путь передачи вируса Зика человеку — через укусы самок активных в дневное время комаров рода Aedes[5]: прежде всего Aedes aegypti и Aedes albopictus, а также древесных комаров Aedes africanus, Aedes apicoargenteus, Aedes furcifer, Aedes hensilli, Aedes luteocephalus и Aedes vitattus. Инкубационный период в комарах составляет примерно 10 дней[15]. Позвоночные носители вируса — как правило, обезьяны и люди. До начала пандемии в 2007 году вирус Зика «редко вызывал заметные „избыточные“ заболевания у человека, даже в высоко энзоотичных районах»[4].
Возможна передача вируса Зика от мужчины к женщине либо иному пассивному половому партнёру в результате полового контакта. Первый случай был зарегистрирован в 2009 году, когда по возвращении из экспедиции в Сенегал учёный-энтомолог из Колорадо передал вирус своей жене; симптомы лихорадки Зика проявлялись у них спустя порядка 9 дней после предполагаемой даты инфицирования[18][19]. Во время эпидемии лихорадки Зика во Французской Полинезии (2013) вирус был обнаружен в семенной жидкости и моче одного из пациентов на Таити, дважды перенесшего острую фазу заболевания в течение 8 недель; несмотря на наличие вируса в сперме, в крови его обнаружить в это же время не удавалось[20]. В обоих случаях у пациентов наблюдалась гемоспермия[18][20]. Во время вспышки 2015—2016 годов только в США было зарегистрировано 6 случаев передачи вируса половым путём[21]. Передача вируса женщинами не регистрировалась[21]. Согласно рекомендациям Центра по контролю и профилактике заболеваний США (CDC), для предотвращения передачи вируса Зика половым путём мужчинам следует постоянно использовать презервативы либо воздерживаться[en] от половых контактов: не менее 8 недель после посещения эндемичных территорий при отсутствии симптомов заболевания, не менее 6 месяцев после перенесённого заболевания с клиническими проявлениями[21].
В 2015 году РНК вируса Зика была обнаружена в околоплодных водах двух зародышей. Это показало, что вирус проникает через плаценту и может вызвать инфекцию у плода[22].
Общие симптомы вирусной инфекции включают лёгкую головную боль, макуло-папулезную сыпь, жар, недомогание, конъюнктивит и боли в суставах. Первый хорошо задокументированный случай заражения вирусом Зика был описан в 1964 году. В начале заболевания пациент жаловался на лёгкую головную боль, затем последовала сыпь, лихорадка и боль в спине. В течение двух дней сыпь начала проходить, через три дня спал жар и осталась только лёгкая сыпь. Сыпь была наиболее распространённым симптомом среди заболевших лихорадкой Зика в 2015 году в Рио-де-Жанейро[23]. До настоящего времени лихорадка Зика считалась достаточно лёгким заболеванием. Только у одного человека из пяти проявлялись симптомы заболевания, отсутствует смертность, однако истинный потенциал вируса до сих пор не известен[15].
По состоянию на июнь 2016 года не существует вакцин и лекарств для профилактики или специфического лечения лихорадки Зика. Симптомы можно облегчить, используя парацетамол, тогда как аспирин и другие НПВС можно применять только после исключения лихорадки денге из-за риска кровотечений[24].
Вирус обладает выраженным нейротропизмом и эффективно инфицирует нейрональные прогениторные клетки. С помощью органоидов, имитирующих эмбриональное развитие переднего мозга[en], были продемонстрированы нарушения, возникающие при размножении вируса Зика в мозге плода, и их аналогия с изменениями, характерными для микроцефалии[25].
Существуют два типа диагностических тестов для определения вируса Зика в сыворотке, выделенной во время острой фазы заболевания[26][15]. Иммуноферментные тесты построены на определении специфичного иммуноглобулина M; часто дают перекрёстные реакции с вирусом денге, реже — с вирусами жёлтой лихорадки, лихорадки Западного Нила, японского энцефалита, энцефалита долины Муррея[15], однако существуют и достаточно специфичные наборы для ИФА[27]. Тесты, основанные на прямом определении вируса или его компонентов, более надёжны, однако длительны и требуют более квалифицированного персонала[26][15]. ПЦР-тесты, основанные на определении вирусной РНК, наиболее популярны и могут проводиться с использованием образцов, полученных не позднее 10 дней после начала заболевания[26][15]. Реакция нейтрализации методом бляшек имеет более высокую специфичность[15].
Схемы дифференциальной диагностики различаются в зависимости от фазы заболевания. Во время острой фазы (< 7 дней после появления симптомов) сначала проводится определение белка NS1 вируса денге методом ПЦР в реальном времени, затем при отрицательном результате тем же методом проводится определение вируса чикунгунья. При отрицательных результатах обоих тестов и положительном результате ПЦР-теста на вирус Зика ставится диагноз. На более поздних стадиях (> 4 дней после появления симптомов) по аналогичной схеме проводится диагностика на основе определения специфичных IgM[5].
7-Деаза-2′-C-метиладенозин[d] проявляет ингибиторные свойства по отношению к репликации вируса Зика[28][29] и замедляет течение болезни у мышей[28]. 2′-C-Метилцитидин, рибавирин, фавипиравир[en] и T-1105 ингибируют цитопатическое действие вируса и уменьшают его урожай[28]. Высокую эффективность подавления репродукции вируса in vitro проявляет также 2′-C-метиладенозин, 2′-C-метилгуанозин и 2′-C-метилуридин менее эффективны[29]
На основании филогенетического анализа обширного набора штаммов вируса была высказана гипотеза, что вирус Зика впервые появился в Уганде в 20-е годы XX века, после чего дважды независимо распространился в Западную Африку — около 1935 года в Нигерию и Сенегал через ЦАР, а также около 1940 года в Кот-д’Ивуар и затем в Сенегал; азиатские штаммы вируса, вероятно, в конце 1940-х были занесены в Малайзию, а в 1960-е — в Микронезию.

寨卡病毒(英语:Zika virus, ZIKV,马新译作茲卡病毒,香港译作寨卡病毒,台湾译作茲卡病毒),是黃病毒科中之黃病毒屬,經由埃及斑蚊傳播,而使受斑蚊叮咬的人罹患茲卡病毒感染症(亦稱寨卡熱)[1]。該病毒最早在1947年於烏干達的寨卡森林中的獼猴體內分離出來,因而得名。依據基因型別分為亞洲型和非洲型兩種型別,在中非、東南亞和印度等都有發現的紀錄。過去只有少數人類病例的報導,直到2007年在密克羅尼西亞聯邦的雅蒲島爆發群聚疫情,才對此疾病有較多的認識。
2015年起茲卡病毒疫情於中南美洲快速擴散,其中巴西甚至出現超過4,100例新生兒小頭畸形,新生兒小頭畸形被懷疑與茲卡病毒相關,世界衛生組織與美國政府都提出緊急因應措施[2]。
茲卡病毒與登革熱,黃熱病,日本腦炎和西尼羅河病毒有親屬關係。它會引發類似溫和的形式的登革熱的症狀,由休息與症狀治療,目前還無法通過藥物或疫苗來預防。茲卡病毒經由母親傳染給孩子,新生嬰兒感染此病毒可能導致小頭畸形,而成人感染可能影響神經系統,包括格林-巴利综合征亦可能有所關聯。
在2016年1月,美国疾病控制与预防中心(CDC)發布了受影響的國家名單,包括強化注意事項,建議孕婦考慮推遲旅行的旅行指南。其他國家的政府或健康部門也很快發出類似的旅行警告,而哥倫比亞,多明尼加共和國,厄瓜多爾,薩爾瓦多,牙買加建議女性推遲懷孕,直到更多的人知道其中的風險。
茲卡病毒有包膜呈二十面體,就像是與它有親屬關係的其他病毒,並且具有不分段,單股正鏈RNA基因組。這是與斯龐德溫尼病毒(Spondweni virus)密切相關的病毒,是斯龐德溫尼病毒病毒進化枝兩種病毒之一。
該病毒最早在1947年4月由黃熱病研究所的科學家從被放置在一個籠子中的獼猴分離出,地點在烏干達,維多利亞湖附近的茲卡森林[3]。隨後在1948年1月在同一地點,從非州斑蚊第二次被分離出來。在1952年當猴子出現發燒症狀,研究人員從它的血清中分離出傳播病原體,這是第一次描述為茲卡病毒。在1968年它首次從尼日利亞人分離出來。從1951年到1981年人類感染的證據是從其他非洲國家如中非共和國,埃及,加蓬,塞拉利昂,坦桑尼亞和烏干達,以及在亞洲的部分地區,包括印度,印度尼西亞,馬來西亞,菲律賓,泰國和越南都有報導。
茲卡病毒有非洲裔和亞洲裔兩個譜系。演化學研究顯示,在美洲蔓延的病毒與法屬波利尼西亞的菌株密切相關。茲卡病毒的完整基因組序列已經公佈。從最近序列調查初步結果,在公共領域發現了一個在非結構蛋白1密碼子可能的變化,這可能會增加在人體中病毒複製的速度。
寨卡病毒病的潜伏期(从接触到出现症状的时间)并不为人所知,但可能为几天。其病症與登革熱等其它蟲媒病毒感染相似,包括發熱、皮疹、结膜炎、肌肉和關節痛、全身乏力、眼窩痛以及头痛。这些症状往往较轻,持续2-7天[3]。
2013-2014年在法属波利尼西亚发生了首起寨卡病毒病疫情,当时还同时出现了登革热疫情,国家卫生当局在此期间报告称,格林-巴利綜合徵出现非正常上升[3]。
格林-巴利综合征是身体免疫系统侵袭部分中枢神经系统而出现的病情。它可由多种病毒引起,并可影响任何年龄的人。尚不了解究竟是什么原因引发该综合征。主要症状包括肌肉无力,胳膊和腿酸麻。如呼吸肌受到影响,则可发生严重并发症,需要住院治疗。受格林-巴利综合征影响的大多数人会痊愈,有些人可能会继续感到身体无力等[4]。
2015年在巴西出现的疫情中,当地卫生当局发现在普通民众中间发生的寨卡病毒感染有所上升,且在巴西东北部出生并患有小头症(microcephalin)的婴儿数量出现增多情况。对寨卡疫情开展调查的机构发现,越来越多的证据表明寨卡病毒与小头症之间存有关联[3]。
主要是人被帶有茲卡病毒的斑蚊叮咬後,經過約3-12天的潛伏期後,約五分之一感染者會發病出現症狀。感染者在發病時期,血液中存在寨卡病毒,此時如再被病媒埃及斑蚊叮咬,病毒將在病媒埃及斑蚊體內增殖,約10天左右[5],病毒進入埃及斑蚊的唾液腺,就具有傳播病毒的能力,而當埃及斑蚊再叮咬其他健康人時,這個健康的人就會感染茲卡病毒。此外,也可能經由性行為[6]、垂直傳染(在懷孕期間由母親傳染給胎兒)[7][8][3]而感染。
世界卫生组织(WHO)表示该病毒有可能通过性接触在人與人之間傳播,不过仍需更多研究以确认性传播是否为兹卡病毒的传播途径之一。 在2016年1月25號倫敦衛生與熱帶醫學院的Laura Rodrigues教授於2016年1月25號強調發展茲卡病毒疫苗的重要性,應該如同德國麻疹疫苗一樣給予有生育計劃的女性接種以防止懷孕時受到病毒感染而導致畸胎。在疫苗出現前,對於想要懷孕或已經懷孕的女性而言應該小心被蚊蟲叮咬以及避免前往高風險的疫區[3]。
寨卡病毒(英语:Zika virus, ZIKV,马新译作茲卡病毒,香港译作寨卡病毒,台湾译作茲卡病毒),是黃病毒科中之黃病毒屬,經由埃及斑蚊傳播,而使受斑蚊叮咬的人罹患茲卡病毒感染症(亦稱寨卡熱)。該病毒最早在1947年於烏干達的寨卡森林中的獼猴體內分離出來,因而得名。依據基因型別分為亞洲型和非洲型兩種型別,在中非、東南亞和印度等都有發現的紀錄。過去只有少數人類病例的報導,直到2007年在密克羅尼西亞聯邦的雅蒲島爆發群聚疫情,才對此疾病有較多的認識。
2015年起茲卡病毒疫情於中南美洲快速擴散,其中巴西甚至出現超過4,100例新生兒小頭畸形,新生兒小頭畸形被懷疑與茲卡病毒相關,世界衛生組織與美國政府都提出緊急因應措施。

ジカウイルス(英: Zika virus)は、フラビウイルス科に属する+鎖のRNAウイルスの1種である。1947年、ウガンダにあるジカ森(英語版)のアカゲザルから初めて分離された[1][2]。
ジカウイルスに感染することで引き起こされる症状はアフリカからアジアにかけての赤道付近の限られた緯度の範囲で1950年代から知られており、ジカウイルス感染症またはジカ熱(以下この記事においてジカ熱という)と呼ばれる。
지카바이러스(영어: zika virus, ZIKV, 포르투갈어: Vírus Zika, 문화어: 지카비루스)는 플라비 바이러스과와 플라비바이러스속에 속하는 바이러스로, 숲모기를 통해 전염된다. 사람에서는 지카열로 알려진 가벼운 증상의 병을 일으키는데, 이 병은 1950년대 이후로 아프리카에서 아시아에 이르는 좁은 적도 대 안에서 발생하는 것으로 알려졌다. 2014년, 지카 바이러스는 태평양을 건너 프랑스령 폴리네시아에, 그리고는 이스터섬, 2015년에는 중앙 아메리카, 카리비아 해로, 남아메리카에서 발생한 지카 바이러스는 범유행의 수준에 이르렀다.[1] 증상은 가벼운 뎅기열과 같고,[2] 휴식을 통해 치료하며,[3] 약이나 백신으로 예방할 수 없다.[3] 지카 열병은 다른 절지동물매개성 플라비바이러스에 의한 황열병과 웨스트 나일 열병에 관련되어 있다.[2] 현재로서는 지카 열병이 바이러스에 감염된 산모에게서 난 신생아의 소두증과 관련되었을 수 있다고 여겨진다.[4][5] 2016년 1월, 미국 질병통제예방센터(CDC)는 열병이 발생한 나라의 여행에 대한, 주의의 강화와 여행의 연기, 임신한 여성을 위한 안내를 포함하는 안내문을 발표하였다.[6][7] 곧이어 다른 정부와 보건 단체에서도 유사한 여행 경고를 발표하였고,[8][9][10][11] 콜롬비아, 에콰도르, 엘살바도르, 자메이카에서는 위험에 대해 더 알게 되기 전까지 여성의 임신을 연기할 것을 권고하였다.[9][12]
같은 과의 다른 바이러스들처럼 지카 바이러스는 막에 싸여 있고 분할 되지 않은 외가닥의 양성가닥 RNA 게놈의 정이십면체이다. 이 바이러스는 스폰드웨니 바이러스와 가장 밀접하게 상관돼 있고 스폰드웨니 바이러스 계통군의 두 바이러스 중 하나이다.[13][14]
지카 바이러스는 1947년 우간다 지카 숲의 히말라야원숭이로부터 처음으로 분리되었고, 1968년에는 나이지리아에서 사람으로부터 최초로 분리되었다.[15] 1951년부터 1981년까지, 사람에 전염된 증거가 중앙아프리카공화국, 이집트, 가봉, 시에라리온, 탄자니아, 우간다 등 아프리카의 여러 나라로부터 보고되었고, 인도, 인도네시아, 말레이시아, 중화민국, 태국, 베트남, 일본 등을 포함한 일부 아시아 국가에서도 보고되었다.[15]
바이러스의 발병기전은 림프절과 혈류로 퍼진 후에 주입부 부근의 수지상 세포를 감염시키면서 시작되는 것으로 추정된다.[16] 플라비바이러스는 일반적으로 세포질 안에서 복제하지만, 지카 바이러스 항원은 감염된 세포핵들에서 줄곧 발견되었다.[17]
두 계통의 지카바이러스 즉 아프리카 계통과 아시아 계통이 있다.[18] 계통학적 연구는 아메리카 대륙에 퍼진 바이러스가 2013년 발발 동안에 프랑스령 폴리네시아에 퍼진 아시아 계통에 가장 밀접하게 상관돼 있다는 것을 나타낸다.[18][19] 이 지카바이러스의 완전한 게놈 서열은 공표되었다.[20]
지카 바이러스는 주간에 활동적인 모기에 의해 전파된다. 이 바이러스는 알을 낳는 암컷 이집트 숲모기(Aedes aegypti)가 주로 전파하지만[21] 아프리카 숲모기(Aedes africanus)를 포함해서 모기의 외적인 부화 기간이 약 10일이면서 나무 위에서 사는 숲모기속의 여러 종으로부터 분리된 바 있다.[15][22] 척추동물의 숙주는 주로 원숭이와 사람이다. 2007년에 시작된 현재의 범유행 전에는 지카 바이러스는 '풍토성이 강한 곳에서도 사람에게는 드물게 유행하는 감염'으로 여겨졌다.[23]
매개체의 실제의 범위는 아직 알려져 있지 않다. 지카바이러스는 Anopheles coustani, Mansonia uniformis, Culex perfuscus와 함께 숲모기 속의 더 많은 모기에서 감지되었지만 그것만으로 그들을 매개체로 단정하기는 어렵다.[24]
흰줄숲모기(Aedes albopictus)에 의한 전파가 가봉의 한 2007년 교외 지역의 발발에서 보고되었는데, 이 전파가 새로 이 국가를 침입해서 병존하는 치쿤구니야 및 뎅기열 바이러스 발생에 대한 주매개체가 되었다.[25] 지카바이러스 감염을 실험실에서 확진한 이탈리아로 수입된 최초 두 증례가 프랑스령 폴리네시아에서 돌아온 바이러스혈증 여행객에게서 왔기 때문에 흰줄숲모기에 감염된 유럽 국가의 도시권에서는 현지 감염에 대한 우려가 있다.[26]
지카 바이러스의 잠재적인 사회의 위협은 이를 전파하는 모기(매개체)의 분포로 한계를 정할 수 있다. 가장 많이 언급되는 지카 바이러스의 매개체인 이집트 숲모기의 세계 분포는 세계무역과 여행에 의해 확장되고 있다.[27] 이집트 숲모기는 현재 역대 최대 규모, 북아메리카와 유럽 부근(마데이라 제도, 네덜란드, 흑해 북동 해안)을 포함한 모든 대륙으로 확장되어 있다.[28] 지카바이러스를 전달할 수 있는 한 모기 개체군이 워싱턴 D. C.에 이웃한 캐피틀힐에서 발견되었고 유전적 증거는 이들이 적어도 그 지역의 네 연속적 겨울에 살아남았다는 것을 시사한다. 이 연구 저자는 이 모기들이 (미국) 북부 기후에 끈질기게 적응하고 있다고 결론지었다.[29]
국제 보건 단체들의 현재의 관심은 라틴 아메리카와 카리브해 지역에 집중되어 있다. 범미주 보건 기구(Pan American Health Organisation, PAHO)에서 지역적인 지카 바이러스 전파가 있었음이 확인된 나라와 지역은 바베이도스, 볼리비아, 브라질, 콜롬비아, 도미니코 공화국, 에콰도르, 엘살바도르, 프랑스령 기아나, 구아테말라, 과들루프, 가이아나, 하이티, 온두라스, 마르티니크, 멕시코, 파나마, 파라과이, 푸에르토리코, 세인트마틴섬, 수리남, 베네수엘라 등이다.[30][31] 묘하게도 지카 바이러스는 치쿤구니야 바이러스병의 세계 전파를 따르는 것처럼 보인다.[23]
2009년 콜로라도주립대학교 절지동물매개성 감염병 연구소(Arthropod-borne and Infectious Diseases Laboratory)의 사례에서는 한 생물학자가 그의 아내에 지카 바이러스를 성적 접촉으로 감염시켰다. 그는 모기의 연구를 위해 세네갈을 방문했고, 수 차례 모기에 물렸다. 며칠 후 미국에 돌아갔을 때 지카열이 발병했으나, 이는 그의 아내와 무방비로 성관계를 가진 후였다. 그의 아내는 후에 빛에 극도로 예민해지는 등의 지카 감염 증세를 보였다. 이는 알려진 사례 중 사람 사이에 성적 접촉으로 곤충매개성 바이러스가 전파된 최초의 경우이다.[32][33]
2015년, 지카 바이러스의 RNA가 두 태아의 양수 안에서 발견되어, 바이러스가 태반을 통과하여 태아감염을 일으킬 수 있음이 시사되었다.[34] 2016년 1월 20일, 브라질 파라나 주의 과학자들은 태아의 소두증으로 임신중절한 여성의 태반에서 지카 바이러스의 유전 물질을 발견하여 바이러스가 태반을 통과할 수 있음을 확인하였다.[35]
지카 바이러스 감염의 흔한 증상은 가벼운 두통, 반점구진발진, 열, 권태감, 결막염, 관절통 등을 포함한다. 1964년에 관련 증거가 많은 사례로서는 최초로 지카 바이러스가 묘사되었다. 이 병은 가벼운 두통으로 시작하여 반점구진발진, 열, 요통으로 진행되었다. 2일 안으로 발진은 사라지기 시작했고, 3일 안으로 열은 내리고 발진만 남았다. 현재까지 지카열은 범위가 한정되고 5명 중 1명 꼴로 증상이 나타나고 치명적이지 않은 상대적으로 가벼운 병이었다.[15]
2016년 1월 현재까지 백신이나 예방약은 없다. 병의 증상은 아세트아미노펜으로 치료하며, 아스피린과 다른 비스테로이드 항염증제는 출혈의 위험을 줄이기 위해 댕기열이 배제되었을 때에만 사용해야 한다.[36]
프랑스령 폴리네시아 유행병에서는 길랭-바레 증후군이 73건 발생했고, 27만 명에서 지카열의 합병증일 가능성이 있는 다른 신경 상태가 발생하였다.[23] 2015년 12월, 유럽 질병예방통제센터(European Centre for Disease Prevention and Control, ECDC)는 지카 바이러스가 선천성 소두증과 이러한 증후군이 연관될 수 있음을 종합적으로 갱신하여 발표하였다.[37]
자료가 시사하는 바에 의하면, 임신 첫 3개월 동안 지카 바이러스에 감염된 임산부에게서 난 갓난아기는 소두증의 위험이 몇배로 더 증가한다.[38] 2015년 12월 이후로 태아의 태반경유감염이 소두증과 두뇌 손상을 초래할 수 있음이 의심되었다. (하지만 증명되지는 않았다.)[39][40] 어쨌든, 브라질 보건부(Ministry of Health)는 지카 바이러스와 소두증과의 관련성을 확인한 바 있다.[41]
다른 뇌질환과도 관련 가능성이 제기되었는데, 감염환자들 가운데 6명에게서 자가면역질환성 뇌 신경 이상 증상이 나타났다. 이 중 길랑-바레증후군증이 포함되어 있으며 급성 산재성 뇌척수염(ADEM)도 나타났다.[42]
2013년, 지카바이러스에 대항하는 항바이러스제는 없으며 치료는 증상 관리에 기반을 두고 있다. 플라비바이러스에는 흔한 출혈을 유도할 수 있는 이부프로펜, 아스피린 사용을 피해야 하며, 열과 통증에 대처하기 위해 아세트아미노펜을 사용할 수 있다.[43] 발진이 가려우면 디펜히드라민을 사용할 수도 있다.[44]
2016년 초, 이 바이러스에 대항할 수 있는 치료제와 백신이 없었다.[45] 이 바이러스의 NS1 항원에 대항하기 위한 방법으로는 면역글로불린 M과 면역글로불린 G를 감지하는 효소 결합 면역 침강 분석법 검사가 있다.[46] 이 검사는 자동화되어 있으며 집단 선별 검사 운동을 채택했다. 백신이 없기 때문에 예방책은 살충제를 사용하면서 서식 장소(찻찬 받침, 배수로, 고인 물의 열린 저장소, 버려진 타이어 등)의 수를 줄임으로써 매개체를 통제할 수 있다[47]. 긴 옷을 입는 것과 방충제와 방충망을 이용하는 것은 바이러스나 다른 질병의 잠재적 매개체인 모기에 물릴 위험을 줄여줄 것이다. 이 원칙은 새로운 매개체를 피하려는 일부 감염된 사람들에게도 적용된다.
이러한 이유로 새로운 지역에 질병을 전파하는 것을 막기 위해 아픈 사람이 여행하는 것은 권고되지 않는다.[48][49] 프랑스에서는 보건부 장관 마리솔 투렌이 카리브해와 프랑스령 기아나로 임산부가 여행하는 것을 연기할 것을 ‘강력히’ 권고했다.[50]
1947년 황열병을 연구하던 과학자들이 우간다 엔테베의 동아프리카 바이러스 연구소(Uganda Virus Research Institute ,UVRI) 부근의 지카 숲('지카'는 간다어로 '제멋대로 자람'을 의미)의 우리 안에 히말라야 원숭이를 두었다. 원숭이는 열병에 걸렸고, 연구자들은 원숭이의 혈청에서 전파성 물질을 분리하였고, 1952년에 처음으로 지카 바이러스로 기술하였다.[51] 1954년에는 나이지리아에서 사람으로부터 바이러스가 분리되었다. 발견 이후 2007년까지 아프리카와 동남아시아의 확인된 지카 바이러스 감염 사례는 드물었다.[52]
지카바이러스는 우간다와 나이지리아의 혈청학적 조사의 결과로 인간을 감염시킨다는 것이 알려졌다. 전연령층 84명의 혈청학적 조사(serosurvey)에서 50명이 항체를 지니고 40세를 넘는 전연령에서 면역이 되는 것으로 나타났다.[53] 1954년이 되어서야 인간의 지카바이러스에 대한 성공적 분리가 공표되었다. 이 분리는 황열로 의심되는 황달에 대한 1952년의 발병 조사의 일환으로 이루어졌는데, 다시 말해 황달이 아닌 말라리아의 증거와 미열과 두통이 있는데도 3일만에 회복된 10살 여성의 혈액에서 발견된 것이다. 이 혈액을 15마리 경과까지 계속된 실험용 쥐의 뇌에 주입했다. 그 다음에 특별히 지카바이러스에 면역이 돼 있는 히말라야 원숭이 혈청을 이용한 중화 검사에서 쥐의 뇌의 바이러스가 시험되었다. 1명은 열과 황달과 기침과 광범위 관절통, 다른 1명은 열과 두통과 눈 뒤와 관절의 통증이 있는 두 감염 환자의 혈액에서는 대조적으로 어떤 바이러스도 분리되지 않았다. 감염은 지카바이러스 특이 혈청 항체의 발원으로 입증되었다.[53] 인도에서 수행된 한 연구에서는 '유의미한 수'의 인도인들이 이 바이러스에 면역 반응을 나타낸다는 것을 보여줬는데, 이는 이 바이러스가 인간 개체군 내에서 오랫동안 널리 퍼져 있었다는 것을 암시한다.[54]
1951년에서 1981년에 걸쳐 지카바이러스의 인간 감염의 증거가 중앙 아프리카 공화국, 이집트, 가봉, 시에라리온, 탄자니아, 우간다와 같은 다른 아프리카 국가뿐만 아니라 인도, 인도네시아, 말레이시아, 필리핀, 타이, 베트남과 같은 아시아 일부에서도 보고되었다.[55] 최초로 발견된 이후 2007년까지는 아프리카와 동남아시아에서 인간에 전염된 예는 14건 뿐이었다.[56]
2007년 4월, 미크로네시아 연방의 야프섬에서 아프리카와 아시아 외 지역에서는 처음으로 지카열이 발생하였다. 발진, 결막염, 관절통이 특징으로, 초기에는 뎅기열, 치쿤구니야 바이러스병, 로스리버 바이러스병으로 여겨지기도 했다.[57] 어쨌거나, 급성기 환자로부터의 혈청 표본은 지카 바이러스의 RNA를 포함하고 있었다. 확인된 발병 사례는 49건, 확인되지 않은 59건으로, 입원이나 사망은 없었다.[58] 이후 폴리네시아, 이스터 섬, 쿡 제도, 뉴칼레도니아에서도 유행병이 발생하였다.[52]
2015년 4월 이후 브라질에서 시작되어 광범위하게 발생이 진행중인 지카 바이러스는 남아메리카와 중앙 아메리카, 카리브 제도에까지 확산되었다. 2016년 1월, 미국 질병통제예방센터(Centers for Disease Control and Prevention, CDC)에서는 지카 바이러스의 전파가 진행되고 있는 지역으로의 여행에 대하여 2단계의 여행 경보를 발령하였다.[59] CDC는 또한 임신 계획이 있는 여성은 여행 전에 의사와 상의할 것을 제안하였다.[60] 영국의 정부 또는 보건 기관,[8] 아일랜드,[9] 뉴질랜드,[10] 캐나다,[11] 유럽 연합[11] 등도 곧이어 유사한 여행 경보를 발령하였다. 콜롬비아의 보건사회보호부(Ministry of Health and Social Protection) 장관은 8개월간 임신을 피할 것을 권고하였고, 에쿠아도르, 엘살바도르, 자메이카 등도 유사한 경고를 발표하였다.[9][12]
브라질 리오데자네이루 당국은 2016년 하계 올림픽 기간 동안 시내에서 지카 바이러스의 확산 방지를 위한 계획을 발표하였다.[11]
CDC에 의하면 브라질 보건당국은 2015년 10월부터 2016년 1월까지 3,500명 이상의 소두증 사례를 보고하였다. 영향을 받은 아기의 일부는 심한 소두증이 있었고, 일부는 목숨을 잃었다. 임신 중의 감염에 관련될 수 있는 결과의 전 영역과 태아에게 위험을 줄 수 있는 요소는 아직 충분히 밝혀지지 않았다. 임신 중 지카 바이러스 감염의 위험성에 대해서는 많은 연구가 계획되어있다.[61] 브라질에서 가장 심하게 영향을 받은 지역에서는 신생아의 약 1%가 소두증이 의심되었다.[62] 2016년 3월에는 쿠바에서도 지카바이러스에 감염된 첫번째 자국민 환자가 나타나 우려가 커지고 있다. 이 환자는 해외여행을 나간 이력이 없기 때문에 더 큰 의혹과 걱정을 야기시키는 일이라고 볼 수 있겠다.[63]
브라질은 올림픽을 통해 경제 상황을 좋게 하려고 시도하였으나 지카의 유행으로 타격을 입게 되었다.
|doi= 값 확인 필요 (도움말). |doi= 값 확인 필요 (도움말). |웹사이트=에 외부 링크가 있음 (도움말) 지카바이러스(영어: zika virus, ZIKV, 포르투갈어: Vírus Zika, 문화어: 지카비루스)는 플라비 바이러스과와 플라비바이러스속에 속하는 바이러스로, 숲모기를 통해 전염된다. 사람에서는 지카열로 알려진 가벼운 증상의 병을 일으키는데, 이 병은 1950년대 이후로 아프리카에서 아시아에 이르는 좁은 적도 대 안에서 발생하는 것으로 알려졌다. 2014년, 지카 바이러스는 태평양을 건너 프랑스령 폴리네시아에, 그리고는 이스터섬, 2015년에는 중앙 아메리카, 카리비아 해로, 남아메리카에서 발생한 지카 바이러스는 범유행의 수준에 이르렀다. 증상은 가벼운 뎅기열과 같고, 휴식을 통해 치료하며, 약이나 백신으로 예방할 수 없다. 지카 열병은 다른 절지동물매개성 플라비바이러스에 의한 황열병과 웨스트 나일 열병에 관련되어 있다. 현재로서는 지카 열병이 바이러스에 감염된 산모에게서 난 신생아의 소두증과 관련되었을 수 있다고 여겨진다. 2016년 1월, 미국 질병통제예방센터(CDC)는 열병이 발생한 나라의 여행에 대한, 주의의 강화와 여행의 연기, 임신한 여성을 위한 안내를 포함하는 안내문을 발표하였다. 곧이어 다른 정부와 보건 단체에서도 유사한 여행 경고를 발표하였고, 콜롬비아, 에콰도르, 엘살바도르, 자메이카에서는 위험에 대해 더 알게 되기 전까지 여성의 임신을 연기할 것을 권고하였다.