en
names in breadcrumbs

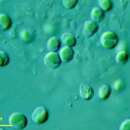
Nannochloropsis is a genus of algae comprising six known species. The genus in the current taxonomic classification was first termed by Hibberd (1981).[2] The species have mostly been known from the marine environment but also occur in fresh and brackish water.[3] All of the species are small, nonmotile spheres which do not express any distinct morphological features that can be distinguished by either light or electron microscopy. The characterisation is mostly done by rbcL gene and 18S rRNA sequence analysis.[4]
The algae of the genus Nannochloropsis differ from other related microalgae in that they have chlorophyll a and completely lack chlorophyll b and chlorophyll c. In addition they are able to build up a high concentrations of a range of pigments such as astaxanthin, zeaxanthin and canthaxanthin.[5] They have a diameter of about 2 to 3 micrometers[6] and a very simple ultrastructure with reduced structural elements compared to neighbouring taxa.
Nannochloropsis is considered a promising alga for industrial applications because of its ability to accumulate high levels of polyunsaturated fatty acids.[7][8] Moreover, it shows promising features that can allow genetic manipulation aimed at the genetic improvement of the current oleaginous strains. Various species of Nannochloropsis indeed are transfectable and there has been evidence that some strains are able to perform homologous recombination.[9] At the moment it is mainly used as an energy-rich food source for fish larvae and rotifers. Nevertheless, it has raised growing interest also for the investigation of biofuel production from photosynthetic organisms. (see Nannochloropsis and biofuels). Nannochloropsis is actually in use as food additive for human nutrition and it is also served at Restaurant "A Poniente" of El Puerto de Santa María (Cádiz, Spain) close to the natural environment where Nannochloropsis gaditana was first isolated and still grows.[10] A 2020 study suggests it could be used for a highly performant, sustainable fish-free feed for farmed fish.[11][12]
The species currently recognised are:
The scientific community has obtained the genomic sequence of different strains of Nannochloropsis belonging to two species: N. gaditana[14][15] and N. oceanica.[16][17] A genome portal based on the N. gaditana B-31 genome allows accessing much of the genomic information that concerns this micro-organism, moreover dedicated web pages are also available for the genomes of N. gaditana CCMP526 and N. oceanica CCMP1779.
The genomes of the sequenced Nannochloropsis strains were between 28.5 and 29 Mega bases long, they had high density of genes, reduced intron content, short intergenic regions[14] and very limited presence of repetitive sequences.[16] The genes of the two species share extended similarity.
The analysis of the genomes revealed that these microalgae have set of genes for the synthesis and incorporation in the cell wall of cellulose and sulfated fucans and that they are able to store carbon in polymers of β-1,3- and β-1,6-linked glucose called chrysolaminarin.[14] An NMR analysis of whole algal cells which were cultivated in autotrophic growth[18] reports evidence of the presence of cellulose in the cell wall and of mobile chrysolaminarin, probably accumulated in solution in vacuoles inside the cell.
Comparison between the lipid metabolic genes of N. gaditana and of red/green/brown algae and diatoms provided some insights into the exemplary lipid production of Nannochloropsis cultures. The comparisons indeed highlighted the presence of an expanded repertoire of some of the genes involved in TAG assembly in Nannochloropsis.[15] Numerous TAG lipases, which can affect TAG metabolism through either TAG degradation or lipid remodeling, were identified in Nannochloropsis,[16] many of them belonging to a gene family which seems to be exclusive of Nannochloropsis.[19]
Analysis of the genomic data suggested the presence in both the two species of Nannochloropsis of regulatory RNA and in particular miRNA.[14][16]
Various orthologs of known blue light sensing proteins were found in the genomes of Nannochloropsis suggesting possible circadian regulation.[14][16]
A research community from Qingdao Institute of Bioenergy and Bioprocess Technology (QIBEBT [1]), Chinese Academy of Sciences, sequenced and compared six Nannochloropsis genomes that include two N. oceanica strains (IMET1 and CCMP531) and one strain from each of four other recognized species: N. salina (CCMP537), N. gaditana (CCMP526, which was previously reported[15]), N. oculata (CCMP525) and N. granulata (CCMP529).[20] They found that the six genomes share key oleaginous traits, such as the gene dose expansion of selected lipid biosynthesis genes compared to green algae Chlamydomonas. The most prominent example of gene dose expansion is Diacylglycerol acyltransferase (DGAT), which catalyzes the last step of triacylglycerol (TAG) synthesis. There are 13 DGAT genes in Nannochloropsis, representing the highest gene dose in known genomes.
Through a comprehensive phylogenetic analysis, researchers proposed that among the 11 DGAT-2s, one gene might originate from the red algae related secondary endosymbiont, four from green algae related endosymbiont, and the other six from the eukaryotic host genome. In addition, a large proportion (15.3%) of TAG biosynthesis related genes were acquired by Nannochloropsis via horizontal gene transfer (HGT) from bacteria. Therefore, multiple genome pooling and horizontal genetic exchange, together with selective inheritance of lipid synthesis genes and species-specific gene loss, have led to the enormous genetic apparatus for oleaginousness and the wide genomic divergence among present-day Nannochloropsis spp.
When cultured in normal growth conditions in f/2 medium, a standard algal culture growth medium, supplemented with nitrogen, Nannochloropsis cells have an oil content of about 30% of their dry weight. This oil can be used to produce biodiesel. In order to produce biodiesel, the oil content of Nannochloropsis cultures must be increased. Fatty acid biosynthesis in N. oceanica was shown to be integrated with the regulation of the cholesterol biosynthetic pathway, suggesting new genetic engineering or chemical biology approaches for enhanced oil production in microalgae.[21] On the other hand, various culturing conditions were observed to increase the average oil content per cell, supporting however only slow growth rates of the cultures (see the related section Nannochloropsis and biofuels), and decreasing the overall productivity. Among these conditions, nitrogen deprivation has been one of the most vastly studied. Studies have examined the behaviour of the cultures in nitrogen stress in various culturing set-ups, as well as the physiological and molecular response of the cells to nitrogen deprivation.
Various strains of Nannochloropsis were shown to accumulate up to 60–70% of their overall biomass as lipids in nitrogen limitation.[8][22] In this condition not only the amount of lipids changes, but also the composition. It was observed that triacylglycerols largely increase in nitrogen depletion while other lipids, mainly polar glycerolipids, free fatty acids and diacylglycerols, slightly decrease. The increase in triacylglycerols in nitrogen depletion is much larger than the decrease in the other glycerolipids, supporting the hypothesis that the cells actively synthesise new triacylglycerols rather than just transforming the existing lipids into triacylglycerols.[23]
While triacylglycerols accumulate and lipid droplets enlarge, other important morphological changes take place. The chloroplasts became smaller and the amount of lipids that are characteristic of the photosynthetic membranes decrease significantly. Photosynthetic yield decreases in the nitrogen depleted cells, but it is still sufficient to drive cell survival and growth. If photosynthesis is inhibited indeed, Nannochloropsis cells stop growing, indicating that they rely on photosynthetic solar energy conversion and not on stored carbohydrates or lipids as energy source.[23]
Nannochloropsis cultivated in normal growth condition and deprived of a nitrogen source continues growing for 4–5 days. The analysis of gene expression reveals that mechanisms for nitrogen assimilation and redistribution are activated in the cells in nitrogen scarcity and allow survival through a partial reorganisation of the cellular metabolism. The genes responsible for the incorporation of free ammonium into glutamate (L-glutamine + 2-oxoglutarate + NADPH + H+ ←→ 2 L-glutamate + NADP+) are up-regulated . Their up-regulation increases the capability of the cells to assimilate minimal amount of ammonium eventually present in the medium and, more importantly, allows them to assimilate the intracellular ammonium that can be released by degradative processes. Transcriptomic data of nitrogen-deprived Nannochloropsis cultures show that various enzymes responsible for degradative processes that release ammonium are indeed up regulated. Moreover, the expression of genes coding for proteins involved in controlled degradation of proteins increase, together with others involved in the formation of cytosolic sequestering vesicles used for degradation and recycling of cellular components.[14]
The machinery of gene expression of chloroplast and mitochondrion is down regulated in Nannochloropsis in response to nitrogen depletion.[14][15]
Corteggiani Carpinelli and coworkers (2013)[14] report a complete analysis of the gene expression of Nannochloropsis cultures grown in normal conditions and nitrogen deprivation for 3 days and 6 days. Data on similar conditions were also collected by Radakovits et al. (2012)[15] and Vieler et al. (2012).[16] The all of this data show that genes involved in fatty acid and triacylglycerol biosynthesis are always abundant in the cells and their expression is not correlated with the amount of oil accumulated. Also the expression of the genes involved in triacylglycerols degradation is not significantly down-regulated as triacylglycerols accumulate. The general conclusion suggested by the experimental data is that Nannochloropsis constitutively produces triacylglycerols and that the metabolic reorganisation that follows nitrogen deprivation increases the flux of substrates through this pathway, which is in turn capable to sustain the increased metabolic flux. Corteggiani Carpinelli and coworkers (2013)[14] advance the hypothesis that, in their experimental conditions, photosynthesis is the main energy source and the down-regulation of the metabolic activity of the mitochondrion is determinant in increasing the amount of substrates that enter the fatty acid biosynthetic pathway. If more precursors are available, more fatty acids are synthesised and as a consequence more triacylglycerols are produced and accumulated into the cells as oil droplets.
Dong et al. (2013)[24] report a quantification of the abundance of various proteins in cultures of Nannochloropsis grown with a supplement of CO2 and deprived of nitrogen. Despite the different experimental conditions, also the proteomic study seems to support the hypothesis that the accumulation of triacylglycerols is due to an increase of the metabolic flux through the fatty acid biosynthetic pathway. The authors advance the hypothesis that, in their experimental conditions, the degradation of storage sugars and the up-regulation of glycolysis are responsible for the increase of substrates through the pathway.
More recently Li and coworkers (2014)[25] collected extensive experimental data from cultures of Nannochloropsis oculata IMET1 grown in nitrogen sufficient and nitrogen depleted media. According to their analysis it is the catabolism of carbohydrates and proteins together with the up-regulation of genes assigned to various pathways (the cytosolic glycolysis pathway, which produces pyruvate; the PDHC bypass, which yields additional acetyl-CoA; and the coupling of TCA reactions with mitochondrial β-oxidation) that have to be claimed for increasing the supply of carbon precursors to the fatty acid biosynthetic pathway. Nevertheless, the authors suggest that it isn't the increased synthesis of fatty acids that leads to accumulation of oil inside the cells, but it is rather the up-regulation of genes involved in the assembly of triacylglycerols that determines the final oil concentration. In other words, under nitrogen depletion, it is the up-regulation of the transcript level of the key genes in triacylglycerol assembly, rather than those in fatty acids biosynthesis, that leads to accelerated triacylglycerol production.
In 2017, a study jointly funded by ExxonMobil and Synthetic Genomics achieved a breakthrough in lipid percentages in Nannochloropsis gaditana through applications of the CRISPR-Cas9 reverse-genetics pipeline and nitrogen starving—improving partitioning of total carbon to lipids from 20% (wild type) to 40-45% (mutant type).[26]
Nannochloropsis is a genus of algae comprising six known species. The genus in the current taxonomic classification was first termed by Hibberd (1981). The species have mostly been known from the marine environment but also occur in fresh and brackish water. All of the species are small, nonmotile spheres which do not express any distinct morphological features that can be distinguished by either light or electron microscopy. The characterisation is mostly done by rbcL gene and 18S rRNA sequence analysis.
The algae of the genus Nannochloropsis differ from other related microalgae in that they have chlorophyll a and completely lack chlorophyll b and chlorophyll c. In addition they are able to build up a high concentrations of a range of pigments such as astaxanthin, zeaxanthin and canthaxanthin. They have a diameter of about 2 to 3 micrometers and a very simple ultrastructure with reduced structural elements compared to neighbouring taxa.
Nannochloropsis is considered a promising alga for industrial applications because of its ability to accumulate high levels of polyunsaturated fatty acids. Moreover, it shows promising features that can allow genetic manipulation aimed at the genetic improvement of the current oleaginous strains. Various species of Nannochloropsis indeed are transfectable and there has been evidence that some strains are able to perform homologous recombination. At the moment it is mainly used as an energy-rich food source for fish larvae and rotifers. Nevertheless, it has raised growing interest also for the investigation of biofuel production from photosynthetic organisms. (see Nannochloropsis and biofuels). Nannochloropsis is actually in use as food additive for human nutrition and it is also served at Restaurant "A Poniente" of El Puerto de Santa María (Cádiz, Spain) close to the natural environment where Nannochloropsis gaditana was first isolated and still grows. A 2020 study suggests it could be used for a highly performant, sustainable fish-free feed for farmed fish.
Nannochloropsis è un genere di alghe che comprende 6 specie identificate fino a questo momento. L'attuale classificazione tassonomica si deve a Hibberd (1981) che è stato il primo a caratterizzare questo genere[1]. Le specie note sono prevalentemente caratteristiche di ambienti marini ed oceanici, tuttavia sono state osservate anche specie che vivono in acqua dolce[2]. Tutte le specie di Nannochloropsis sono cellule sferoidali piccole e prive di strutture motorie e non sono stati osservati tratti morfologici caratteristici che permettano di distinguere le varie specie fra loro utilizzando l'osservazione al microscopio. Le varie specie tuttavia possono essere chiaramente distinte fra loro se si analizza uno dei geni codificanti per l'RNA ribosomale, denominato 18S gDNA[3].
Nannochloropsis ha solo clorofilla a ed è assolutamente priva di clorofille b e c che sono invece comuni nelle microalghe evolutivamente vicine. Accumula grandi concentrazioni di vari pigmenti come astaxantina, zeaxantina e cantaxantina[4].
Queste alghe hanno una struttura morfologica cellulare molto semplice e presentano molte meno strutture interne delle alghe che gli sono evolutivamente più vicine. Hanno un diametro di circa 2 micrometri.
Vengono considerate alghe molto promettenti per diverse applicazioni industriali. La ragione principale è la loro facoltà di accumulare grandi quantità di acidi grassi polinsaturi al loro interno in diverse condizioni di crescita[5][6]. Una seconda ottima ragione è costituita dalla grande manipolabilità genetica di queste microalghe, che consentirebbe di migliorare in poco tempo la resa delle colture e la tipologia di molecole che si possono ottenere da queste colture algali. Le cellule di Nannochloropsis possono accettare DNA dall'esterno e alcuni ceppi sono anche in grado di integrarlo nel proprio genoma per ricombinazione omologa[7]. Al momento queste alghe sono largamente coltivate al livello industriale per produrre cibo altamente energetico per nutrire pesciolini e rotiferi. Tuttavia recentemente hanno attratto principalmente attenzione per gli studi legati alla produzione di biodiesel a partire da micro-organismi che crescono grazie alla sola luce del sole. Nannochloropsis è anche un ghiotto prodotto per l'alimentazione umana, è infatti utilizzata per produrre integratori alimentari ed è servita anche in alcuni ristoranti [8].
Questa alga in Italia è particolarmente abbondante nella laguna di Comacchio, dove la specie N. gaditana è addirittura infestante[9]
Le specie note e classificate al momento sono:
La comunità scientifica ha ottenuto i genomi di diversi ceppi di Nannochloropsis appartenenti a due specie: N. gaditana[10][11] e N. oceanica[12][13]. È disponibile in rete un portale basato sul genoma di N. gaditana B-31 che consente di accedere la gran parte delle informazioni genomiche disponibili riguardo a Nannochloropsis. Inoltre sono state pubblicate anche delle pagine dedicate ai genomi di N. gaditana CCMP526 e N. oceanica CCMP1779.
I genomi dei ceppi di Nannochloropsis sequenziati sono grandi circa 28.5-29 mega basi, sono caratterizzati da un'alta densità di geni, un ridotto contenuto di introni e sequenze intergeniche molto corte[10], inoltre ci sono relativamente poche sequenze ripetute[12]. I genomi delle due specie sequenziate sono molto simili fra loro.
L'analisi dei genomi ha messo in evidenza che queste alghe possiedono i geni che gli consentono di sintetizzare ed allocare nella parete cellulare cellulosa e fucani solfati e che sono in grado di conservare carbonio ed energia in polimeri di glucosio β-1,3- e β-1,6-chiamati crisolaminarine[10]. Un'analisi tramite spettroscopia NMR fatta su cellule intere di Nannochlorpsis cresciute in autotrofia [14] ha permesso di evidenziare la presenza di cellulosa nelle pareti cellulari e di crisolaminarine parzialmente mobili, probabilmente in soluzione nei vacuoli.
L'analisi comprata dei geni coinvolti nel metabolismo dei lipidi in N. gaditana e nelle alghe rosse/verdi/brune e diatomee ha fornito alcune indicazioni riguardo all'ingente accumulo di lipidi nelle colture di Nannochloropsis. L'analisi infatti ha rivelato che Nannochloropsis ha un set più numeroso di geni coinvolti nella sintesi dei trigliceridi rispetto alle altre alghe prese in considerazione[11]. In entrambe le specie di Nannochloropsis sequenziate è stato trovato un alto numero di lipasi, che contribuiscono al metabolismo dei trigliceridi attraverso la degradazione dei trigliceridi e il rimodellamento dei lipidi[12]. Molte di queste lipasi sembrano appartenere a una famiglia genica esclusiva di Nannochloropsis[15].
L'analisi dei dati genomici e trascrittomici suggerisce che sia in N. gaditana che in N. oceanica siano presenti RNA con funzione regolatoria ed in particolare miRNA[10][12].
In Nannochloropsis sono stati trovati inoltre gli diversi ortologhi di proteine che sono note come sensori della luce blu. Questo consente di ipotizzare che sia presente qualche forma di controllo circadiano in queste microalghe[10][12].
Quando vengono coltivate in condizioni di crescita normali con terreno di coltura f/2 standard con aggiunta di nitrato, le cellule di Nannochloropsis hanno un contenuto medio di olio al loro interno pari a circa il 30% del loro peso secco. Questo olio è utilizzabile per fare biodiesel. Perché il processo di produzione di biodiesel da Nannochloropsis sia efficiente, è necessario aumentare la resa di olio dalle colture. È stato osservato che diverse condizioni di coltura aumentano il contenuto medio di olio per cellula, ma rallentano al tempo stesso la crescita delle alghe rispetto alle condizioni normali di coltura, abbassando così la resa complessiva. Fra le varie condizioni che producono questo effetto, c'è la deprivazione di azoto dal terreno di coltura. Si tratta di una delle condizioni di crescita più studiate, per la quale sono stati riportati i parametri di crescita delle alghe in vari impianti e per la quale conosciamo anche la caratterizzazione fisiologica e molecolare delle alghe in coltura.
Vari ceppi di Nannochloropsis accumulano fino al 60% - 70% di lipidi rispetto alla massa totale quando crescono in assenza di azoto[6][16]. Inoltre non cambia solo la quantità totale di lipidi ma anche la loro composizione. È stato osservato che la quantità di trigliceridi prodotti dalla coltura aumenta vistosamente in risposta alla deprivazione di azoto, mentre la quantità di altri lipidi, essenzialmente glicerolipidi, acidi grassi liberi e diacilgliceroli, diminuisce lievemente. Poiché l'aumento di trigliceridi è più grande della diminuzione degli altri lipidi, si deduce che le cellule sono impegnate a sintetizzare ex novo i trigliceridi piuttosto che a trasformare i lipidi tutti gli altri in trigliceridi[17].
Mentre si accumulano i trigliceridi e diventano visibili all'interno delle cellule cospicue gocce di olio, avvengono anche altri importanti cambiamenti morfologici. I cloroplasti si rimpiccioliscono e la quantità di lipidi che sono caratteristici delle membrane plastidiali diminuisce in modo significativo. La resa dell'attività fotosintetica è più bassa nelle cellule che crescono senza azoto rispetto a quelle che crescono in condizioni sufficienti di nutriente, però è comunque sufficiente a tenere in vita le cellule e supportare la crescita della coltura. Un esperimento riportato da Simionato et al.[17] infatti dimostra che se la fotosintesi viene inibita le cellule smettono immediatamente di crescere. Pertanto la crescita delle colture in deprivazione di azoto è supportata dalla conversione della luce solare e non dalla degradazione di carboidrati o lipidi di riserva all'interno delle cellule.
Quando viene coltivata in condizioni normali di crescita e deprivata di azoto, Nannochloropsis continua a crescere per circa 4-5 giorni. L'analisi dell'espressione genica rivela che le cellule cresciute in deprivazione di azoto attivano un meccanismo di assimilazione e ridistribuzione dell'azoto intracellulare che gli consente di sopravvivere riorganizzando parzialmente il metabolismo. I geni responsabili per l'assimilazione dell'ammonio libero in molecole di glutammato (L-glutamine + 2-oxoglutarate + NADPH + H+ ←→ 2 L-glutamate + NADP+) sono sovra-espressi e aumentano la capacità delle cellule di assimilare quantità anche minime di ammonio eventualmente presenti nel mezzo, ma soprattutto consentono alle cellule di riciclare l'ammonio presente all'interno delle cellule stesse che viene rilasciato da processi degradativi. La trascrittomica mostra che nelle colture di Nannochloropsis in deprivazione di azoto, diverse vie degradative che portano al rilascio di azoto sono sovra-espresse al livello di mRNA. Inoltre i geni che codificano per proteine coinvolte nella degradazione regolata di altre proteine e nelle formazione di vescicole di autofagocitosi sono anche sovra-espressi[10].
Il macchinario per l'espressione genica del cloroplasto e del mitocondrio è notevolmente ridotto nelle cellule di Nannochloropsis cresciute in assenza di azoto[10][11].
Corteggiani Carpinelli e colleghi (2013)[10] riportano un'analisi completa dell'espressione genica di Nannochloropsis coltivata in condizioni normali di crescita e deprivata di azoto per 3 giorni e 6 giorni. Dati ottenuti crescendo Nannochloropsis in condizioni analoghe sono stati anche prodotti da Radakovits et al. (2012)[11] e da Viler et al. (2012)[12]. Tutti questi dati mostrano che i geni coinvolti nella biosintesi degli acidi grassi e dei trigliceridi sono sempre abbondanti nelle cellule di Nannochloropsis e che la loro espressione non è correlata con la quantità di lipidi accumulata nelle cellule. Inoltre non si registrano neanche cambiamenti significativi di espressione dei geni coinvolti nella degradazione dei trigliceridi. Questi dati sperimentali conducono alla conclusione generale che Nannochloropsis produce normalmente trigliceridi e che la riorganizzazione metabolica della cellula in risposta alla deprivazione di azoto aumenti il flusso di substrati che entrano nella via biosintetica dei trigliceridi, che a sua volta è in grado di trasformarli e di portare all'accumulo dei prodotti. Corteggiani Carpinelli e colleghi (2013)[10] avanzano l'ipotesi che, in queste condizioni sperimentali, la fotosintesi sia la principale fonte di energia della cellula e la riduzione dell'efficienza dell'attività mitocondriale sia determinante per l'accumulo dei substrati che entrano nella via biosintetica degli acidi grassi. L'aumento degli acidi grassi conduce poi all'aumento dei trigliceridi ed al loro accumulo in vescicole oleose all'interno delle cellule.
Dong et al. (2013)[18] riferiscono di un esperimento in cui quantificano l'abbondanza di varie proteine in colture di Nannochloropsis aerate con un supplemento di CO2 e deprivate di azoto. Nonostante le condizioni sperimentali siano diverse da quelle utilizzate per gli esprimenti di trascrittomica, i dati di proteomica ottenuti in questo modo sembrano confermare l'ipotesi che l'aumento del flusso metabolico attraverso la via di biosintesi degli acidi grassi sia la principale causa dell'accumulo di olio all'interno delle cellule. Gli autori avanzano l'ipotesi che, nelle loro condizioni sperimentali, la degradazione degli zuccheri di riserva e la sovra-espressione delle proteine coinvolte nella glicolisi siano responsabili per l'accumulo di substrati che entrano nella via di biosintesi degli acidi grassi.
Recentemente Li e colleghi (2014) [19] hanno ottenuto dati sperimentali molto approfonditi da colture di "Nannochloropsis oculata" IMET1 cresciuta in presenza ed assenza di azoto. Secondo le loro analisi il catabolismo dei carboidrati e delle proteine, insieme all'aumento dell'espressione di varie vie metaboliche (la glicolisi citosolica che produce piruvato; la sintesi di acetil-CoA nel cloroplasto; e l'accoppiamento nel mitocondrio del ciclo di Krebs con la b-ossidazione) sono da ritenersi responsabili per l'aumento del flusso di substrati che alimentano la biosintesi degli acidi grassi. Tuttavia, secondo gli autori, non sarebbe l'aumento degli acidi grassi prodotti a determinare l'accumulo di olio dentro le cellule, bensì l'aumento dei trigliceridi prodotti a partire da quegli acidi grassi. In altre parole sarebbe la regolazione dei geni coinvolti nella sintesi dei trigliceridi ad essere principalmente responsabile della più veloce sintesi dei trigliceridi stessi e quindi dell'accumulo di questi in vescicole oleose all'interno delle cellule.
Nannochloropsis è un genere di alghe che comprende 6 specie identificate fino a questo momento. L'attuale classificazione tassonomica si deve a Hibberd (1981) che è stato il primo a caratterizzare questo genere. Le specie note sono prevalentemente caratteristiche di ambienti marini ed oceanici, tuttavia sono state osservate anche specie che vivono in acqua dolce. Tutte le specie di Nannochloropsis sono cellule sferoidali piccole e prive di strutture motorie e non sono stati osservati tratti morfologici caratteristici che permettano di distinguere le varie specie fra loro utilizzando l'osservazione al microscopio. Le varie specie tuttavia possono essere chiaramente distinte fra loro se si analizza uno dei geni codificanti per l'RNA ribosomale, denominato 18S gDNA.
Nannochloropsis ha solo clorofilla a ed è assolutamente priva di clorofille b e c che sono invece comuni nelle microalghe evolutivamente vicine. Accumula grandi concentrazioni di vari pigmenti come astaxantina, zeaxantina e cantaxantina.
Queste alghe hanno una struttura morfologica cellulare molto semplice e presentano molte meno strutture interne delle alghe che gli sono evolutivamente più vicine. Hanno un diametro di circa 2 micrometri.
Vengono considerate alghe molto promettenti per diverse applicazioni industriali. La ragione principale è la loro facoltà di accumulare grandi quantità di acidi grassi polinsaturi al loro interno in diverse condizioni di crescita. Una seconda ottima ragione è costituita dalla grande manipolabilità genetica di queste microalghe, che consentirebbe di migliorare in poco tempo la resa delle colture e la tipologia di molecole che si possono ottenere da queste colture algali. Le cellule di Nannochloropsis possono accettare DNA dall'esterno e alcuni ceppi sono anche in grado di integrarlo nel proprio genoma per ricombinazione omologa. Al momento queste alghe sono largamente coltivate al livello industriale per produrre cibo altamente energetico per nutrire pesciolini e rotiferi. Tuttavia recentemente hanno attratto principalmente attenzione per gli studi legati alla produzione di biodiesel a partire da micro-organismi che crescono grazie alla sola luce del sole. Nannochloropsis è anche un ghiotto prodotto per l'alimentazione umana, è infatti utilizzata per produrre integratori alimentari ed è servita anche in alcuni ristoranti .
Questa alga in Italia è particolarmente abbondante nella laguna di Comacchio, dove la specie N. gaditana è addirittura infestante