mk
имиња во трошки

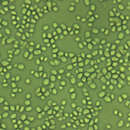
Candida glabrata ye una especie de lleldu haploide, enantes conocíu como Torulopsis glabrata. Esta especie de lleldu nun ye dimórficu y nun s'observó actividá d'apareamientu. Hasta hai poco, camentábase que C. glabrata yera un organismu non patoxénicu. De toes formes, cola población creciente d'individuos inmunodeficientes, vióse que C. glabrata presenta tendencia a ser un patóxenu oportunista del tractu uroxenital y del torrente sanguineu.
Candida glabrata és una espècie de llevat haploide, abans coneguda com a Torulopsis glabrata. Aquesta espècie de llevat no és dimòrfica i no s'ha observat activitat d'aparellament. Fins fa poc, es pensava que C. glabrata era un organisme no patogènic. De totes maneres, amb la població creixent d'individus immunodeficients, s'ha vist que C. glabrata presenta tendència a ser un patogen oportunista del tracte urogenital i del torrent sanguini.
Candida glabrata ist eine haploide Hefe der Gattung Candida, früher bekannt als Torulopsis glabrata.
Auf Glucose-Pepton-Agar bilden sie kremfarbene, glatte, glanzlose Kolonien, die gewölbt sind und längere hefeartige Zellen bilden, ein Pseudomycelium. Die Zellen sind eiförmig, wachsen einzeln oder knospen und sind 2 bis 4 µm × 3 bis 5,5 µm groß. Auf Maismehlagar wird kein Pseudomycel gebildet. Der Keimfadentest ist negativ. Harnstoff kann nicht abgebaut werden. Der GC-Gehalt beträgt 39,6 bis 40,2 mol%.[1]
Bis vor kurzem galt C. glabrata als ein primär nicht pathogener Organismus. Mit der ständig wachsenden Zahl immunsupprimierter Personen zeigte sich, dass C. glabrata ein hoch opportunistischer Erreger des Urogenitaltrakts und der Blutbahn ist (Fungämie). Er kommt ubiquitär vor und ist ein Kontaminationskeim von Obstsäften. Bei Kühen kann er eine Mastitis hervorrufen[2]. C. glabrata ist eine häufige Ursache für einen Soor bei AIDS- und Krebspatienten unter Strahlentherapie und/oder Polychemotherapie. Hieraus ist auch die Entstehung invasiver Kandidosen und einer Sepsis möglich.[3]
Ein vielzitierter potenzieller Virulenzfaktor der Pathogenität von C. glabrata ist eine Reihe von Adhäsinen, die von den EPA-Genen codiert (Epithelzellen-Adhäsin)[4] werden. Diese Gene befinden sich in der subtelomerischen Region und können auf Signale der Umgebung reagieren, die es ihnen erlauben, massenhaft exprimiert zu werden, sodass der Organismus auf biotischen und abiotischen Oberflächen in mikrobiellen Matten haften kann.
Dies ist auch der vermutete Mechanismus, durch den C. glabrata mikrobielle „Biofilme“ auf Harnkathetern bildet. Es verursacht auch Probleme mit zahnmedizinischen Geräten, wie z. B. Prothesen. Tortulosis oder Candida glabrata kann in der „Seltene Krankheiten“-Datenbank auf der NIH-Website[5] und auch auf der CDC-Website[6] gefunden werden.
Zu Klärung der Infektion bieten sich mehrere Methoden an[7]:
Eine mikroskopische Hautdiagnose aus Kulturen von Abstrichen und Biopsien kann schnell zu falschen Ergebnissen führen und erfordert eine spezielle Bewertung.
Ein häufiger Phänotyp und möglicher Virulenzfaktor von C. glabrata ist eine intrinsische Resistenz[11] gegen Azole, d. h. die am meisten verschriebenen Antimykotika-Medikamente. Diese Stoffe, inklusive Fluconazol und Ketoconazol, sind in 15–20 % der Fälle nicht wirksam gegen C. glabrata. Mit Miconazol treten diese Probleme derzeit nicht auf.[12] Während man früher annahm, dass dieser Organismus eine „angeborene“ Immunität gegen die Arzneistoffe besitzt, ist es richtiger, dass er einen weiterentwickelten Widerstand gegen die Medikamente besitzt. C. glabrata ist empfindlich auf polyene Medikamente wie Amphotericin B und Nystatin, zusammen mit variabler Empfindlichkeit für 5-Fluorcytosin und Caspofungin. Die systemische Gabe von Amphotericin B ist wegen des beträchtlichen Nebenwirkungsspektrums ein letztes Mittel, da es oft den geschwächten Patienten töten kann.
Blutinfektionen können am besten über Symptome beurteilt werden, wenn weitere Körperbereiche beteiligt sind.
Eine experimentelle, aber effektive Second-Line-Behandlung für chronische Infektionen ist der Einsatz von Borsäure-Vaginalzäpfchen. Vitamin-E-Öl kann in Verbindung verwendet werden, um Reizungen zu bekämpfen. Amphotericin-B-Vaginalzäpfchen wurden in Fallstudien zur Behandlung von chronischen Infektionen verwendet. Borax und Borsäure können für persistente Kopfhaut und Hautinfektionen eingesetzt werden.
Eine Impfung unter Berücksichtigung der Pilzgifte wie bei Tetanus-Bakterien existiert bisher nicht.
Die genetische Information von C. glabrata liegt im Zellkern in 13 Chromosomen sowie im Kern der Mitochondrien vor. Das Genom des Stamms CBS138 wurde im Jahr 2004 erstmals vollständig analysiert. Es besteht aus 12,3 Millionen Basenpaaren und geschätzten 5.200–5.300 Genen.[13][14][15] 2009 wurde das Genom von C. parapsilosis in 'Nature 459' bebildert offengelegt.[16]
Das KEX2-Gen von C. glabrata ist für die Integrität der Zelloberfläche erforderlich.[17] Die Krankheitsrelevanz von Teilen der mitochondrialen DNA(COB) wurde erforscht.
Candida glabrata ist eine haploide Hefe der Gattung Candida, früher bekannt als Torulopsis glabrata.
Candida glabrata is a species of haploid yeast of the genus Candida, previously known as Torulopsis glabrata. Despite the fact that no sexual life cycle has been documented for this species, C. glabrata strains of both mating types are commonly found.[1] C. glabrata is generally a commensal of human mucosal tissues, but in today's era of wider human immunodeficiency from various causes (for example, therapeutic immunomodulation, longer survival with various comorbidities such as diabetes, and HIV infection), C. glabrata is often the second or third most common cause of candidiasis as an opportunistic pathogen.[2] Infections caused by C. glabrata can affect the urogenital tract or even cause systemic infections by entrance of the fungal cells in the bloodstream (Candidemia), especially prevalent in immunocompromised patients.[2]
Candida glabrata is of special relevance in nosocomial infections due to its innately high resistance to antifungal agents, specifically the azoles.[2] Besides its innate tolerance to antifungal drugs, other potential virulence factors contribute to C. glabrata pathogenicity. One of them is the expression of a series of adhesins genes.[3] These genes, which in C. glabrata are mostly encoded in the subtelomeric region of the chromosome, have their expression highly activated by environmental cues, so that the organism can adhere to biotic and abiotic surfaces in microbial mats. Adhesin expression is the suspected first mechanism by which C. glabrata forms fungal biofilms, proved to be more resistant to antifungals than the planktonic cells.[4]
Candida glabrata genome frequently undergoes rearrangements that are hypothesized to contribute to the improvement of this yeast's fitness towards exposure to stressful conditions, and some authors consider that this property is connected to the virulence potential of this yeast.[5]
Cultures are an effective method for identifying non-albicans vaginal infections. Urinalyses are less accurate in this process. The culture may take several days to grow, but the identification of the yeast species is quick once the yeast is isolated. Skin disease diagnosis is difficult, as cultures collected from swabs and biopsies will test negative for fungus and a special assessment is required. Listed under the 'Rare Diseases' database on the NIH web site, Torulopsis glabrata, or Candida glabrata can also be found on the CDC's web site.[6] Although listed as the second most virulent yeast after Candida albicans, the fungus is becoming more and more resistant to common treatments like fluconazole. Like many Candida species, C. glabrata resistance to Echinocandin is also increasing, leaving expensive and toxic antifungal treatments available for those infected.[6] Although high mortality rates are listed, assessment of the critical nature of a glabrata infection is a gray area.
Candida glabrata ferments and assimilates only glucose and trehalose, opposing to other Candida species and this repertoire of sugar utilization is used by several commercially available kits for identification.[7]
A major phenotype and potential virulence factor that C. glabrata possesses is low-level intrinsic resistance to the azole medications, which are the most commonly prescribed antifungal (antimycotic) medications. These medications, including fluconazole and ketoconazole, are "not effective in 15–20% of cases"[2] against C. glabrata. It is still highly vulnerable to polyene medications such as amphotericin B and nystatin, along with variable vulnerability to flucytosine and caspofungin. However, intravenous amphotericin B is a medication of last resort, causing among other side effects, chronic kidney failure. Amphotericin B vaginal suppositories are used as an effective form of treatment in combination with boric acid capsules as they are not absorbed into the bloodstream.
A first-line treatment for vaginal infections may be the use of terconazole 7-day cream. Several courses may be needed. The cure-rate for this treatment is approximately 40%. Recurrences are common, causing chronic infections and spread to other areas such as skin and scalp. Blood infections might be best assessed per symptoms if other areas are involved.
An experimental, but effective second-line treatment for chronic infections, is the use of boric acid. Compounding pharmacies can create boric acid vaginal suppositories. Use of Vitamin E oil may be used in conjunction to combat irritation. Amphotericin B vaginal suppositories have also been used in case studies to treat chronic infections, both symptomatic and asymptomatic. Borax and boric acid may be used for persistent scalp and skin infections.
The currently assigned genus name of Candida can lead to confusion. Compared with other potential pathogens of the genus (such as C. albicans or C. auris), C. glabrata is more closely related to Saccharomyces cerevisiae. In fact, C. glabrata belongs to the group of Nakaseomyces inside the whole genome duplication clade within Saccharomycetaceae.[8] The whole genome duplication event occurred about 90 million years ago, whereas phylogenetic studies indicate that the common ancestor between C. glabrata and C. albicans is dated between 200 and 300 million years ago. The largest phylogenetic study to date about Saccharomycotina, also known as budding yeasts, indicated in 2018 that the (currently construed) genus Candida is found in Pichiaceae, CUG-Ser1 clade, Phaffomycetaceae and Saccharomycetaceae. Consequently, despite that the name Candida evokes a unitary notion of candidiasis, the pathogenic power of some budding yeasts is a paraphyletic trait shared by several subphyla with different kinds of metabolism.[9]
Candida glabrata is a species of haploid yeast of the genus Candida, previously known as Torulopsis glabrata. Despite the fact that no sexual life cycle has been documented for this species, C. glabrata strains of both mating types are commonly found. C. glabrata is generally a commensal of human mucosal tissues, but in today's era of wider human immunodeficiency from various causes (for example, therapeutic immunomodulation, longer survival with various comorbidities such as diabetes, and HIV infection), C. glabrata is often the second or third most common cause of candidiasis as an opportunistic pathogen. Infections caused by C. glabrata can affect the urogenital tract or even cause systemic infections by entrance of the fungal cells in the bloodstream (Candidemia), especially prevalent in immunocompromised patients.
Candida glabrata es una especie de levadura haploide, antes conocida como Torulopsis glabrata. Esta especie de levadura no es dimórfica y no se ha observado actividad de apareamiento. Hasta hace poco, se pensaba que C. glabrata era un organismo no patogénico. De todos modos, con la población creciente de individuos inmunodeficientes, se ha visto que C. glabrata presenta tendencia a ser un patógeno oportunista del tracto urogenital y del torrente sanguíneo.
Candida glabrata es una especie de levadura haploide, antes conocida como Torulopsis glabrata. Esta especie de levadura no es dimórfica y no se ha observado actividad de apareamiento. Hasta hace poco, se pensaba que C. glabrata era un organismo no patogénico. De todos modos, con la población creciente de individuos inmunodeficientes, se ha visto que C. glabrata presenta tendencia a ser un patógeno oportunista del tracto urogenital y del torrente sanguíneo.
Candida glabrata est une espèce de levures, haploïde du genre Candida, connue auparavant sous le nom de Torulopsis glabrata. Cette espèce de champignon ne présente pas de dimorphisme et aucune activité de mating n'a été encore observée. C. glabrata n'était pas considéré comme pathogène. Toutefois, avec l'augmentation du nombre de patients immuno-déprimés (HIV positifs, transplantés, patients soumis à une chimiothérapie…), il s'est avéré que C. glabrata est un pathogène opportuniste du tractus urogénital. De plus, lorsque C. glabrata s'infiltre dans le flux sanguin, il peut y avoir le développement d'une candidémie.
Deux facteurs de virulence ont été décrits chez C. glabrata :
Candida glabrata est une espèce de levures, haploïde du genre Candida, connue auparavant sous le nom de Torulopsis glabrata. Cette espèce de champignon ne présente pas de dimorphisme et aucune activité de mating n'a été encore observée. C. glabrata n'était pas considéré comme pathogène. Toutefois, avec l'augmentation du nombre de patients immuno-déprimés (HIV positifs, transplantés, patients soumis à une chimiothérapie…), il s'est avéré que C. glabrata est un pathogène opportuniste du tractus urogénital. De plus, lorsque C. glabrata s'infiltre dans le flux sanguin, il peut y avoir le développement d'une candidémie.
Deux facteurs de virulence ont été décrits chez C. glabrata :
le premier de ces facteurs est la famille d'adhésines codées par les gènes EPA (de l'anglais : epithelial adhesin). Ces gènes sont localisés dans la région des télomères et peuvent répondre massivement à une stimulation extérieures, de manière que le champignon puisse adhérer aux surfaces biotiques ou abiotiques,. On suppose que ce mécanisme est impliqué dans la formation de biofilms sur les cathéters et sur les prothèses dentaires ; le deuxième facteur de virulence rencontré chez C. glabrata est la mise en place de mécanismes de résistance aux azoles,, qui sont les antifongiques (antimycosiques) les plus souvent utilisés lors des thérapies. Des azoles tels que le fluconazole ou le kétoconazole sont inefficaces dans 15 à 20 % des cas contre C. glabrata. Par contre, C. glabrata reste très sensible à l'action des polyènes (Amphotéricine B, nystatine) et des drogues comme la 5-fluorocytosine et la caspofongine présentent une efficacité variable.Candida glabrata é uma espécie de fungo haplóide do género Candida. Trata-se, juntamente com a Candida auris, de uma espécie de levedura que não forma filamentos e portanto no teste PCB dá resultados negativos tanto para os clamidósporos (esporos de resistência) como para os filamentos. Inicialmente, era considerada não-patogénica ao ser humano, no entanto, com o aumento do número de pessoas imunodeficientes, verificou-se que a Candida glabrata é um fungo agressivo, extremamente oportunista e resistente que ataca principalmente os indivíduos debilitados (p.e. portadores de HIV, doentes oncológicos)[1][2]. A Candida glabrata tem demostrado uma grande e rápida capacidade de desenvolver tolerâncias e resistências a fármacos antifúngicos, principalmente azóis e equinocandinas (p.e. fluconazole, clotrimazole, caspofungina, micafungina). Um dos mecanismos mais comuns deste fenómeno é a sobreexpressão de vários genes de resistência [3]
Candida glabrata é uma espécie de fungo haplóide do género Candida. Trata-se, juntamente com a Candida auris, de uma espécie de levedura que não forma filamentos e portanto no teste PCB dá resultados negativos tanto para os clamidósporos (esporos de resistência) como para os filamentos. Inicialmente, era considerada não-patogénica ao ser humano, no entanto, com o aumento do número de pessoas imunodeficientes, verificou-se que a Candida glabrata é um fungo agressivo, extremamente oportunista e resistente que ataca principalmente os indivíduos debilitados (p.e. portadores de HIV, doentes oncológicos). A Candida glabrata tem demostrado uma grande e rápida capacidade de desenvolver tolerâncias e resistências a fármacos antifúngicos, principalmente azóis e equinocandinas (p.e. fluconazole, clotrimazole, caspofungina, micafungina). Um dos mecanismos mais comuns deste fenómeno é a sobreexpressão de vários genes de resistência
Candida glabrata je grzib[3], co go nojprzōd ôpisoł H.W. Anderson, a terŏźnõ nazwã doł mu S.A. Mey. & Yarrow 1978. Candida glabrata nŏleży do zorty Candida, rzyndu Saccharomycetales, klasy Saccharomycetes, grōmady Ascomycota i krōlestwa grzibōw.[4][5] Żŏdne podgatōnki niy sōm wymianowane we Catalogue of Life.[4]
Candida glabrata je grzib, co go nojprzōd ôpisoł H.W. Anderson, a terŏźnõ nazwã doł mu S.A. Mey. & Yarrow 1978. Candida glabrata nŏleży do zorty Candida, rzyndu Saccharomycetales, klasy Saccharomycetes, grōmady Ascomycota i krōlestwa grzibōw. Żŏdne podgatōnki niy sōm wymianowane we Catalogue of Life.