mk
имиња во трошки

Ledvinovec psí (Dioctophyme renale) je parazitická hlístice napadající ledviny a vůbec vylučovací soustavu savců. Obvyklými konečnými hostiteli jsou psi a norci, kteří se nakazí při konzumaci ryb. Jím způsobované onemocnění u savců je nazýváno dioktofymóza. Výskyt dioktofymózy u člověka je extrémně vzácný, ovšem bez léčení vede k destrukci ledviny. Léčba se provádí chirurgicky.
Ledvinovec psí se vyskytuje téměř celosvětově, jednou z výjimek je střední Evropa. Nelze však zcela vyloučit, že si pes přiveze nákazu z cest či že se sem dostane nakažené rybí maso. V listopadu 2014 se v České republice objevilo podezření na první případ dioktofymózy u člověka ve Střední Evropě.[1]
Ledvinovec psí (Dioctophyme renale) je parazitická hlístice napadající ledviny a vůbec vylučovací soustavu savců. Obvyklými konečnými hostiteli jsou psi a norci, kteří se nakazí při konzumaci ryb. Jím způsobované onemocnění u savců je nazýváno dioktofymóza. Výskyt dioktofymózy u člověka je extrémně vzácný, ovšem bez léčení vede k destrukci ledviny. Léčba se provádí chirurgicky.
Ledvinovec psí se vyskytuje téměř celosvětově, jednou z výjimek je střední Evropa. Nelze však zcela vyloučit, že si pes přiveze nákazu z cest či že se sem dostane nakažené rybí maso. V listopadu 2014 se v České republice objevilo podezření na první případ dioktofymózy u člověka ve Střední Evropě.
Der Nierenwurm oder Riesennierenwurm (Dioctophyme renale, Syn.: Dioctophyma renale) ist ein parasitischer Fadenwurm, dessen adulte Form die Nieren und gelegentlich auch die Bauchhöhle von Säugetieren befällt.
Es handelt sich um einen der größten bekannten parasitischen Nematoden bei Säugetieren: Weibliche Tiere können bei einem Durchmesser von 10 bis 12 mm Längen von über einem Meter erreichen. Der Parasit befällt vor allem Raubtiere wie Hunde und Marderartige, ein Befall des Menschen ist heute selten. Ein Nierenwurmbefall führt normalerweise zur Zerstörung einer oder beider Nieren des Wirts.
Die Erstbeschreibung des Nierenwurms erfolgte im Jahr 1782 durch Johann August Ephraim Goeze, der den Wurm in der Niere eines Hundes entdeckte. Die Art gehört zur Familie Dioctophymidae und der Gattung Dioctophyme, wobei lange auch die Schreibung Dioctophyma verwendet wurde. 1987 legte die International Commission on Zoological Nomenclature den Gattungsnamen Dioctophyme als verbindlich fest.[1]
Der Nierenwurm ist weltweit verbreitet, kommt aber in Afrika und Ozeanien seltener vor als in der übrigen Welt.[2] Seine hauptsächlichen Endwirte sind fischfressende Säugetiere, darunter Nerze und Haushunde.
Der Parasit ist vor allem in der gemäßigten Klimazone verbreitet. Nerze sind die häufigsten Endwirte, wobei der Befall lokal häufiger auftreten kann, insbesondere in Teilen der kanadischen Provinz Ontario[1] und im US-Bundesstaat Minnesota.[3] In diesen Regionen können bis zu 50 % der Elritzen Träger des Parasiten sein.[2] Ein Befall des Menschen ist sehr selten; am häufigsten kommt der Nierenwurm beim Menschen rund um das Kaspische Meer vor, wobei die höchste Prävalenz im Iran erreicht wird.[4]
2003 wurden in sechs menschlichen Koprolithen aus der jungsteinzeitlichen Pfahlbausiedlung Arbon-Bleiche 3 im Kanton Thurgau in der Schweiz Eier des Nierenwurms nachgewiesen. Die Funde wurden auf 3384–3370 v. Chr. datiert. Dies legt den Schluss nahe, dass Nierenwurmbefall durch den Verzehr von Fischen in diesem Zeitraum wahrscheinlich häufiger vorkam, da vermutlich unzureichende Gartechniken verwendet wurden.[5]
Der Nierenwurm besitzt einen ausgeprägten Geschlechtsdimorphismus. Adulte männliche Tiere erreichen bei einem Durchmesser von 5–6 mm eine Länge von 20–40 cm, wohingegen adulte weibliche Tiere bei einem Durchmesser von 10–12 mm eine Länge von bis zu 103 cm erreichen können. Beide Geschlechter sind hellrot und an beiden Enden spitz zulaufend. Männliche Würmer besitzen an ihrem Hinterende eine Bursa, mittels derer sie sich bei der Paarung an die weiblichen Würmer anheften können.
Die Eier des Nierenwurms sind oval, zum Zeitpunkt der Ausscheidung nicht embryoniert, von gelbbrauner Färbung und haben eine Länge von 60–80 μm bei einem Durchmesser von 39–47 μm. Sie weisen eine charakteristische dicke Hülle auf. Ihre Oberfläche ist abgesehen von den Enden rau.
Adulte Nierenwürmer befallen typischerweise die rechte Niere des Endwirts,[6][7] wo sie sich paaren. Die weiblichen Tiere legen danach Eier, die mit dem Urin ausgeschieden werden. Im Wasser embryonieren diese Eier nach 15 bis 100 Tagen.[2] Die Eier werden von im Wasser lebenden Wenigborstern aufgenommen (darunter auch der Regenwurm), die als Zwischenwirte fungieren. Im Zwischenwirt schlüpfen die Wurmlarven und häuten sich bis zur Larve 3. Die Larven können sich danach in verschiedenen Sammelwirten anreichern, die sich von solchen Wenigborstern ernähren, wobei vor allem Fische und Amphibien eine Rolle spielen.[8]
Nimmt nun ein Säugetier einen infizierten Zwischen- oder Sammelwirt auf, so dringen die Larven in die Darmwand ein und wandern in die Leber, wo sie für ungefähr 50 Tage verbleiben. Danach wandern sie in die Nieren (typischerweise in die rechte Niere), wo sie ins Nierenbecken eindringen und sich dort paaren. Nierenwürmer können innerhalb der Niere bis zu fünf Jahre lang überleben und zerstören das Organ dabei. Gelegentlich können sie die Niere dabei auch perforieren und in die Bauchhöhle wandern.[1]
Hauptsächlicher Endwirt des Nierenwurms ist der Nerz.[9] Daneben können auch weitere Raubtiere wie Wölfe, Kojoten, Füchse,[10] Hunde,[11] Wiesel, Waschbären und Bären als Endwirte fungieren.[7] Der Nierenwurm kann auch Menschen befallen, wobei die Infektion meistens durch Verzehr nicht genügend gekochter Süßwasserfische oder Frösche erfolgt.[12]
Als Erregerreservoir spielt in der Praxis vor allem der Nerz eine Rolle, aber jeder mögliche Endwirt kann die Eier mit dem Urin ausscheiden und so zur Infektionsquelle werden.[3]
Ein Befall mit dem Nierenwurm führt zu wenig spezifischen Symptomen, darunter typischerweise Hämaturie und Schmerzen in der Lendengegend; zusätzlich kann es durch das Eindringen des Wurms in den Harnleiter zu Nierenkoliken kommen. In den meisten Fällen ist nur eine Niere befallen, die durch fibrotische Veränderungen zerstört wird. Ein beidseitiger Befall kann zum Tod durch Nierenversagen führen.[2]
Im Blutbild kann oft Eosinophilie nachgewiesen werden. Befinden sich Würmer beiderlei Geschlechts in derselben Niere, so kommt es zur Ausscheidung von Eiern im Urin, deren Nachweis diagnostisch ist. Oft wird die Diagnose aber auch zufällig anlässlich einer Ultraschalluntersuchung oder einer Computertomographie gestellt.[13]
Beim Menschen existiert keine standardisierte Behandlung des Nierenwurmbefalls. Meist werden die Würmer chirurgisch entfernt, je nach deren Zustand auch die befallene Niere (Nephrektomie). Diese Behandlung ist auch in der Veterinärmedizin üblich. Zudem existiert eine Fallbeschreibung einer erfolgreichen medikamentösen Behandlung mit Ivermectin bei einem Menschen mit Nierenwurmbefall.[4]
Der Nierenwurm oder Riesennierenwurm (Dioctophyme renale, Syn.: Dioctophyma renale) ist ein parasitischer Fadenwurm, dessen adulte Form die Nieren und gelegentlich auch die Bauchhöhle von Säugetieren befällt.
Es handelt sich um einen der größten bekannten parasitischen Nematoden bei Säugetieren: Weibliche Tiere können bei einem Durchmesser von 10 bis 12 mm Längen von über einem Meter erreichen. Der Parasit befällt vor allem Raubtiere wie Hunde und Marderartige, ein Befall des Menschen ist heute selten. Ein Nierenwurmbefall führt normalerweise zur Zerstörung einer oder beider Nieren des Wirts.
Dioctophyme renale, commonly referred to as the giant kidney worm,[1][2][3] is a parasitic nematode (roundworm) whose mature form is found in the kidneys of mammals. D. renale is distributed worldwide, but is less common in Africa and Oceania.[4] It affects fish eating mammals, particularly mink [1] and dogs.[4] Human infestation is rare, but results in kidney destruction, usually of one kidney and hence not fatal. A 2019 review listed a total of 37 known human cases of dioctophymiasis in 10 countries with the highest number (22) in China. Upon diagnosis through tissue sampling, the only treatment is surgical excision.[5]
Dioctophymosis,[4] dioctophymiasis, giant kidney worm, kidney worm infection,[6] Dioctophyme renale infection[7][8]
Dioctophyme renale was discovered in 1583. Almost two centuries later, in 1782, Johann Goeze first described D. renale upon discovering the worms in a dog kidney. The family Dioctophymidae has only one genus (Dioctophyme), and the name of the genus was in contention (with the possibility of being Dioctophyma) for two hundred years. The issue was finally resolved by the International Commission on Zoological Nomenclature[1] in 1989.
In 2003, D. renale eggs were discovered in six human coprolites in the neolithic site Arbon-Bleiche 3, Switzerland. This location is near a lake, which likely provided early humans with access to freshwater fish and frogs. The samples were dated from 3384 to 3370 BC, and is evidence that the prevalence of this infection was higher in early human history (before full understanding of proper cooking techniques).[9] Eggs were also found in 2019 in a well-preserved largely fish-eating settlement in England dating to 900 BC.[10]'[]
Individuals with Dioctophyme renale infection (known as dioctophymosis) typically present with unspecific symptoms including hematuria[4][7] (blood in urine), nephritis, loin pain,[3] renal enlargement, and/or renal colic[4] (intermittent pain in the kidney area), which may result from the rare migration of worms through ureters.[1][3][4][7] In some cases the fibrosis occurring after parasite infection is an incidental finding in ultrasound or CT scan, mimicking renal cancer, leading to radical nephrectomy.[11]
Adult worms typically only infect one kidney. The kidney is destroyed because of fibrosis, the development of excess fibrous connective tissue. Global renal dysfunction is typically limited because the non-infected kidney is usually capable of assuming the increased work. However, parenchymal inflammation can lead to death in extreme circumstances.
Adult Dioctophyme renale inhabit the kidney (typically the right kidney).[2][6] Females produce eggs which are passed in urine. In aquatic environments, eggs embryonate after 15–100 days.[4] These eggs are ingested by an aquatic oligochaete, hatch, penetrate blood vessels, and develop into a stage three larvae. A paratenic host[12] may then ingest the oligochaete. The oligochaete or paratenic host is then eaten by a definitive host, wherein juveniles penetrate intestinal lining and migrate to the liver. After maturing for approximately 50 days, the juveniles then migrate to the kidneys (typically the right kidney). Upon maturation, D. renale can survive for five years.[1][8][13]
Definitive hosts are carnivorous mammals, notably mink,[14] but also includes wolves, coyotes, foxes,[15] dogs,[16] raccoons, and weasels.[6]
Transmission to humans typically occurs upon ingestion of raw or undercooked freshwater fish or frog.[3][7]
There are multiple reservoirs for D. renale. Confirmed cases of infection have occurred in minks,[17][18] dogs,[16] swine, bears, oxen, and humans.[3][4][6]
D. renale is the largest nematode to parasitize humans. Adult male worms are 20–40 cm long and 5–6 mm wide; females can grow to 103 cm in length with a width of 10–12 mm.[3] Both sexes appear bright red in color and taper at both the anterior and posterior ends. Male D. renale worms have a bursa, which is used to attach to facilitate mating.
Eggs are 60–80 micrometres x 39–47 micrometres, contain an embryo, and have characteristic sculpturing of the shell.[3] They have an oval-shape and brownish-yellow hue. Eggs have a thick shell, and the surface appears to be pitted except at the poles.
The only means of obtaining a definitive diagnosis is through the identification of D. renale eggs in a patient's urine. However, obtaining patient history (i.e., if the patient has consumed undercooked or raw freshwater fish) is an important first step that can be coupled with radiological exams[4] to search for enlarged or calcified kidneys. Urinalysis will likely show hematuria blood tests may reveal eosinophilia.
Likely because of the rarity of human cases, there is no standard treatment[6] for D. renale infection in humans. The only known means is surgical excision of either adult worms[8] or the infected kidney.[7] Nephrectomy is generally considered extreme for human cases.[19]
A physician reportedly used Ivermectin to treat a patient, who was effectively cured.[19] The use of anti-helminth drugs has not yet been evaluated as the proper course of action to treat this infection.
Though D. renale is distributed worldwide, though markedly less frequent in Africa and Oceania, human infection is extremely rare. Regions around the Caspian Sea have the highest number of cases, with the most occurring in Iran.[19] Infections are also most commonly found in areas where freshwater fish is a dietary mainstay.
Non-human infections are more common worldwide, especially in areas of temperate climate. Prevalence in mink populations may be high, such as portions of Ontario[1] or Minnesota.[17] Similarly, some minnow populations may be as high as 50%.[4]
No public health measures have been undertaken or vaccines developed because of the rarity[13] of human infection. The majority of D. renale infections have resulted from undercooked or raw freshwater fish consumption. Thus, the simple practice of thoroughly cooking fish prior to consumption could be promoted and lead to eradication of D. renale infection in humans.
Dioctophyme renale, commonly referred to as the giant kidney worm, is a parasitic nematode (roundworm) whose mature form is found in the kidneys of mammals. D. renale is distributed worldwide, but is less common in Africa and Oceania. It affects fish eating mammals, particularly mink and dogs. Human infestation is rare, but results in kidney destruction, usually of one kidney and hence not fatal. A 2019 review listed a total of 37 known human cases of dioctophymiasis in 10 countries with the highest number (22) in China. Upon diagnosis through tissue sampling, the only treatment is surgical excision.
Dioctophyme renale o Dioctophyma renale es considerado el más grande de los nemátodos parásitos, comúnmente conocido como el "gusano gigante de riñón". Ha sido descrito fundamentalmente en mustélidos y cánidos: visón, lobo, perro, hurón, nutria, zorro, perro vinagre, oso, cerdo, rata, foca, y, accidentalmente en el hombre.
Aunque D. renale es un parásito cosmopolita, se distribuye con menos frecuencia en África y Oceanía. Los casos humanos son debidos al consumo crudo de peces o ranas importados desde Oriente, principalmente en regiones en torno al Mar Caspio, como Irán. Aunque las infecciones en humanos se producen muy raramente, son más comunes en zonas de clima templado.
La prevalencia puede ser alta en regiones donde existen poblaciones de visón, tales como porciones de Ontario o Minnesota. En España el mayor número de casos se han hallado en perros, sobre todo en provincias como Granada, Murcia o Madrid.
Los gusanos machos adultos miden unos 20-40 cm de largo y 5-6 mm de ancho, sin embargo la hembra puede alcanzar de 60 a 100 cm de longitud x 7 mm de anchura. Ambos sexos aparecen de color rojo brillante en color y forma cónica. Los huevos que contienen el embrión miden alrededor de 60-80 micrómetros x 39 a 47 micrómetros, de forma ovalada y tono café amarillo. Los huevos tienen una cáscara gruesa con una superficie característica.
Los huevos producidos por la hembra pasan a la orina y son, sucesivamente, expulsados en ambiente hídrico donde sufren modificaciones. En agua la L1 se desarrolla en una semana y ésta es ingerida por su hospedador intermedio, Lumbriculus variegatus, donde evoluciona hasta L3. El hospedador definitivo se infecta ingiriendo el anélido (L. varientus) infectado, o uno de sus depredadores (peces, ranas).
La larva, una vez que ha llegado, de este modo, al intestino del perro o de otro hospedante definitivo (accidentalmente al hombre), supera la barrera intestinal y se localiza en la pelvis renal, donde tendrá lugar la producción de huevos, de tal manera que éstos viven normalmente en la pelvis renal, en los uréteres y en la vejiga, aunque a veces pueden encontrarse en la cavidad peritoneal, nódulos subcutáneos, etc.
Solamente la localización renal lleva a la eliminación de huevos con la orina. Las restantes ubicaciones ectópicas son "sin salida". SALVADOR, F. (18Feb2014). «Dioctophyma renale, ubicación aberrante del parásito adulto.» (Artículo). En Unidad de Ecografía., ed. Artículo. Buenos Aires: Hospital Escuela. FCV. UBA. Archivado desde el original el 4 de marzo de 2016. Consultado el 19Feb2014. «Dioctophyma renale».
Los individuos con infección por Dioctophyma renale presentan síntomas inespecíficos que incluyen hematuria (sangre en orina), nefritis, dolor lumbar, ampliación renal y / o cólico a causa de la destrucción del parénquima renal. En algunos casos, la fibrosis que se produce después de la infección por el parásito es un hallazgo realizado mediante en ecografía o tomografía computarizada, imitando el cáncer renal, lo que lleva a la nefrectomía radical.
El parénquima renal va siendo completamente destruido a medida que los parásitos se desarrollan hasta que prácticamente sólo permanece la cápsula renal, que envuelve a los Dioctophyma, pero los gusanos adultos normalmente sólo afectan a un riñón (derecho), por lo que el riñón no infectado suele ser capaz de suplir la función renal. Sin embargo, la inflamación del parénquima puede llevar a la muerte en circunstancias extremas. «Dioctophyma renale». «sangre en la orina (hematuria)».
La única forma de obtener un diagnóstico definitivo es a través de la identificación de huevos de D.renale en la orina de un paciente cuando el parásito está en la sede renal. Sin embargo, la obtención de los antecedentes del paciente (es decir, si el paciente ha consumido pescado poco cocido o crudo de agua dulce) es un primer paso importante que se puede complementar con los exámenes radiológicos. Probablemente debido a la rareza de los casos humanos, no existe un tratamiento estándar para D. renale. El único medio conocido es la extirpación quirúrgica de cualquiera de los gusanos adultos o el riñón infectado. La nefrectomía es generalmente considerada extrema de los casos humanos.
No permitir que el perro se alimente con peces de agua dulce si antes no se han cocido suficientemente.
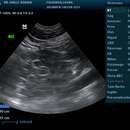
 Ecografía de riñón derecho en canino hembra infestado con D. renale.
Ecografía de riñón derecho en canino hembra infestado con D. renale. Dioctophyme renale o Dioctophyma renale es considerado el más grande de los nemátodos parásitos, comúnmente conocido como el "gusano gigante de riñón". Ha sido descrito fundamentalmente en mustélidos y cánidos: visón, lobo, perro, hurón, nutria, zorro, perro vinagre, oso, cerdo, rata, foca, y, accidentalmente en el hombre.
Dioctophyme renale, aussi appelé « strongle géant »[1], « eustrongle géant »[2] ou « ver rénal géant »[3],[4],[5] est une espèce de nématodes parasites dont la forme adulte infecte les reins des mammifères. D. renale est trouvé dans le monde entier[6]. Il affecte en particulier les visons et les chiens. L'infection humaine est rare : 37 cas humains de dioctophymiose étaient connus en 2019[7]. Ces 37 cas étaient répartis dans dix pays d’Asie, d’Europe, d’Amérique du Nord et d’Océanie, le nombre le plus élevé étant en Chine (22 cas)[7]. La maladie peut provoquer la destruction des reins. Le traitement est l'exérèse chirurgicale.
Dioctophymosis[8], Dioctophyme renalis[9],[10], Eustrongylus gigas[11], Ascaris gigas renale.
Dioctophyme renale est connu depuis au moins 1583[12]. Presque deux siècles plus tard, en 1782, Johann Goeze fait la première description scientifique[13] de D. renale. La famille Dioctophymidae n'a qu'un seul genre (Dioctophyme), et le nom du genre (avec la possibilité d'être Dioctophyma) a été débattu pendant deux cents ans. Le problème a finalement été résolu par la Commission Internationale de Nomenclature Zoologique en 1989.
En 2003, des œufs de D. renale ont été découverts dans six coprolithes du site néolithique de l'Arbon-Bleiche 3, en Suisse. Cet emplacement est situé près d'un lac, qui a probablement fourni aux premiers humains l'accès à l'eau douce, les poissons et les grenouilles. Les échantillons ont été datés entre -3384 et -3370, et prouve que la prévalence de cette infection était plus élevée au début de l'histoire humaine, avant la mise au point des bonnes techniques de cuisson[14].
Les personnes ou animaux infectés présentent généralement des symptômes non spécifiques, y compris une hématurie (du sang dans les urines), une néphrite, des douleurs rénales, un gonflement rénal, et/ou une colique néphrétique (douleur intermittente dans la région des reins) due à la rare migration des vers à travers les uretères. Dans certains cas, la fibrose survenant après une infection parasitaire est découverte fortuitement à l'échographie ou à la tomodensitométrie. Si elle est prise pour un cancer du rein, une néphrectomie radicale risque d'être réalisée[15].
Les vers adultes infectent souvent un seul rein (le droit). Le rein est détruit par fibrose. La dysfonction rénale est généralement limitée car l'autre rein compense. Cependant, l'inflammation du parenchyme peut conduire à la mort dans des circonstances extrêmes.
Le Dioctophyme renale adulte réside dans le rein (généralement le rein droit). Les femelles produisent des œufs qui passent dans l'urine. Dans les milieux aquatiques, les œufs développent un embryon après 15-100 jours. Ces œufs sont ingérés par un oligochète (ver) aquatique. Ils éclosent et pénètrent dans les vaisseaux sanguins, puis se développent en trois stades larvaires. Un hôte paraténique[16] (souvent un poisson ou une grenouille) peut alors ingérer l'oligochète. Cet hôte paraténique est ensuite consommé par un hôte définitif, où les jeunes pénétrent la muqueuse intestinale et migrent vers le foie. Après une phase de maturation d'environ 50 jours, les juvéniles migrent alors vers un rein (généralement le rein droit). Après maturation, ils peuvent vivre pendant cinq ans[17].
Les hôtes définitifs sont des mammifères carnivores, notamment les visons[18],[19], les grisons[20], les loups, les coyotes, les renards des savanes[21], les chiens[22], les ratons laveurs, les belettes, les ours, plus rarement les bœufs, les porcs, et les humains.
La transmission à l'homme se produit généralement après l'ingestion de poissons d'eau douce ou de grenouilles crus ou pas assez cuits.
D. renale est le plus grand des nématodes à parasiter l'homme. L'adulte mâle mesure de 20 à 40 cm de long et de 5 à 6 mm de large; les femelles peuvent atteindre 103 cm de longueur avec une largeur de 10 à 12 mm. Ils sont rouge vif. Tant les extrémités antérieures que postérieures sont coniques. Les vers mâles ont une bursa, pour faciliter l'accouplement.
Les œufs sont ellipsoïdes de 60 à 80 micromètres x 39-47 micromètres, brunâtres/jaunes, contiennent un embryon, et ont une épaisse coquille perforée caractéristique.
Le diagnostic définitif se fait par l'identification des œufs dans les urines du patient. Toutefois, l'historique du patient (c'est-à-dire, si le patient a consommé crus ou insuffisamment cuits des poissons d'eau douce) est une première étape importante qui peut être couplée avec des examens radiologiques des reins. L'analyse d'urine va probablement montrer une hématurie. Les tests sanguins peuvent révéler une éosinophilie.
Probablement à cause de la rareté des cas humains, il n'existe pas de traitement standard pour l'infection chez les humains. Le seul traitement reconnu est l'exérèse chirurgicale des vers adultes ou du rein entier (néphrectomie)[23] dans les cas extrêmes.
Un médecin aurait utilisé de l'Ivermectine pour traiter un patient, qui a été effectivement guéri[réf. souhaitée]. L'utilisation d'antihelminthiques n'a pas encore été évalué pour traiter cette infection.
Même si D. renale est distribué dans le monde entier, bien que nettement moins fréquent en Afrique et en Océanie, l'infection humaine est extrêmement rare. Les régions autour de la Mer Caspienne ont le plus grand nombre de cas, la plupart ayant eu lieu en Iran. Les infections sont communes dans les zones où les poissons d'eau douce sont un pilier de l'alimentation.
Les infections non-humaines sont plus fréquentes dans le monde entier, en particulier dans les zones de climat tempéré. La prévalence dans les populations de visons peut être élevée, comme en Ontario ou au Minnesota. La prévalence chez les carpes peut atteindre 50%.
Aucune mesure de santé publique n'a été entreprise, ni aucun vaccin mis au point, à cause de la rareté de l'infection de l'homme. La simple pratique de bien cuire le poisson pourrait conduire à l'éradication de l'infection chez les humains.
Dioctophyme renale, aussi appelé « strongle géant », « eustrongle géant » ou « ver rénal géant »,, est une espèce de nématodes parasites dont la forme adulte infecte les reins des mammifères. D. renale est trouvé dans le monde entier. Il affecte en particulier les visons et les chiens. L'infection humaine est rare : 37 cas humains de dioctophymiose étaient connus en 2019. Ces 37 cas étaient répartis dans dix pays d’Asie, d’Europe, d’Amérique du Nord et d’Océanie, le nombre le plus élevé étant en Chine (22 cas). La maladie peut provoquer la destruction des reins. Le traitement est l'exérèse chirurgicale.
Dioctophyme renale is een rondwormensoort uit de familie van de Dioctophymidae. De wetenschappelijke naam van de soort is voor het eerst geldig gepubliceerd in 1782 door Goeze.
Bronnen, noten en/of referenties''Dioctophyma renale'' é um parasita do rim de mamíferos.[1][2][3] D. renale ocorre no mundo inteiro, mas é menos comum na África e Oceania.[4] Infecta mamíferos pscívoros, especialmente o vison[1] e cães.[4] Infestação em humanos é rara, mas caso aconteça, ela pode destruir os rins. O único tratamento é a remoção cirúrgica dos vermes.
''Dioctophyma renale'' é um parasita do rim de mamíferos. D. renale ocorre no mundo inteiro, mas é menos comum na África e Oceania. Infecta mamíferos pscívoros, especialmente o vison e cães. Infestação em humanos é rara, mas caso aconteça, ela pode destruir os rins. O único tratamento é a remoção cirúrgica dos vermes.
Palissadmask (Dioctophyme renale[1] tidigare Eustrongylus visceralis eller Eustrongylus gigas) är en rundmask av familjen Dioctophymidae.
Kroppen är cylindrisk med en rad palissadformig anordnade papiller längs bägge sidolinjerna och sex tydliga munpapiller. Honan kan bli ända till en meter lång, hanen 40 centimeter. Palissadmasken lever i njurbäckenet hos sälar och flera rovdjur samt nötboskap, men kan även leva hos människor. Laverna lever främst hos fiskar.
Palissadmask (Dioctophyme renale tidigare Eustrongylus visceralis eller Eustrongylus gigas) är en rundmask av familjen Dioctophymidae.
Kroppen är cylindrisk med en rad palissadformig anordnade papiller längs bägge sidolinjerna och sex tydliga munpapiller. Honan kan bli ända till en meter lång, hanen 40 centimeter. Palissadmasken lever i njurbäckenet hos sälar och flera rovdjur samt nötboskap, men kan även leva hos människor. Laverna lever främst hos fiskar.